
| ��һ�� | �ڶ��� | ������ | |
| ��ȡ�Ͻ������/g | 10 | 10 | 20 |
| ����ϡ���������/g | 60 | 80 | 50 |
| ��������������/g | 0.2 | 0.2 | ��0.2 |
���� ��1�����ݵ�һ��ʵ���������������������ȡ�õ�ϡ������Ͻ���Ʒ��������������Ͻ���п��������
��2��������ʵ�����ݿ�֪�������η�Ӧ��п����������Ϊ�����η�Ӧ���������������ǡ��Ϊ0.2g�����Ե�һ�η�Ӧ�кϽ��е�п��ϡ����ǡ����ȫ��Ӧ���Ӷ��ó����ǵ������ȣ�
��3�����ݣ�1���л�ѧ����ʽ�ı�����ϵ��������ʵ����������������غ�ó���Һ�����������빫ʽ�������ǡ����ȫ��Ӧ��������Һ�����ʵ�����������
��� �⣺��1����Ͻ���п������Ϊx����������п����Ϊy
Zn+H2SO4�TZnSO4+H2��
65 161 2
x y 0.2g
$\frac{65}{x}$=$\frac{161}{y}$=$\frac{2}{0.2g}$
x=6.5g
y=16.1g
�Ͻ���п����������Ϊ��$\frac{6.5g}{10g}$��100%=65%��
��2��������ʵ�����ݿ�֪�������η�Ӧ��п����������Ϊ�����η�Ӧ���������������ǡ��Ϊ0.2g�����Ե�һ�η�Ӧ�кϽ��е�п��ϡ����ǡ����ȫ��Ӧ�������Ͻ��������ϡ�����������Ϊ1��5ʱǡ�÷�Ӧ��ȫ��
��3�����ݣ�1���ó�������������п������Ϊ16.1g��
������Һ������Ϊ��Ӧǰ����Ͻ�����������֮�ͼ�ȥ����������������
������Һ��ZnSO4������������$\frac{16.1g}{6.5g+50g-0.2g}$��100%=28.6%
��������Һ��ZnSO4����������Ϊ28.6%��
�ʴ�Ϊ����1��65%��
��2��1��5��
��3��28.6%��
���� ������Ҫ����ѧ������ͼ�����ݺ��ݻ�ѧ����ʽ���м����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ë���ڻ��������գ����ŵ�����ëζ��˵����ë�к��е����� | |
| B�� | ���ڰڶ�ʱ�������߶�Խ��Խ�ͣ�˵�����ֻ�е��ת��Ϊ������ʽ���� | |
| C�� | �μ�BaCl2��Һ���а�ɫ�����������Һ��һ����CO32- | |
| D�� | ���ۺ���ǻ�ϼ��Ⱥ��������������������˵�������˻�ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ɱ����� | B�� | ����ե֭ | C�� | ����ȼ�� | D�� | ��ѩ�ۻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ۢڢܢ� | C�� | �ڢۢ� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���嶡�����ӵĸ�Ԫ��������Ϊ10��14��1 | |
| B�� | ���嶡���������������������ӹ��� | |
| C�� | ���嶡���������ھƾ��γɵľƾ���Һ���������ȱ��������������������嶡������ | |
| D�� | ���嶡�������е�̼Ԫ�ص���������Ϊ80% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
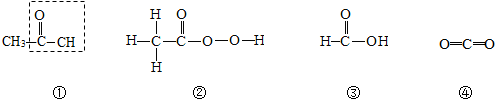
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | ���� | ���� |
| ��ȡ1.44g��ɫ����װ���Թܣ�����������ϡ���ᣬ��ַ�Ӧ | ��ɫ���岿�ּ��٣���Һ��Ϊ��ɫ | ����ٴ��� |
| �ڹ����Թ��в����ĺ�ɫ���壬ϴ�Ӹ����������Ϊ1.04g | / | �������ȷ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com