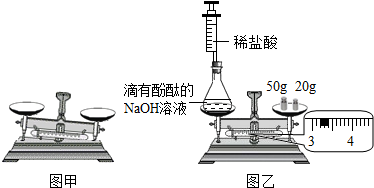
酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这几类化合物进行了一系列的探究活动.
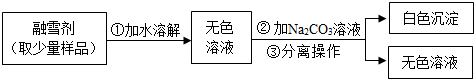
(1)盐酸、硫酸等具有相似的化学性质,是因为二者的水溶液中都含有
离子.打开盛浓盐酸和浓硫酸的试剂瓶的瓶盖,立即就能把它们区分开来,这是因为
.
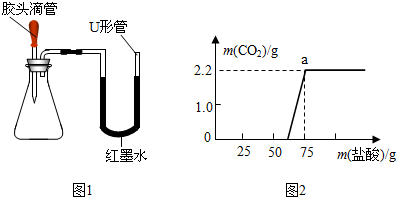
(2)如图1是甲同学设计的趣味实验装置,其气密性良好.若胶头滴管中的物质是浓NaOH溶液,锥形瓶中充满CO
2,则挤压胶头滴管后能观察到什么现象?
,并写出有关反应的化学方程式
.
(3)盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末.乙同学和丙同学对这种白色粉末的成分进行了如下猜想和验证.
(Ⅰ)可能是NaOH(Ⅱ)可能是Na
2CO
3(Ⅲ)可能是NaOH与Na
2CO
3的混合物
①乙同学向所取少量粉末中滴加
溶液,观察到
的现象后,排除了(Ⅰ)的可能性.
②丙同学提议用酚酞试液来鉴定,你认为可行吗?请简要说明理由:
.
(4)某同学称取13.3g 的NaOH样品(杂质为Na
2CO
3),加水配成溶液100g,然后向溶液中逐滴加入稀盐酸,根据生成CO
2的质量测定Na
2CO
3的质量.
实验测得加入稀盐酸的质量与产生CO
2气体的质量关系如图2所示.
①求完全反应后生成的二氧化碳的质量是
g.
②求样品中Na
2CO
3的质量分数?(要求写出计算过程,结果精确到0.1%)
③假如此反应恰好完全,则所得溶液中溶质的质量分数是多少?(要求写出计算过程,结果精确到0.1%)