
【题目】氢氧化钾是工业强碱之一,与氢氧化钠化学性质相似。一次化学实验后同学忘记盖瓶塞。化学兴趣小组同学想探究该瓶氢氧化钾固体是否变质。大家展开充分讨论,邀你参与。
(猜想)A、没有变质
B、部分变质
C、完全变质
(1)氢氧化钾在空气中变质的原因____(用方程式表示)。
(査阅资料)氯化钾溶液和氯化钙溶液呈中性。
(2)设计甲、乙两组实验方案并完成实验取瓶中固体少许,加水溶解配成溶液,分装于两支洁净试管。
实验方案 | 实验操作 | 实验现象 | 实验结论 |
甲 | 取一支试管,滴入无色酚酞试液,振荡 | 溶液变红色 | 猜想A正确 |
乙 | 取另一支试管,滴入足量的氯化钙溶液充分反应后再滴入几滴硫酸铵试液 | 先有___产生 再有____产生 | 猜想B正确 |
(3)(相互交流)大家认为甲的方案不可信,请你说出理由_____。滴入硫酸铵后发生的化学反应方程式_____。
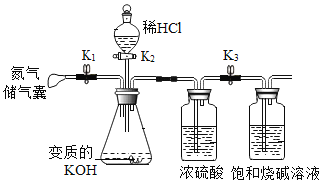
(4)如果B猜想是正确的,大家想继续探究该瓶氢氧化钾固体中KOH的质量分数。设计了下列实验。
(操作步骤)①首先称量出饱和烧碱溶液(含仪器)的质量m1再与前面装置连接。
②按正确方法检查装置气密性,气密性良好。
③关闭K2,打开K1和K3,挤压N2储气囊给装置充分充气。
④关闭K1,打开K2滴入足量稀HCl,充分反应。⑤关闭K2,打开K1再次挤压N2储气囊,给装置充分充气。⑥关闭K3取下盛装烧碱的装置,称量质量为m2。回答问题:
(Ⅰ)步骤③充入N2的目是_____。
(Ⅱ)浓硫酸的作用是_______。
(Ⅲ)若不进行步骤⑤,KOH质量分数(偏大或偏小)____。
【答案】![]() 先有白色沉淀产生 后有剌鼻性气体放出 碳酸钾溶液也显碱性,能使酚酞试液变红色
先有白色沉淀产生 后有剌鼻性气体放出 碳酸钾溶液也显碱性,能使酚酞试液变红色 ![]() 排除装置中的空气(或排除装置中的二氧化碳) 干燥二氧化碳 偏大
排除装置中的空气(或排除装置中的二氧化碳) 干燥二氧化碳 偏大
【解析】
(1)氢氧化钾与氢氧化钠化学性质相似,氢氧化钾在空气中变质的原理与氢氧化钠在空气中变质的原理相似,即吸收空气中的二氧化碳生成碳酸盐和水,反应的化学式为:
![]() ;
;
(2)氯化钙和碳酸钾反应,生成白色沉淀碳酸钙,实验现象是有白色沉淀产生;滴入硫酸铵之后,氢氧化钾与硫酸铵反应生成硫酸钾、氨气和水,氨气是有刺激性气味的气体;
(3)碳酸钾溶液呈碱性,同样可以是无色酚酞变成红色,不能区分此处是氢氧化钾还是碳酸钾;氢氧化钾与硫酸铵反应生成硫酸钾、氨气和水,反应的化学方程式为:
![]() ;
;
(4)(Ⅰ):氮气性质稳定,不与实验装置中的氢氧化钾、碳酸钾和氢氧化钠反应,在装置中充入氮气,把实验装置中的空气(主要是二氧化碳)排除干净,可以使实验结果更加精准;
(Ⅱ):浓硫酸具有吸水性,可以吸收反应中生成的水,使二氧化碳气体在通过浓硫酸瓶后成为干燥的二氧化碳气体;
(Ⅲ):按压氮气气球,使氮气将装置中反应生成的二氧化碳全部与饱和的烧碱溶液反应,这样可以根据生成的二氧化碳的质量来计算混合物中碳酸钾的质量,如果不采取步骤⑤,实验装置中有二氧化碳存在,计算得出的碳酸钾质量偏小,相应的氢氧化钾的质量偏大。


科目:初中化学 来源: 题型:
【题目】如下图所示,将少量液体 X加入到广口瓶中,关闭活塞,液体 X和固体Y 因发生化学变化而使a侧液柱低于b侧液柱的组合是( )
① | ② | ③ | ④ | |
X | 水 | 水 | 双氧水 | 稀盐酸 |
Y | NH4NO3 | NaOH | MnO2 | Na2CO3 |
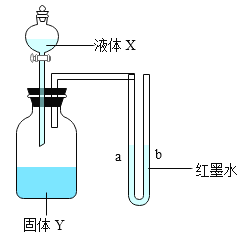
A.①②③B.②③④C.①②D.③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如下图所示。
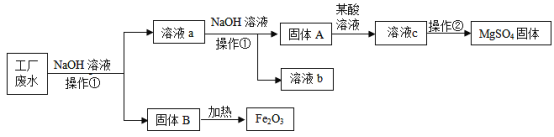
回答下列问题:
(1)操作①的名称是_____________,操作②时,当___________________时,即可停止加热。
(2)写出固体A与某酸溶液反应的化学方程式为________________。
(3)固体B加热的产物是两种常见氧化物,写出该反应的化学方程式为:________。
(4)溶液b除了可能含有NaOH外,还一定含有的溶质是___________(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气中氧气含量测定的再认识.
Ⅰ.(实验回顾)如图是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
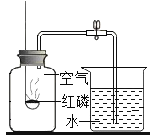
(1)写出红磷燃烧的化学方程式________________,现象是_________.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
(问题提出)有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
Ⅱ.(实验改进)
根据铁在空气中生锈的原理设计如图实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.测得实验数据如表
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
(交流表达)
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式_________.
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是_____(计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是___________;(写一条)
III.四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数,反应原理为:2Na2S4+O2+2H2O═8S↓+4NaOH
(查阅资料)①Na2S4受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢.
②硫代硫酸钠(Na2S2O3)可溶于水,常温下与NaOH溶液不反应.
③NaOH溶液可吸收硫化氢和二氧化碳.
(实验过程)
①取0.5g碳酸钠、0.2g硫粉混合后置于试管中,加入(如图①所示,夹持装置已略去),制得Na2S4,反应为:4Na2CO3+12S+X![]() 2Na2S4+2Na2S2O3+4CO2,X的化学式为___________;
2Na2S4+2Na2S2O3+4CO2,X的化学式为___________;
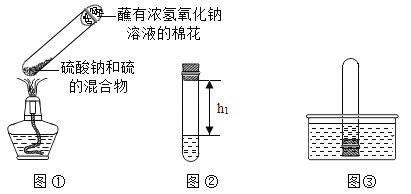
②冷却后,取下棉花,放置一段时间,再向该试管中加入10mL水,迅速塞紧橡胶塞,充分振荡.测量液面至橡胶塞下沿的距离,记录数据h1(如图②所示);
③将该试管插入水中(如图③所示),拔下橡胶塞,观察到_________,塞紧橡胶塞.将试管取出,倒转过来,测量液面至橡胶塞下沿的距离h2,记录数据h2.理论上h2:h1=___________;
④(反思与评价)实验过程①中要塞氢氧化钠溶液的棉花的原因是___________;若实验过程②中,冷却取下棉花后,未放置一段时间即进行后续操作,测定结果_________(填“偏大”、“偏小”或“无影响”),理由是:_______________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某化学反应的微观示意图,下列说法正确的是( )
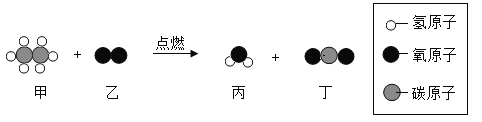
A.该反应属于置换反应B.该反应前后原子数目发生了变化
C.反应物甲中碳和氢元素的质量比为1:3D.反应生成的丙和丁的分子个数比为3:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图回答有关问题
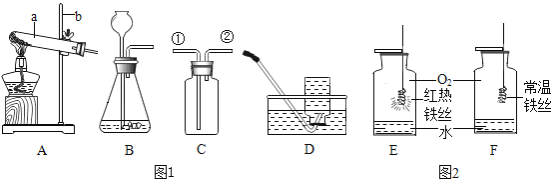
(1)写出图1中标号仪器的名称:b_____。
(2)若用A装置制取氧气,用D装置收集完氧气后,应先将导管从水中移出再熄灭酒精灯,其目的是防止_____。制得的氧气用来做如图2所示的实验,发现F中铁丝不燃烧,其原因是_____,写出E中反应的化学方程式_____。
(3)实验室制取二氧化碳的化学方程式为_____,其发生装置可选图1中的_____(填序号),若用装置C收集二氧化碳,则气体应从_____(填“①”或“②”)端进入。
(4)实验室用15.8g高锰酸钾最多可制得氧气多少g?_____(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】依据下列实验室制取气体的发生和收集装置回答下列问题。
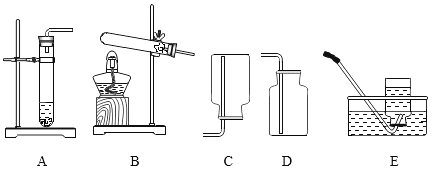
(1)实验室制取二氧化碳的化学方程式是_____;
(2)选择D为收集二氧化碳的装置是因为二氧化碳_____。
为研究实验室制取二氧化碳的适宜条件,进行如下实验。
实验编号 药品 | 甲 | 乙 | 丙 | 丁 |
1g大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
10g盐酸(过量) | 10%盐酸 | 30%盐酸 | 10%盐酸 | 30%盐酸 |
(3)实验甲与实验_____对照,是为了研究固体反应物颗粒大小对反应速率的影响。
(4)上述实验中,另一个影响反应速率的因素是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人们曾用贝壳(主婴成分是碳酸钙,杂质不参与反应且不溶于水) 和纯碱为原材料制取烧碱,制取流程如图所示。
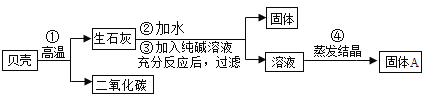
(1)写出步骤①的反应化学方程式_____
(2)固体 A 的成分可能是纯净的氢氧化钠,还可能是_________、_____(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com