
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铝是地壳里含量最多的元素,铝合金的密度一般都比较小 | |
| B. | 合金的硬度一般比组成它们的纯金属更高 | |
| C. | 铁在潮湿的空气中比在干燥的空气中更易生锈 | |
| D. | 在金属表面涂油漆能防止金属生锈 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
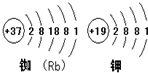 阅读下列材料,回答有关问题.
阅读下列材料,回答有关问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酒精挥发,木材燃烧 | B. | 干冰易升华,苹果腐烂 | ||
| C. | 粉碎矿石,铁能生锈 | D. | 分离空气制氧气,火药爆炸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该物质的一个分子中含 25 个原子 | |
| B. | 该物质的相对分子质量为 296 | |
| C. | 该物质中各元素的质量比为 C:H:N:S:O=2:4:2:1:4 | |
| D. | 该物质是由碳、氢、氮、硫、氧五种元素组成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
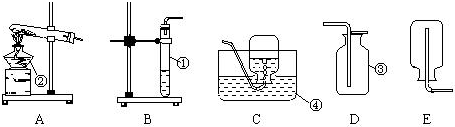
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
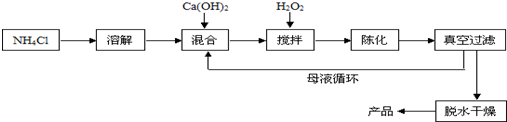
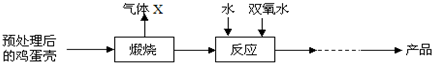
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com