
����Ŀ����ͼ��ʵ������ȡ����ij��������������Ҫ����գ�
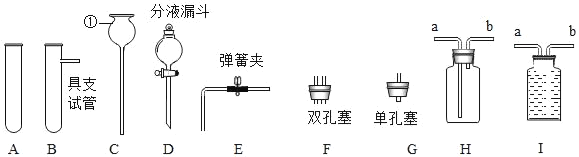
��1��ͼ�������ٵ�������_____��
��2��ʵ������ȡ������̼�Ļ�ѧ����ʽΪ_____����Ҫ��װһ���Ʊ�������̼���岢����ʱ����Һ��ҩƷ�ķ���װ�ã���ѡ��ͼ�е�B��_____������ϣ�����ĸ��������Hװ���ռ�������̼������Ӧ��_____��ͨ�룬ԭ����_____��
��3������ͼ2��������װһ���Ʊ�O2���ܿ��Ʒ�Ӧ���ʷ���װ�ã���ѡ��ͼ�е�A��_____������ϣ�����ĸ������Ӧ�Ļ�ѧ����ʽΪ_____��
��4������Iװ���ռ��������뽫ͼI���ռ�װ�ò���������
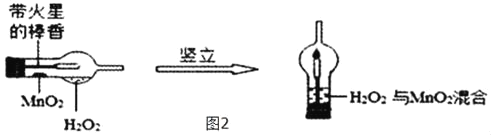
��5��ʵ�鴴������ѧ����Ϊ��Ҫ�Ŀ�ѧ��������ͼ��ijѧУʦ����MnO2��H2O2�ֽ�ʵ��װ�õĴ����������ʵ��������£��ٽ�һ֧���θ����ˮƽ���ã��õι���ȡ3mL���ܶ�Ϊlg/mL����������Ϊ5%��H2O2��Һ�������ܵ������ڣ�����ҩ��ȡ0.2g MnO2��ĩ�����ڸ���Ľ����ܵĹܱ��ϣ��ڵ�ȼ�����Ϲ̶��İ������������ܲ������������۲쵽�����ǵİ���_____����ʵ��װ�ô��ڵ��ŵ���_____ ����һ�㼴�ɣ���
���𰸡�����©�� CaCO3+2HCl=CaCl2+H2O+CO2�� CG��DG a ������̼���ܶȱȿ����� DEF ![]() ���ϸ�ȼ ��ԼҩƷ
���ϸ�ȼ ��ԼҩƷ
��������
��1����ͼ��֪�����ٵ������dz���©����
��2��ʵ������ȡCO2�����ڳ����£��ô���ʯ��ʯ��ʯ��ϡ������ȡ�ģ�̼��ƺ����ᷴӦ�����Ȼ��ƺ�ˮ�Ͷ�����̼����ѧ����ʽΪ��CaCO3+2HCl=CaCl2+H2O+CO2������˲���Ҫ���ȣ���Ҫ��װһ���Ʊ�������̼���岢����ʱ����Һ��ҩƷ�ķ���װ�ã���ѡ��ͼ�е�B��CG��DG������ϣ�����Hװ���ռ�������̼������Ӧ�ӳ��ܽ��룬��Ϊ������̼���ܶȱȿ�����
��3������ͼ2��������װһ���Ʊ�O2���ܿ��Ʒ�Ӧ���ʷ���װ�ã���ѡ��ͼ�е�A��DEF�����������ڶ�������������������������ˮ����������ѧ����ʽΪ��![]() ��
��
��4��I��װ��ˮ���ռ�����Ҫ�Ӷ̽��룬��Ϊ�������ܶȱ�ˮС����ͼ�� ��
��
��5���۲쵽�����ǵİ������ϸ�ȼ����Ϊ���������ɣ���ʵ��װ�ô��ڵ��ŵ��ǽ�ԼҩƷ�ȡ�


 ��������ϵ�д�
��������ϵ�д� ��ӡ�Ļ���ʱ����ϵ�д�
��ӡ�Ļ���ʱ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���û�ѧ���źͻ�ѧʽ��ʾ��������������_____������������Ԫ�ػ��ϼ�_____�����������Ҫ�ɷ�_____����ͯȱ��_____Ԫ������ʱ��������Ͳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����9�֣�ij��ѧС��������ͼ��ʾװ�ã�ͼ�й̶�װ������ȥ���ⶨͭп�Ͻ���п������������
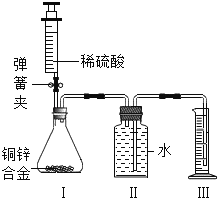
̽���������£�
������ʵ��װ�ò����װ�������ԣ�
����װ�����е���ƿ����2��0g��ͭп�Ͻ���Ʒ��ĩ����ע��������ע��ϡ���ᣬ������ƿ�в��ٲ�������ʱ��ȷ��ȡע�����ڶ���������10��5mLϡ���ᣬͬʱ�����н����ɼУ��Ƴ�װ�����еĵ��ܣ�ȷ��ȡ��Ͳ��ˮ�����Ϊ214��0mL����ע����Ʒ�е����ʲ��μӷ�Ӧ��
��װ������ʣ��������ʾ����ʵ�������ȷ����������1��4g��
����С�����λͬѧ����ʵ����̲�ò�ͬ���ݣ�����ͭп�Ͻ���Ʒ��п������������
��ͬѧ����װ�����з�Ӧǰ�������������м��㣻
��ͬѧ����װ�����м���ϡ����������м��㣻
��ͬѧ����װ��������ȡˮ��������м��㣬����ã��ڱ�״���£��������ܶ�Ϊ0��09g/L��
�ش��������⣺
��1��װ�����з�Ӧ�Ļ�ѧ����ʽΪ ��ʵ������������ϡ���������ٲ������壬Ŀ���� ��
��2���������г���ʣ�����֮ǰ����ȷ������ ��ϴ�ӡ����
��3������ʵ��ⶨ�����ݣ�������λͬѧ�� ����������������������������ͬѧ�����м�����Ʒ��п������������
��4����ѧС��ͬѧ���֣����ձ�ͬѧ�ķ������м��㣬��ʹʵ�������ֽϴ�ƫ��������ؿ������ƫ����� �����ţ���
A���Ƴ�װ����ʱ��������������һ����ˮ
B��ʵ�����ǰ��û���ų�װ�����еĿ���
C�����ݴ���ʱ��δ�ų�����ϡ������ռ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ���о�����ԭ����ijС����CO��Fe2O3��Ӧ����ʵ��.
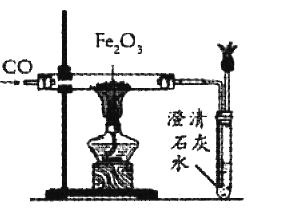
��1����ʵ�鿪ʼʱ��Ҫ��ͨһ���һ����̼�ټ��ȣ���Ŀ����____________________.
��2��Ӳ�ʲ������ڷ�����Ӧ�Ļ�ѧ����ʽ��____________________.
��3����Ӧ����ʱ��Ӧ�ȳ��ƾ��ƣ�����ͨCO����������ȴ��Ŀ����______________________.
��4����װ�õIJ���֮����______________________
��5����Ӧֹͣ��ͬѧ�Ƕ���ȴ�������ڹ������ʵ���ɳɷֲ�������Ȥ����ҷ�����Լ��IJ���.�뽫��IJ���д����
����һ��____________________.
�������____________________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���������Ȼ��ط�ĩ���������ʿ������Ȼ��ơ�����ء�����ơ��Ȼ�ͭ��̼�����е�һ�ֻ��֡�Ϊȷ����ɷ֣�ij��ȤС���ͬѧ�ǽ�������ʵ�飺
��1��ȡ�����÷�ĩ���ձ��У�������ˮ����ֽ��裬����ɫ������Һ��
��2��ȡ������ɫ��Һ�������Թ��У��μ��Ȼ�����Һ�а�ɫ�������ɡ�
��3������ȡ14.9g�÷�ĩ���ձ��У���������ˮ�ܽ⣬�ټ�����������������Һ��ϡ���ᣬ��ַ�Ӧ������28.7g��ɫ������
����������Ϣ�ش�
�ɣ�1����֪��������һ��û��_____���ɣ�2����֪��������һ������_____���ɣ�3����֪��������һ������_____�������в���ȷ������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ᩁ����������BaCl2��ų��ж�����H2S����ˮ��Һ�����ԣ�������NaOH��Һ����H2S��ȡNa2S�������ֳƳ�����մƼ�����з�Ӧ�Ļ�ѧ����ʽΪ��H2S+2NaOH��Na2S+2H2O
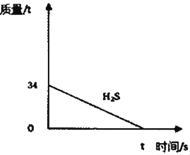
��1����ij������ÿ��Ҫ����34��H2S������������������Һ�е�����NaOH���ٶ�_____����д��������̣�
��2����ͼ�Ѿ���������34��H2S�������仯���ߣ�����ͼ�л���������Na2S�����ı仯���ߣ������������ϱ�����Ӧ������_____��
��3�������ǻ���H2S���յĸ��������ɱ���
��Ŀ | ���ۣ���Ԫ/�֣� |
NaOH | 0.25 |
Na2S | 0.5 |
�������ã��Դ���1��H2S�ƣ� | 0.12 |
��ҵ����β���迼�Ǿ���Ч������Ч�棬�����������Ϸ��������Ӿ���Ч�濼�����ִ���34��H2S�ķ�����ӯ��_____��Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ա�ʵ���ǻ�ѧ�о��о������õķ�������ѧ��ȤС���ͬѧΪ�о�CO2ͨ��NaOH��Һ�Ƿ����˷�Ӧ,���������ʵ�顣��ͻ�ѧ��ȤС���ͬѧһ��̽�����ش����⣺
�������ʵ�飩
ʵ�� | ʵ�鲽��һ | ʵ�鲽��� | ʵ�� | ʵ�鲽��һ | ʵ�鲽��� |
ʵ��I |
|
| ʵ��II |
|
|
��̽������ۣ�
(1)ʵ��I�в���һ������Ӧ�Ļ�ѧ����ʽ��____________________________�������������������________________��
(2)ʵ�����в����������Ӧ�Ļ�ѧ����ʽ��____________________________��
CaCl2��ҺҲ������______(�����)����ﵽʵ��Ŀ�ġ�
A���ᱵ��Һ B�Ȼ�����Һ
C̼�����Һ D��������Һ
(3)ʵ�������,����ͬѧ�������ͨ������CO2��NaOH��Һ�еμ���ɫ��̪,�ж������Ƿ�����Ӧ��������С��ͬѧ��,ԭ����____________________________��
���������ϣ�
���� | �ܽ�ȣ�s��/g |
NaOH | 17.3 |
Na2CO3 | ��0.01 |
(4)ͬѧ���ڲ������Ϻ��������ʵ��������CO2ͨ��NaOH�ľƾ���Һ�����۲쵽____________������֤������ȷʵ�����˷�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2��O2��N2�Ļ������20�ˣ���ȼ��ȫ��Ӧ������18��ˮ����ʣ�����岻�����ǣ�������
A. 2��H2��O2��N2�Ļ������
B. 2��N2
C. 2��H2
D. 2��O2��N2�Ļ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��������ͼ��ʾװ��(ͼ�й̶�װ������ȥ)�ⶨͭп�Ͻ���п������������̽���������£�
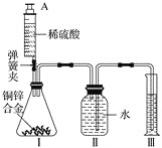
������ʵ��װ�ò����װ�������ԡ�
����װ�â��е���ƿ����2.0g��ͭп�Ͻ���Ʒ��ĩ����ע��������ע��ϡ���ᣬ������ƿ�в��ٲ�������ʱ��ȷ��ȡע�����ڶ���������10.5mLϡ���ᣬͬʱ�����н����ɼУ��Ƴ�װ�â��еĵ��ܣ�ȷ��ȡ��Ͳ��ˮ�����Ϊ214.0mL(ע����Ʒ�е����ʲ��μӷ�Ӧ
��װ�â���ʣ��������ʾ����ʵ�������ȷ����������Ϊ1.4g
�ܸ�С�����λͬѧ����ʵ����̲�ò�ͬ���ݣ�����ͭп�Ͻ���Ʒ��п����������
��ͬѧ����װ�â��з�Ӧǰ�������������м��㣻
��ͬѧ����װ�â��м���ϡ����������м��㣻
��ͬѧ����װ�â�����ȡˮ��������м��㣬����ã��ڱ�״���£��������ܶ�Ϊ0.09gL��1��
�ش��������⣺
(1)װ�â��з�Ӧ�Ļ�ѧ����ʽΪ___��ʵ������������ϡ���������ٲ������壬Ŀ����___��
(2)������г���ʣ�����֮ǰ����ȷ������_______��ϴ�ӡ����
(3)����ʵ��ⶨ�����ݣ�������λͬѧ��________(������������������������)ͬѧ�����м�����Ʒ��п������������
(4)��ѧС��ͬѧ���֣����ձ�ͬѧ�ķ������м��㣬��ʹʵ�������ֽϴ�ƫ��������ؿ������ƫ�����________(����)��
A �Ƴ�װ�â�ʱ��������������һ����ˮ
B ʵ�����ǰ��û���ų�װ�â��еĿ���
C ���ݴ���ʱ��δ�ų�����ϡ������ռ�����
���𰸡���1��![]() ��ʹ��Ʒ�е�п��ȫ��Ӧ����2�����ˣ���3���ң���4��AC��
��ʹ��Ʒ�е�п��ȫ��Ӧ����2�����ˣ���3���ң���4��AC��
��������
���⣨1������ͭ��������ĺ��棬���������Ӧ����Ӧ����п�����ᣬ������������п��������������������������ţ�ʵ������������ϡ���������ٲ������壬Ŀ����ʹ��Ʒ�е�п��ȫ��Ӧ����2����ͭ������п��Һ�Ļ�����еõ�ͭ���Ƚ��й��ˣ��õ���������п��Һ��ͭ���ٽ���ϴ�ӳ�ȥ���������п���ٽ��и����ȥˮ���ɣ���3�����ݼ���ϡ����������м�����Ҫ֪��ϡ�������������������������û�и�֪����4������п�����ᷴӦ��������п������ʱ���ų����������û����ȴ�����£���������������ԭ����֪������Ͳ��ˮƫ�࣬��������Ϊ�õ��������࣬�پ������ݴ���ʱ��δ�ų�����ϡ������ռ�����������Ľ����ƫ��
���㣺�����Ļ�ѧ���ʣ���ѧ����ʽ��ʵ����������
��������ǽ������˳�����֪��������֮ǰ�Ľ�����ϡ����������ᷴӦ������������������֮��Ľ�����ϡ�������ϡ���������������ѧ��Ӧ�����ʵ������ȶ��Ǵ�����֮��������ȣ�����Һ�����ʵ�����=��Һ���������������������������׳����ĵط��Ƕ�ʵ���������ۣ�Ҫ֪��п�����ᷴӦ�ų��������������Ӧ����������ȴ�����²��ܽ��й۲�ͼ��㡣
�����͡�ʵ����
��������
30
����Ŀ����1000t��������80���ij�����ʯ�������Ͽ�����������96���������������Ƕ��٣�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com