
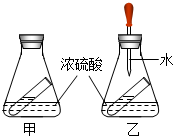
 如图是小婧对硫酸的一些性质的探究,锥形瓶内的小试管盛装饱和的澄清石灰水.
如图是小婧对硫酸的一些性质的探究,锥形瓶内的小试管盛装饱和的澄清石灰水.分析 (1)根据浓硫酸有吸水性进行分析;
(2)根据浓硫酸溶于水,放出大量的热,氢氧化钙的溶解度受温度的影响进行分析.
解答 解:(1)浓硫酸有吸水性,所以甲装置放置一段时间后,澄清的石灰水出现浑浊,原因是:浓硫酸吸收了石灰水中的水,使氢氧化钙固体析出;
(2)浓硫酸溶于水,放出大量的热,氢氧化钙的溶解度随温度的升高而减小,所以把乙装置分液漏斗中的浓硫酸滴入水中,发现澄清石灰水也出现浑浊,原因是:浓硫酸溶于水放热,氢氧化钙的溶解度随温度的升高而减小,使氢氧化钙固体析出.
故答案是:(1)浓硫酸吸收了石灰水中的水,使氢氧化钙固体析出.(2)浓硫酸溶于水放热使温度升高;Ca(OH)2的溶解度随温度升高而减小.
点评 本题主要考查了浓硫酸的性质和氢氧化钙的溶解度随温度的变化,难度不大,需要加强记忆.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 化学家谢赫特曼研究发现:铝锰合金晶体中的原子排列方式没有出现“规则有序而重复排列”的普遍现象,提出了“准晶体”概念,因此获得2011年诺贝尔化学奖.下列观点正确的是( )
化学家谢赫特曼研究发现:铝锰合金晶体中的原子排列方式没有出现“规则有序而重复排列”的普遍现象,提出了“准晶体”概念,因此获得2011年诺贝尔化学奖.下列观点正确的是( )| A. | 铝锰合金的强度和硬度比铝高 | |
| B. | 铝锰合金不具有导电导热性 | |
| C. | 铝的直接构成微粒是铝分子 | |
| D. | 合金中原子排列方式与纯金属的原子排列方式相同 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
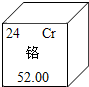 最近,“铬超标胶囊”事件引起社会强烈关注.铬的毒性与其价态及含量有关.铬常用作合金的生产原料,铬元素也是哺乳动物所需的微量元素之一.如图是铬在元素周期表中的相关信息,请回答:
最近,“铬超标胶囊”事件引起社会强烈关注.铬的毒性与其价态及含量有关.铬常用作合金的生产原料,铬元素也是哺乳动物所需的微量元素之一.如图是铬在元素周期表中的相关信息,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com