
【题目】一定条件下,在一密闭的容器中发生某反应,测得反应过程中各物质的质量如下表所示:
物质 | X | Y | Z | Q |
第一次测得的质量/g | 32 | 51 | 漏测 | 6 |
第二次测得的质量/g | 60 | 17 | 11 | 12 |
下列判断正确的是( )
A.该反应中X和Q的质量变化之比为5:1
B.该反应的化学方程式可表示为:Y→X+Z+Q
C.Z可能是该反应的催化剂
D.该反应可能是置换反应
【答案】C
【解析】解:X质量增加了:60g﹣32g=28g,即生成了28gX;Y的质量减少了:51g﹣17g=34g,即参加反应的Y质量为34g;Q质量增加了12g﹣6g=6g,所以生成Q6g,根据质量守恒定律可知参加化学反应的物质质量,等于生成的各物质质量总和,参加反应的Y的质量,正好等于生成的X和Q的质量总和,所以Z的质量应该不变,可能是催化剂. A、该反应中X和Q的质量变化之比为:28g:6g=14:3,故A错;
B、如果Z是催化剂时,该反应的化学方程式可表示为Y ![]() X+Q,故B错;
X+Q,故B错;
C、因为Z的质量在反应前后不变,可能是催化剂,故C正确;
D、该反应属于分解反应,故D错.
故选C.
【考点精析】利用质量守恒定律及其应用对题目进行判断即可得到答案,需要熟知①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:初中化学 来源: 题型:
【题目】化学兴趣小组利用下图所示装置,测定某碳酸饮料中CO2的含量. 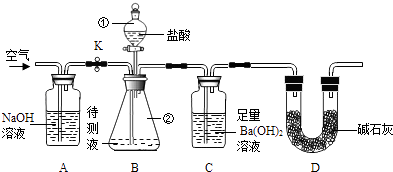
资料:①CO2与足量Ba(OH)2反应生成BaCO3沉淀.②NaHCO3与盐酸反应生成CO2
将一瓶饮料冷藏24小时(未结冰),开封后取一定量样品加入到盛有过量NaOH溶液的容器中,充分反应后作待测液.
回答下列问题:
(1)装置B中仪器①②的名称分别为和 . 加入足量盐酸,仪器②中发生的化学反应方程式为、.
(2)反应后持续缓缓通入空气,若缺少装置A,则实验结果(填“偏大”、“偏小”或“无影响”,下同),若饮料未冷藏,则实验结果 .
(3)装置D的作用是 , 若冷藏温度过低,饮料结冰,则实验结果明显偏小,可能的原因是 . 若不测定C中BaCO3的质量,只测定C在实验前后的质量差,则实验结果明显偏高,原因是 .
(4)下列各项措施中,不能提高实验结果准确度的是 . (填字母) a、滴加盐酸不宜过快
b、在A~B之间添加盛有浓硫酸的洗气装置
c、在B~C之间添加盛有NaHCO3的洗气装置.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据要求填空:
(1)下列三种金属被发现、使用的先后顺序为:铜、铁、铝.金属大规模被使用的先后顺序跟(选填字母)(A.地壳中金属元素的含量 B.金属的导电性 C.金属的活动性)关系最大; 目前世界上已有50%以上的废钢铁得到回收利用,其目的是A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈;
生锈的铁制品放入盛有过量稀盐酸的洗槽中,观察到溶液变黄,有无色气泡逸出.写出其中一个反应的化学方程式 , 其反应类型是 . 若要验证银、铁、锌的活动性顺序,某同学已经选择了打磨过的铁丝,你认为他还需要的另外两种溶液是、 .
(2)A、B两种固体物质溶解度曲线如图所示. ①t1℃时,A和B的溶解度大小关系是 .
②把t1时,A和B的饱和溶液变成不饱和溶液,除了升高温度外,还可以采取的方法有 .
③t2℃时,A的溶解度为25g,在t2℃时,向50g水中加入20g的A物质,充分溶解所得溶液的溶质质量分数为 .
④A中混有少量的杂质B,若想得到较为纯净的A,可以采用的方法是 . 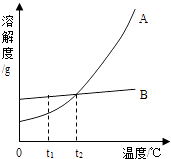
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究.
2NaOH+H2↑+Cl2↑),这种工业成为“氯碱工业”,某研究性学习小组对该厂生产的烧碱样品进行如下探究.
(1)I.定性探究 【提出问题】烧碱样品中含有哪些杂质?
【猜想】猜想一:可能含有Na2CO3 , 作出此猜想的依据是(用化学方程式表示).
猜想二:可能含有NaCl,作出此猜想的依据是(用简洁的文字表述).
【设计实验】
实验步骤 | 实验现象 | 解释或结论 |
①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁. | 试管外壁发热 | 原因是 |
②向①所得的溶液中逐渐加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水浑浊的气体 | 样品中含有的杂质是 |
③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有的杂质是 |
【交流与讨论】小明同学提出:“上述实验中稀硝酸也可以用稀盐酸代替”,你认为他的观点(填“正确”或“不正确”).
(2)II.定量探究 【提出问题】烧碱样品中氢氧化钠的质量分数是多少呢?
【设计实验】小婉同学设计探究方案后进行实验并测得数据如下:
请你利用小婉同学测得的数据计算烧碱样品中氢氧化钠的质量分数(请列出计算过程).
(3)【交流与反思】小强同学认为小婉同学设计的探究方案不够严密,其理由是: ①探究方案中没考虑氢氧化钠的吸水性.
②探究方案中因缺少(填操作名称),导致测得的氢氧化钠的质量分数偏小.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列反应的化学方程式并填空.
(1)碳在过量氧气中充分燃烧:该反应属于(选填“放热”或“吸热”)反应.
(2)锌和稀硫酸反应:;反应类型是
(3)盐酸与碳酸氢氨反应:;明显的现象是
(4)实验室加热高锰酸钾制取氧气:在发生装置的试管口放一团棉花的作用是
(5)用熟石灰和硫酸铜溶液制备波尔多液:反应类型是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋是个巨大的资源宝库,利用海水可制取许多化工产品.
(1)用海水制食盐,常通过得到粗盐,粗盐中含有少量的CaCl2、Na2S04等杂质.除去上述杂质,先加过量BaCl2溶液除去 , 再加溶液除去CaCl2和过量的BaCl2 , 生成的沉淀经除去.
(2)从海水中提取溴常用吹出法,即用氯气(C12)将海水里溴化钠(NaBr)中的溴置换出来,再用空气或水蒸气吹出溴(Br2).流程示意图如下: 
①写出氯气置换出溴单质的化学方程式:;该反应在pH=3的酸性条件下进行,可用测定反应液的酸碱度.
②吹出的溴和大量空气混合在一起进入吸收塔(吸收塔中发生的反应:Br2+SO2+2H2O═H2SO4+2HBr).根据流程图分析,通入SO2的目的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com