
【题目】下列化学肥料属于复合肥的是( )
A. 氯化钾 B. 尿素 C. 碳酸氢铵 D. 硝酸钾
科目:初中化学 来源: 题型:
【题目】如图所示是A、B、C三种物质的溶解度曲线,据此图回答: 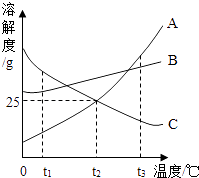
(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是;
(2)t2℃时,将30gA放入100g水中,充分搅拌后,所得溶溶液的溶质质量分数是;
(3)t3℃时,将等质量A、B两种物质的饱和溶液降温到t2℃时,析出晶体质量较大的是;
(4)t3℃时,将25gC放入100g水中,充分搅拌后得到C的饱和溶液,在不改变溶剂量的前提下,将其变为不饱和溶液的方法是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一工业过程:电石(CaC2) ![]() 灰浆
灰浆 ![]() 残渣 其中电石与水的反应为:CaC2+2H2O=Ca(OH)2+C2H2↑
残渣 其中电石与水的反应为:CaC2+2H2O=Ca(OH)2+C2H2↑
(1)残渣中主要成分是Ca(OH)2和 . 工业上利用乙炔(C2H2)产生的灰浆和残渣制备化工原料KClO3和超细CaCO3 .
(2)Ⅰ.制备KClO3的流程如下: 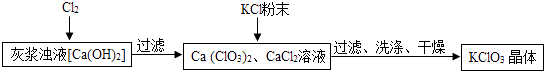
向灰浆浊液中通入Cl2 , 得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式 .
(3)有关物质在常温下的溶解度如下:
物质 | Ca(ClO3)2 | CalO3 | KClO3 | KCl |
溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
上述流程中加入KCl粉末,KCl与(填化学式)发生了复分解反应,得到KClO3晶体.你认为能得到KClO3晶体的原因是 .
(4)洗涤时,可选用下列洗涤剂(填字母编号). A、KCl饱和溶液 B、冰水 C、饱和KClO3溶液
(5)Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl的目的是溶解残渣中的难溶盐): 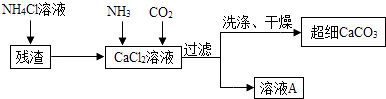
向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式 .
(6)流程中溶液A可循环使用,其主要成分的化学式是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】今年央视3.15晚会曝光,少数不法厂家向液化石油气中掺入了二甲醚(C2H6O),二甲醚会对液化气罐的配件造成腐蚀,存在安全隐患.下列关于二甲醚的说法错误的是( )
A.属于氧化物
B.每个分子中含有9个原子
C.碳、氢、氧元素的质量比为12:3:8
D.碳元素的质量分数约为52.2%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请用化学用语表示或写出符号的意义:
(1)①氢氧根离子;②二氧化硫中硫元素的化合价;③3H2O .
(2)下列食物:①米饭;②鸡蛋;③大豆油;④西红柿.能提供大量蛋白质的是(选填序号),蛋白质属于(填“无机物”或“有机物”).在日常生活中常用聚乙烯塑料来生产食品包装袋、保鲜膜,聚乙烯塑料属于材料.
(3)香烟烟气中含有多种有害物质,毒副作用大的有、尼古丁和焦油,不吸烟的人能闻到烟味的原因是;随手丢弃的烟头还容易引发火灾,原因是(选填字母)A.提供可燃物 B.提供氧气 C.使可燃物的温度达到着火点);一旦发生火灾,消防队员通常用水来灭火,该方法的化学原理是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定条件下,在一密闭的容器中发生某反应,测得反应过程中各物质的质量如下表所示:
物质 | X | Y | Z | Q |
第一次测得的质量/g | 32 | 51 | 漏测 | 6 |
第二次测得的质量/g | 60 | 17 | 11 | 12 |
下列判断正确的是( )
A.该反应中X和Q的质量变化之比为5:1
B.该反应的化学方程式可表示为:Y→X+Z+Q
C.Z可能是该反应的催化剂
D.该反应可能是置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】富含淀粉的谷物、甘薯等可以酿酒.在酿酒过程中淀粉在酶的作用下转化为葡萄糖,葡萄糖发酵为酒精.香甜的酒酿就是利用该原理.用酒曲酶(俗称酒药)制作的.家庭一般制作酒酿的简单流程图如图:(注:有机反应化学方程式可用箭号表示) ![]()
(1)配平化学方程式:(C6H10O5)n(淀粉)+H2O ![]() nC6H12O6(葡萄糖)
nC6H12O6(葡萄糖)
(2)如温度、水分等因素控制不当,易导致乳酸量过多而味偏酸,请完成该反应的化学方程式:C6H12O6 ![]() 2(乳酸).
2(乳酸).
(3)成熟的酒酿放置时间越长酒味越浓,因为更多的葡萄糖在酒化酶作用下发酵分解为酒精(C2H5OH )和二氧化碳,写出该反应的化学方程式 .
(4)若用1kg大米酿米酒,假设其中有0.81kg的淀粉全部转化为酒精,则理论上可酿制含酒精质量分数为10%的米酒kg,(提示:由淀粉转化为酒精的关系式为(C6H10O5)n~2nC2H5OH).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某硫酸厂废水中含有少量硫酸,为达标排放,技术员小张对废水中硫酸的含量进行检测.
(1)配制溶液: 欲配制溶质质量分数为4%的NaOH溶液100g,需要NaOH固体g,水ml(水的密度为1g/cm3);
(2)检测分析: 取废水样品98g,向其中逐滴加入NaOH溶液至恰好完全反应时,消耗4%的NaOH溶液20g.(假设废水中其它成分均不和NaOH反应;发生反应的化学方程式为:2NaOH+H2SO4═Na2SO4+2H2O)
试计算废水中硫酸的质量分数(写出计算过程).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com