
【题目】如图是甲、乙两种固体物质的溶解度曲线,下列有关说法正确的是( )
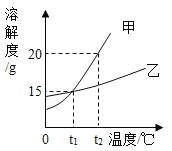
A.甲的溶解度大于乙的溶解度
B.若乙中混有少量的甲,可以采用降温结晶的方式提纯乙
C.t2℃时,甲、乙的饱和溶液中,溶质质量的大小关系为甲>乙
D.t1℃时,在10g水中加入20g甲,所得溶液中溶质的质量分数为13%
科目:初中化学 来源: 题型:
【题目】A~E是初中化学中常见的物质,下图为这些物质的相互转化关系图,图中“—”表示相连的物质间能相互发生反应,“→”表示物质间有相应的转化关系。其中,A、B都是黑色固体,通常状况下,C是一种能使澄清石灰水变浑浊的气体,D溶于水形成蓝色溶液,常用于配制一种具有杀菌作用的农药。请写出:

(1)物质C的化学式为_________;
(2)反应①的化学方程式为_______________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校“我与化学”活动小组在探究活动中要制取一定量的氨气。该小组查阅资料可知:
①常温下NH3是一种无色、有刺激性气味的气体,极易溶于水,密度比空气小。
②氯化铵固体和熟石灰粉末在加热条件下生成氨气
2NH4Cl + Ca(OH)2![]() CaCl2+ 2NH3↑+ 2H2O
CaCl2+ 2NH3↑+ 2H2O
1. 根据以上信息和如下图所示装置,完成下列空白:
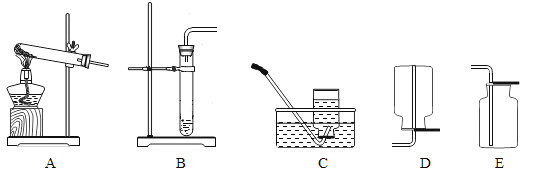
制取氨气发生装置是__________(填序号),制取氨气收集装置是__________(填序号)。
2.NH3水溶液呈碱性,能使湿润的紫色的石蕊试纸变成蓝色。收集氨气时,检验氨气集满的方法是(写出实验操作及现象)___________________________。
3.NH3具有还原性,加热条件下能够还原氧化铜得到单质铜。判断反应发生的现象是___________。
4.B装置可用于实验室制取氧气,其化学方程式是___________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种“白色粉末”很感兴趣,与小刚进行了相关探究.

【查阅资料】这种“白色粉末”的主要成分是过碳酸钠(化学式为Na2CO4),常温下,与水反应生成氧气.【实验1】小明选用如图所示装置中的 (选填序号)进行过碳酸钠与水的反应并收集产生的气体,经检验该气体是氧气,检验方法是
【提出问题】过碳酸钠与水反应后得到的溶液M中溶质的成分是什么?
【作出猜想】根据过碳酸钠与水的组成作出三种猜想.
猜想一:Na2CO3;猜想二:NaOH;猜想三:Na2CO3和NaOH.
【实验2】小明取溶液M,滴加CaCl2溶液,观察到有白色沉淀生成,他认为白色沉淀是CaCO3,溶液中一定含有Na2CO3.小刚提出质疑,产生的白色沉淀不一定是CaCO3,他的理由是: .
【实验3】小刚取溶液M,滴加稀HCl,观察到 ,证明溶液中一定含有Na2CO3,从而否定了猜想二.Na2CO3与稀HCl反应的化学方程式为 .
【实验4】为进一步确定溶液M中是否含有NaOH,他们向溶质M中滴加CaCl2溶液至不再产生沉淀为止,取上层溶液,加入 ,无明显现象.证明溶液中无NaOH溶液,猜想一正确.该实验中用CaCl2溶液而不用饱和石灰水,原因是: .
【反思拓展】
(1)根据过碳酸钠的性质,保存时应注意防潮.
(2)检验A、B两种物质是否同时存在,一定要考虑二者性质的互相干扰问题.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质A、B、C、D、E分别是硫酸、氢氧化钠、氢氧化钡、碳酸钠、氯化锌五种溶液中的一种。已知C为氢氧化钠溶液,它们两两之间反应情况如下表所示:
反应物 | 反应现象 |
往C中加B | 溶液的pH变化趋势如图 |
往D中加B | 溶液中的溶质质量变化如图 |
B和E混合 | 产生大量的气泡 |
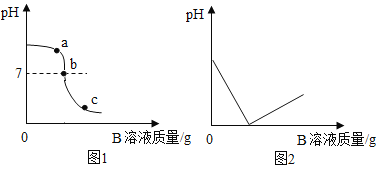
(1)A是__________溶液;E是__________溶液。
(2)图8中a点处溶液中所含溶质有____________________
(3)图9所示的反应原理为_________________(用化学方程式表示)。
(4)五种溶液两两之间混合后,可产生白色沉淀的反应原理共有__________个。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙是初中化学中常见的物质,其转化关系如图所示(其中部分反应物和生成物及反应条件略去):
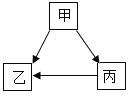
(1)若反应皆为化合反应,且均在点燃条件下进行,则丙为_____(填化学式),乙转化为丙的反应为_____(填“吸热”或者“放热”)反应。
(2)若反应皆为置换反应,且均在溶液中进行,甲、乙、丙都为金属,则它们的活动性由强到弱的顺序为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有________产生,反应的化学方程式是________________________________________________________。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
试管(盛有同体积同浓度的盐酸) | ① | ② | ③ | ④ |
镁条长度 | 1cm | 2cm | 3cm | 4cm |
相同的实验现象(省略题干现象) | 快速反应,试管发热,镁条全部消失 | |||
沉淀量差异(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
[得出结论]镁条与盐酸反应产生白色沉淀与________有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是____________________(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | ________,白色沉淀________ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀________ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是: |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个坐标示意图分别表示四个实验过程中的某些变化情况,其中肯定错误的是( )
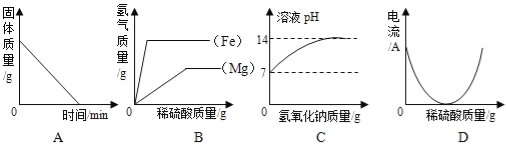
A. 加热一定量碳铵(NH4HCO3)的实验,试管中固体的质量变化
B. 等质量的镁条和铁丝分别与足量的稀硫酸反应,产生气体的质量变化
C. 向一定质量的水中加入氢氧化钠时,形成的溶液pH的变化
D. 向盛有一定量Ba(OH)2溶液的烧杯中逐滴滴加稀硫酸,测得烧杯中溶液导电性的变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组利用如图所示装置研究碳及其氧化物的性质。
(提示:氢氧化钠溶液能与二氧化碳反应;丙处试管可防止液体倒吸。)
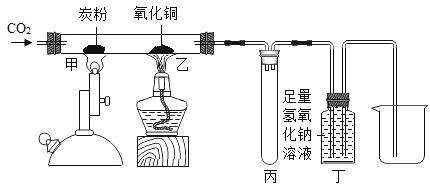
(1)甲处的现象是_________________,体现了碳的______________性。
(2)乙处的现象是__________________,反应的化学方程式是_________________________。
(3)丁装置的作用是_____________________________________。
(4)该实验体现了CO的性质有_____________________________。
(5)若将丁处氢氧化钠溶液改为澄清石灰水,能否检验乙处反应生成的二氧化碳?请说明理由________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com