
【题目】(4分)下图为几种固体的溶解度曲线,回答下列问题:
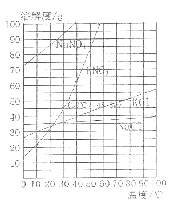
(1)NaCl的溶解度随温度变化的规律是_________________。
(2)30℃时,KNO3溶液的最大浓度(溶质质量分数)为__________(只列计算式,不需要计算结果)。
(3)60℃时,10g NaCl和90g KNO3完全溶解于100g蒸馏水, 冷却到30℃后,_________(“有”或“没有”)NaCl析出,有_______g KNO3结晶析出。
【答案】(1)NaCl 溶解度受温度影响较小,随温度的升高而升高。
(2)![]() ;(3)没有;44.2。
;(3)没有;44.2。
【解析】
试题分析:(1)由给出的溶解度曲线图可知,氯化钠的溶解度曲线是“平缓”型,就是温度升高,NaCl的溶解度增大较小,但是依旧是随温度的升高而增大;(2)根据KNO3 在30℃时的溶解度为45.8g,在物质形成饱和溶液时,溶质的质量分数最大,质量分数是![]() 。 (3)对于氯化钠,60℃时溶解度为37.5g,30℃时的溶解度36g,所以10g的氯化钠在100g水中没有形成饱和溶液,因此不会析出NaCl晶体。对于硝酸钾,60℃时溶解度大于90g,所以是不饱和溶液, 30℃时的溶解度为45.8g,此时是过饱和溶液,而且会析出硝酸钾晶体(90-45.8)g=44.2g
。 (3)对于氯化钠,60℃时溶解度为37.5g,30℃时的溶解度36g,所以10g的氯化钠在100g水中没有形成饱和溶液,因此不会析出NaCl晶体。对于硝酸钾,60℃时溶解度大于90g,所以是不饱和溶液, 30℃时的溶解度为45.8g,此时是过饱和溶液,而且会析出硝酸钾晶体(90-45.8)g=44.2g


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:初中化学 来源: 题型:
【题目】阿司匹林(化学式为C9H8O4)是一种常见的解热镇痛药,下列说法正确的是( )
A. 阿司匹林中含有24个原子
B. 阿司匹林的相对分子质量为180g
C. 阿司匹林中碳、氢元素质量比为9:8
D. 阿司匹林中碳的质量分数为60%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答有关问题。
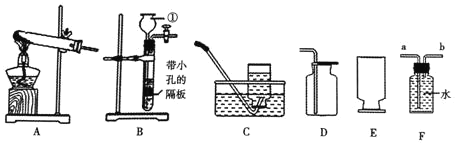
(1)图中标有①的仪器名称是_____。
(2)实验室制取CO2气体的化学方程式为_____,若用D装置收集CO2气体,证明集气瓶已充满CO2的方法是______
(3)实验室常用无水醋酸钠和碱石灰的固体混合物在加热条件下制取甲烷气体,发生装置可选择_____(填字母),甲烷气体一般采用装置C进行收集,收集满后集气瓶的放置方式如图E所示,据此可推断甲烷一定具备的物理性质是_____。如果选用F装置收集甲烷,气体应从_____(填“a”或“b”)端管口通入。
(4)饱和NH4Cl溶液与饱和NaNO2溶液混合共热可制取氮气,再用制得的氮气和氢气在一定条件下化合生成氨气。如图是实验室模拟合成氨的装置。
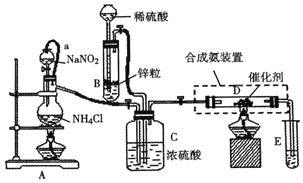
①装置A中导管a所起的作用是_____(用序号回答)。
a.防止NaNO2饱和溶液蒸发 b.使分液漏斗中溶液能顺利滴下 c.使实验装置不漏气
②装置A中反应物所有的氮元素都转化成氮气,该反应的方程式为_____
③装置C可以使N2、H2两种气体充分混合,并通过观察气泡以调节N2和H2的气流的速度,除此以外,还有一个作用是_____
④从装置E中导出的气体成分是_____,向装置E的试管中滴人酚酞溶液,观察到的现象是_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某赤铁矿石样品160g与75g含碳36%的一氧化碳和二氧化碳的混合物恰好完全反应,则该赤铁矿石的纯度为( )
A. 40% B. 50% C. 60% D. 80%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定氯化钠和碳酸钠混合物的组成情况,童童同学进行了如下实验。

(1)实验中发生反应的化学方程式为________________________________________;
(2)求混合物中发生反应物质的质量(X)的比例式为_______________;
(3)混合物中氯化钠和碳酸钠质量的最简整数比为____________;
(4)用36.5%的浓盐酸配制实验中所用的稀盐酸需加水的质量为____________;
(5)求蒸发掉100g水后,所得溶液中溶质的质量分数为____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(关注生产实际)
我国化学家侯德榜创立的“侯氏制碱法”促进了世界制碱技术的发展,其主要生产流程如图1所示。NH4Cl和NaCl的溶解度曲线如图2所示。
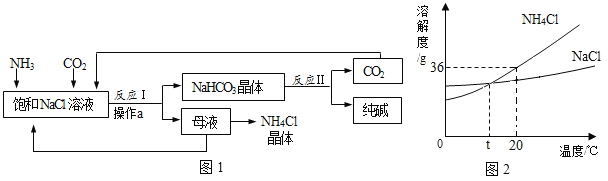
(1)操作a的名称是_____,图1流程中可循环利用的一种物质是_____。
(2)NaCl与NH4C1相比,_____的溶解度受温度的影响较大。
(3)20℃时,将72g NaCl溶于水制成饱和溶液,需加入水的质量是_____;将20℃时NaCl饱和溶液降温到t℃,该过程没有改变的是_____。(填序号)
A 溶液质量 B 溶质质量 C 溶剂质量 D 溶质的溶解度
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合图示回答下列问题:

(1)食醋有酸味,因为食醋中含有_____(填化学式)。
(2)浓硫酸具有_____作用能夺取纸张里的水分,生成黑色的炭。
(3)氢氧化钠固体密封保存的原因是_____。
(4)汽车铅蓄电池中含有的一种酸的化学式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)请你与小明和他的同学一起进行实验室制取二氧化碳的探究.
小明对三组药品进行了研究,实验记录如下:
组别 | 药品 | 实验现象 |
① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
从制取和收集的角度分析,一般选择第①组药品,所发生反应的化学方程式为_____;不选择第③组药品的原因是_____.
(2)老师为他们提供的如图1所示的实验仪器(导管、橡皮塞等未画出).
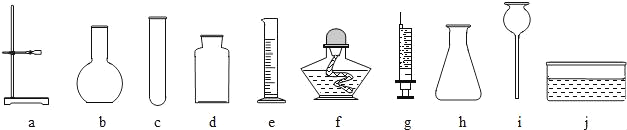
小明根据提供的实验仪器分别设计了如图2所示四套制取和收集二氧化碳的装置.
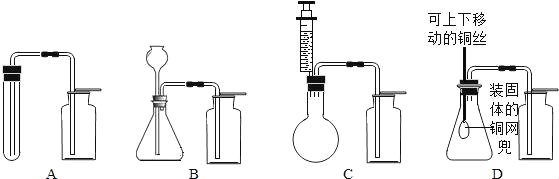
对上面的设计方案小明和他的同学进行了交流讨论.
其中可能收集不到二氧化碳气体的装置是_____;能够使反应随时停止和发生的装置是_____.用澄清石灰水可鉴定CO2 气体,请写出其化学方程式为_____.
反思小结:
气体制取和收集装置的选择依据:①发生装置——反应物状态和反应条件;②收集装置——气体密度、气体溶解性和_____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com