
【题目】化学在开发可替代能源、保护环境等方面起到主要作用。下列措施,不利于节能减排和改善环境的是
A.开发太阳能、风能 B.推行“限塑令”
C.推广乙醇汽油 D.焚烧秸秆
科目:初中化学 来源: 题型:
【题目】“绿水青山就是金山银山”。你认为下列做法与这一理念不相符的是
A. 工业废水经处理达标后排放 B. 加高燃煤锅炉烟囱,将废气排到高空
C. 植树造林,增大绿化面积 D. 尽量不使用一次性塑料袋购物,减少“白色污染”
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示.下列叙述中正确的是( ) 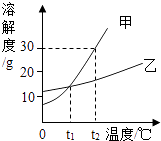
A.甲物质的溶解度大于乙物质的溶解度
B.t1℃时,甲、乙两物质饱和溶液的溶质质量分数一定相等
C.t2℃时,将30g甲物质放入70g水中,所得饱和溶液的质量为100g
D.t2℃时,甲、乙两物质的饱和溶液降温到t1℃,析出晶体质量甲>乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH﹣═H2O.如图,像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式.
(1)离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例) 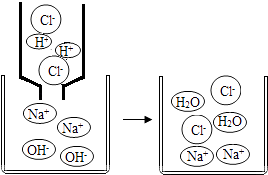
①写出Na2SO4与BaCl2反应的化学方程式:;
②把易溶于水、易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示.上述方程式可改写成:2Na++SO42﹣+Ba2++2Cl﹣═BaSO4↓+2Na++2Cl﹣
③删去方程式两边不参加反应的离子:Ba2++SO42﹣═BaSO4↓
④检查方程式两边各元素的原子个数和电荷总数是否相等.
请回答:
下列各组中的离子,在pH=3的水溶液中能大量共存的是
A、Na+、Mg2+、Cl﹣、SO4 2﹣ B、Na+、K+、Cl﹣、OH﹣
C、Na+、Cu2+、Cl﹣、SO42﹣ D、Na+、K+、Cl﹣、CO32﹣
(2)写出稀盐酸滴在石灰石上所发生反应的离子方程式;
(3)写出一个与离子方程式Mg+2H+═Mg2++H2↑相对应的化学方程式;
(4)酸、碱、盐在水溶液中发生的复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,只要具备生成物中有气体或沉淀或生成,反应就能发生.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色.
(1)人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”,在“五金”顺序中把金属的位置移到最后,正好符合由弱到强的顺序.
(2)汽车车体多用钢材制造.表面喷漆不仅美观,而且可有效防止与接触而生锈.
(3)工业上用CO还原赤铁矿冶炼金属铁的化学方程为 . 西汉时期中国古老的冶铜方法是“湿法冶铜”主要的反应原理是铁与硫酸铜溶液反应,写出反应的化学方程式
(4)在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是 . (填一种即可)
(5)铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图. ①铁锅含有合金单质(写化学式),含有的有机合成材料是 . (填写名称)
②炒菜时铁锅中的油着火可用锅盖盖灭,其原理是 .
③铜也易生锈,铜锈的主要成分是碱式碳酸铜(Cu2(OH)2CO3),是铜与空气中的氧气、水和共同作用的结果.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在生产生活中,你会发现“化学就在身边”.
(1)低碳出行是为了减少的排放.
(2)硬水中的钙离子是以碳酸氢钙的形式存在的,试写出碳酸氢钙的化学式为 .
(3)以下服装的饰品中,由合成材料制成的是(填序号).
A.真丝领带
B.真皮手套
C.羊毛围巾
D.尼龙长袜
(4)举重运动员比赛时,常用的防滑剂是碱是碳酸镁〔Mg5(OH)2(CO3)4〕,它分解的化学方程式为:Mg5(OH)2(CO3)4 ![]() 5MgO+X+4CO2↑,则X的化学式为 .
5MgO+X+4CO2↑,则X的化学式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示的A、B、C三种物质的溶解度曲线回答下列问题: 
(1)t2℃时,在50g水中加入45g固体A,充分溶解后,得到的是溶液.
(2)升高温度可使物质(填“A”、“B”或“C”)的不饱和溶液变为饱和溶液.
(3)M点表示 .
(4)当A中混有少量B,可用法提纯A.
(5)t2℃时,将A、B、C的饱和溶液分别降温至t1℃,所得溶液的溶质质量分数关系是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高纯氧化钙是用于电子工业重要的无机化工原料.用硝酸钙溶液制备高纯氧化钙的工艺流程如图: 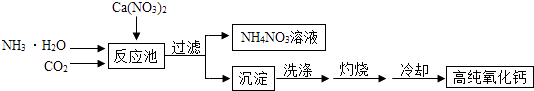 反应池中发生反应的化学方程式为:CO2+2NH3H2O+Ca(NO3)2═2NH4NO3+CaCO3↓+H2O
反应池中发生反应的化学方程式为:CO2+2NH3H2O+Ca(NO3)2═2NH4NO3+CaCO3↓+H2O
请回答下列问题:
(1)过滤操作中玻璃棒的作用是 .
(2)过滤后所得沉淀表面可能含有的可溶性杂质有(写出一种即可).
(3)该工艺流程中可循环使用的物质是 .
(4)冷却需在干燥的环境中进行,否则制得的高纯氧化钙中会混有的杂质是 .
(5)上述流程中的副产物NH4NO3可用作氮肥,氮肥的主要作用是 .
A.促进植物生长,叶色浓绿
B.增强作物的抗寒,抗旱能力
C.增强作物的抗病虫害和抗倒伏能力.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com