
【题目】(1)化学式是用元素符号表示物质组成的式子。如Al(NO3)3、O3、CO2、CO、Na2S、Hg其中由原子直接构成的物质是_______________,引起温室效应的主要物质是_________,含有原子团的物质的名称是_________。化学方程式是表示化学反应的式子。写出检验物质中含有水的化学方程式_________,生成物的俗名为_______________。
(2)某品牌补铁剂主要成分是富马酸亚铁(C4H2FeO4),富马酸亚铁有_________种元素组成,其摩尔质量是_________,该分子中各原子的个数比为_________,0.25mol的C4H2FeO4中约含有_____________个氢原子,含有_______________mol氧原子。
【答案】Hg CO2 硝酸铝 ![]() 胆矾(或蓝矾) 4 170g/mol C、H、Fe、O原子个数比为4:2:1:4 3.01×1023 1mol
胆矾(或蓝矾) 4 170g/mol C、H、Fe、O原子个数比为4:2:1:4 3.01×1023 1mol
【解析】
(1)金属、稀有气体一般由原子直接构成物质,Hg是由原子直接构成的物质;O3、CO2、CO 由分子构成,Al(NO3)3、、Na2S由离子构成。
引起温室效应的主要物质是CO2,含有原子团的物质是Al(NO3)3,它的名称是硝酸铝;
水与白色硫酸铜反应生成蓝色硫酸铜晶体,常用这个反应来检验物质中是否有水,化学方程式为![]() ,生成物的俗名为胆矾或蓝矾。
,生成物的俗名为胆矾或蓝矾。
(2)富马酸亚铁(C4H2FeO4)含有碳、氢、铁、氧4种元素组成;富马酸亚铁的相对分子质量为12×4+1×2+56+16×4=170,则C4H2FeO4的摩尔质量为170g/mol;由富马酸亚铁的化学式C4H2FeO4可知,其中C、H、Fe、O元素的原子个数比为4:2:1:4,1mol C4H2FeO4中含有2mol氢原子,则0.25molC4H2FeO4中含有0.5mol氢原子,约含有3.01×1023个氢原子。1mol C4H2FeO4中含有4mol氧原子,则0.25molC4H2FeO4中含有1mol氧原子。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】氢氧化钙是熟石灰的主要成分,在生产和生活中有广泛的用途。
(1)熟石灰可由生石灰加水制得,其反应的化学方程式为_________________。由此生石灰可做某些饼干包装袋中的_________。
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应原理用化学方程式解释为___________________。
(3)用熟石灰来改良酸性土壤,反应的化学方程式是__________________(以土壤中含有硫酸为例)。
(4)用熟石灰粉与草木灰(主要成分是![]() )按一定比例混合可制得高效环保农药“黑白粉”。使用时,选择在有露水的早晨,把“黑白粉”撤在植物茎叶上,可消除忌碱虫体。“黑白粉”比熟石灰更高效,是由于生成了碱性更强的氢氧化钾,反应的化学方程式______________________。
)按一定比例混合可制得高效环保农药“黑白粉”。使用时,选择在有露水的早晨,把“黑白粉”撤在植物茎叶上,可消除忌碱虫体。“黑白粉”比熟石灰更高效,是由于生成了碱性更强的氢氧化钾,反应的化学方程式______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据图中实验回答下列问题。
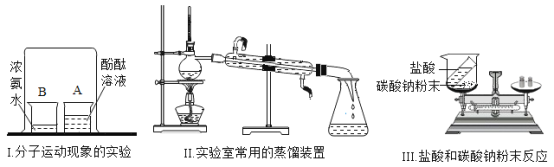
(1)实验I,烧杯_____(填“A”或“B”)中溶液变红;
(2)实验II,烧瓶中放入几粒沸石的作用是_____;
(3)实验III,观察到反应后天平不平衡,该反应是否符合质量守恒定律:_____(填“符合”或“不符合”),该反应前后,一定不变的是_____(填序号)。
a.原子种类 b.原子数目 c.分子种类 d.分子数目 e.元素种类 f.物质种类
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】质量守恒定律是化学的重要定律。它不仅反映化学变化中各物质的质量关系,同时也是书写化学方程式的理论依据。请根据下面两组实验,回答有关问题:
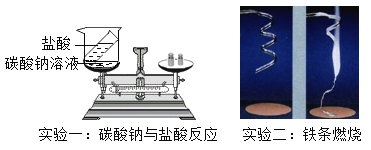
(1)实验一中,发生反应的化学方程式为:![]() ,则X的化学式为_____;
,则X的化学式为_____;
(2)实验二中,从理论上判断,反应前镁的质量_____(选填“小于”、“大于”或“等于”)反应后生成物的质量;
(3)从上述两个实验可以得出,在验证质量守恒定律时,凡是有气体参与或生成的化学反应,都应该在_____(选填“敞口”或“密闭”)容器内进行。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】取氯酸钾和二氧化锰的混合物30g,加热一段时间后冷却,冷却后称得剩余固体质量为20.4g,将剩余固体加入一定量的水中,充分搅拌后过滤,得到的滤渣经洗涤、烘干后称量为1.5g。计算:(根据化学方程式列式计算)
(1)生成氧气______________mol。
(2)反应后剩余固体的成分及相应的质量__________________。
(3)将氯酸钾、二氧化锰、高锰酸钾的混合物装入试管并充分加热,反应完成后试管中残渣中物质有___________________。
(4)将A、B、C各10g的混合物加热后,A全部参加反应,生成4gD,同时增加了8gC,则反应中A与B的质量比是__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】蜡烛燃烧实验细探究。I.蜡烛燃烧过程探究。蜡烛燃烧时可观察到火焰集中在烛芯周围,石蜡不段融化但液态石蜡却没有直接燃烧,同学们对蜡烛燃烧过程展开了探究。
(1)火焰结构特点探究:点燃蜡烛,将一张滤纸从火焰上方盖下,1-2秒后取出,观察到滤纸上炭化形成黑圈(如图),得出结论:________________。

(2)焰心所含物质探究:如图,点燃蜡烛,用注射器在烛芯附近抽取气体物质。
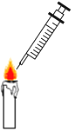
(猜想假设)同学们对该物质主要成分提出三种猜想:
①二氧化碳;②水蒸气
猜想①②的由是________________。
③石蜡蒸气,理由是液态石蜡受热会气化。
(实验探究)
操 作 | 现 象 | 结 论 |
(1)立即将注射器内物质注入内壁涂有澄满石灰水的烧杯。 | 观察到_________________________ | 猜想①成立 |
(2)立即将注射器内物质注入干而冷的烧杯。 | 内壁没有出现水雾,而是出现白色固体物质。 | 猜想②不成立 |
(3)立即将注射器靠近火焰,推动活塞。 | 注射器口产生火焰,物质能燃烧。 | 猜想③_______ |
(实验反思)经过讨论,同学们认为猜想①不成立,实验中产生明显现象的原因是:______________________。
(补充实验)将蜡烛熄灭,瞬间可观察到一缕“白烟”轻轻升起,立即用燃着的火柴去点燃“白烟”,“白烟”____________(填“能”或“不能”)燃烧。
(实验结论)石蜡燃烧是固态石蜡先受热液化,然后在烛芯气化形成气态石蜡后才能燃烧。
II.蜡烛熄灭原因探究。下如图和2实验中的蜡烛均会逐渐熄灭。
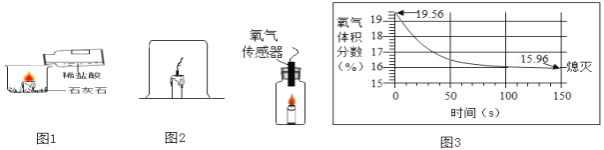
(1)如图实验中,烧杯底部产生大量气泡,反应的符号表达式为________________蜡烛(足量)逐渐想灭,说明二氧化碳的性质为_______________。
(2)同学们对如图实验中蜡烛(足量)熄灭的原因展开研究。
(猜想与假设)①可能是二氧化碳含量过大;②可能是氧气被完全消耗。
(探究与结论)
(1)甲同学收集1瓶含20%氧气和80%二氧化碳的气体,将点燃的蜡烛慢慢伸入瓶中并密封,蜡烛燃烧一段时间后才慢慢熄灭。根据实验现象可知:假设①___________(填“合理”或“不合理”)
(2)乙同学使用氧气传感器测量密闭装置内蜡烛(足量)从燃烧到熄灭的过程中氧气含量的变化,实验装置和实验结果如图所示。下列判断或结论正确的是(________________)
a.实验开始时密封装置内是纯净的氧气 b.蜡烛熄灭的原因是瓶内氧气已经耗尽
c.蜡烛想灭后瓶内气体是二氧化碳和氧气 d.氧气浓度小于一定值时,蜡烛无法燃烧
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】初三的同学在实验室里进行相关的有趣数字化实验,他们对实验充满了浓厚的兴趣。做了以下实验:探究制取氧气的适宜催化剂
实验方案如下:
I.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
II.取30粒含MnO2的海藻酸钠微球,采用如图装置进行实验。改用其他三种微球,分别重复上述实验,得到如图的锥形瓶内压强随时间变化的曲线图。

(1)每次实验时,海藻酸钠微球数应相同的原因_____。
(2)用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是_____。
(3)从实验曲线看,催化效果较好、反应温和的催化剂是_____
(4)实验结束后要从锥形瓶中重新回收二氧化锰。通过以下三步实验操作进行回收,正确操作的先后顺序是_____(填写序号)
A烘干 B过滤 C洗涤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是KNO3和NaCl固体的溶解度曲线,下列有关说法中正确的是
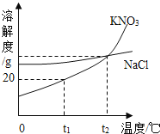
A. KNO3的溶解度受温度的影响比NaCl大
B. t1℃时,100gKNO3饱和溶液中含有20gKNO3
C. t2℃时,NaCl溶液与KNO3溶液中溶质质量分数相等
D. 若NaCl中混有少量KNO3,可用降温结晶的方法提纯NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com