
| | 实验方案及现象 | 实验结论 |
| A | ①铜丝插入硫酸锌溶液,一段时间后,无明显现象 ②铜丝插入硝酸银溶液,一段时间后,铜丝上有银白色金属析出 | 金属活动性:锌>铜>银 |
| B | ①加热KClO3制O2速度慢 ②加热KClO3和KMnO4混合物制O2速度快 | KMnO4是KClO3制取O2的催化剂 |
| C | 碳酸钙受热发生分解反应,检验到有CO2生成 | 碳酸钙中一定含有碳元素和氧元素 |
| D | ①向盛有蒸馏水的试管中加入一根铁钉(铁钉一半露置在空气中),一段时间后,铁钉生锈 ②将铁钉浸没在经煮沸并迅速冷却蒸馏水中,再加入 2 mL植物油,一段时间后,铁钉未生锈 | 与氧气接触是铁钉生锈的条件之一 |


科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.点燃氢气时发生爆炸,可能因为没有检验氢气的纯度 |
| B.稀释浓硫酸时,出现液滴大量飞溅,可能是把水向酸中倾倒的原因 |
| C.你做过的“纸船烧水”实验主要是为了探究燃烧条件中的“物质必须具有可燃性” |
| D.测定空气中氧气的体积分数时,充分放应后要冷却至室温在读数,否则测量结果偏低 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验编号 | 实验操作 | 实验现象 |
| ① | 分别在试管A、B中加入 5 mL 5%(溶液浓度) H2O2溶液,各滴入2 滴相同浓度的CuSO4溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 | 试管A中不再产生气泡; 试管B中产生的气泡量增大。 |
| ② | 另取两支试管分别加入5mL 5%H2O2溶液和5 mL 10%H2O2溶液 | 试管A、B中均未明显见到有气泡产生。 |

查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| 选项 | 目的 | 操作 | 现象 | 结论 |
| A | 检验某固体物质中是否含有碳酸根 | 取少量样品于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有气泡产生 | 该固体物质中含有碳酸根 |
| B | 检验集气瓶中是否集满二氧化碳 | 将燃着的木条伸入集气瓶中 | 燃着的木条熄灭 | 集气瓶中已集满二氧化碳 |
| C | 比较人体吸入的空气和呼出的气体中氧气的含量 | 分别向盛有空气和呼出气体的集气瓶中伸入燃着的木条 | 燃着的木条在空气中继续燃烧,在呼出气体中熄灭 | 空气中的氧气含量高于呼出气体 |
| D | 除去二氧化碳中混有的一氧化碳 | 将混合气体通过足量的澄清石灰水 | 澄清石灰水变浑浊 | 得到二氧化碳 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
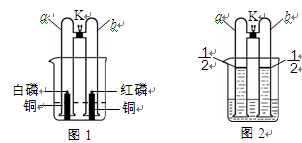
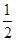 体积的氢气于两管中。再将镁条和大理石分别置于a、b管口内,向烧杯内逐滴加入浓盐酸,a、b管内均有气泡产生,其中a管反应的化学方程式是 。待两管内液体恰好全部排出后,向烧杯中加入过量的浓氢氧化钠溶液,溶液变浑浊。一段时间后,打开K,此时观察到a、b管中的现象是 。
体积的氢气于两管中。再将镁条和大理石分别置于a、b管口内,向烧杯内逐滴加入浓盐酸,a、b管内均有气泡产生,其中a管反应的化学方程式是 。待两管内液体恰好全部排出后,向烧杯中加入过量的浓氢氧化钠溶液,溶液变浑浊。一段时间后,打开K,此时观察到a、b管中的现象是 。查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验目的 | 实验步骤 | 可能的实验现象 | 化学方程式和实验结沦 |
| 探究所用 澄清石灰 水是否变 质 | ①用一支试管另取少量原澄清石灰水 ②取稀硫酸与碳酸钠反应制取CO2 ③ | 步骤③中现象为: | 步骤②中反应方程式为: 实验结论:所用的澄清石灰水没有变质。 |
| 实验目的 | 实验步骤 | 实验现象 | 化学方程式和实验结论 |
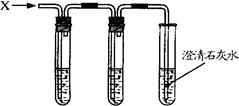
| 探究小白的假设是否成立 | 将气体X通入AgNO3溶液 | | 反应方程式为: 实验结论:小白的假设成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com