

���� ˮ��Դ����ȡ֮������֮���ߵģ�Ҫ����ˮ��Դ�ͽ�Լ��ˮ��
��� �⣺��1���������У�����ϴ��ˮ������ʹ�ý�ˮˮ��ͷ�ȣ������Խ�Լ��ˮ��
���ϴ��ˮ������
��2���ٹ��˲�������ˮ��
�������������ˮ��
�۳�����������ˮ��
����п�������ˮ��
����ڢܣ�
��3������ͼ��ʾװ�ý���ʵ�飬һ��ʱ���������A�Թ��в�������������������B�Թ��в��������������������Ϊ1��2����ʵ������з�����Ӧ�Ļ�ѧ����ʽΪ��2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2H2��+O2����
���1��2�� 2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2H2��+O2����
��4��ͨ�����ˮʵ�飬����֪��ˮ������Ԫ�غ���Ԫ����ɵģ�
�����Ԫ�غ���Ԫ�أ�
���� �������ʱ��ˮ�еĸ����ӡ�þ�����ܹ���̼��Ƴ�����������þ��������ʽ��ˮ���������Ӷ�����ˮ��Ӳ�ȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | ���� | ���� | ������̼ |
| �е㣨�棩 | -195.8 | -183.0 | -78.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
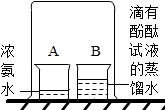 ij��ȤС��������ʵ��̽�����ӵ��˶�����ش�ʵ���е��й����⣮
ij��ȤС��������ʵ��̽�����ӵ��˶�����ش�ʵ���е��й����⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��ȡ��ʹ�� | B�� |  ���� | C�� |  ���� ���� | D�� |  ��ҩƷ����ζ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
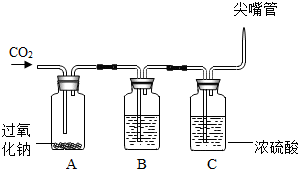
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com