
【题目】碘酸钾(KIO3)主要用作食盐加碘剂 Ⅰ、制备碘酸钾
实验室制备碘酸钾的路线如下:
干海带→I2 ![]() HIO3
HIO3 ![]() KIO3
KIO3
(1)KIO3中I的化合价为 , 含碘盐中的碘是指(填字母). a、离子 b、元素 c、分子
(2)实验中需要用试纸测定溶液的pH,其操作方法是 .
(3)过滤操作需要的玻璃仪器有玻璃棒、烧杯和 .
(4)用冰水洗涤过滤所得KIO3晶体,其原因是 .
(5)温度过高,会造成H2O2利用率降低,可能的原因是 .
(6)Ⅱ测定碘含量 资料:
①碘酸钾与碘化钾反应方程式为:KIO3+5KI+3H2SO4═3K2SO4+3H2O+3I2
②淀粉溶液遇碘显色时,碘浓度越大颜色越深;
③扬州作为轻度缺碘地区,食盐中碘含量(以I计)应为18~33mg/Kg
步骤1:配置以下各种试剂:100g/L食盐溶液,2.14×10﹣3g/L KIO3溶液,测试液(含10g/L淀粉、196g/L H2SO4、1.66g/L KI).
步骤2:取5支相同规格小试管,贴上编号标签,按下表要求分别依次加入步骤1中配置的KIO3溶液,测试液、蒸馏水,塞上橡皮塞,混合后有序放置在试管架上(各试管中KIO3完全反应).
试管编号 | 1 | 2 | 3 | 4 | 5 |
KIO3溶液滴数 | 30 | 25 | 20 | 15 | 10 |
测试液滴数 | 10 | 10 | 10 | 10 | 10 |
蒸馏水滴数 | 0 | 5 | 10 | 15 | 20 |
步骤3:另取一支小试管,一次加入步骤1中所配置的食盐溶液10滴、测试液10滴、和蒸馏水20滴,混合后与步骤2中各试管内颜色对照.
步骤3所得溶液呈色,则说明该食盐是含碘盐.
(7)步骤2实验的目的是 , 步骤2中测试液的滴数保持一致的原因是 .
(8)若步骤3所得溶液颜色与3号试管一致,则100mL该食盐溶液中含有碘酸钾mg.该食盐中碘含量为mg/Kg,扬州地区要求(填“符合”或“不符合”).
【答案】
(1)+5价;b
(2)用玻璃棒蘸取待测液滴在pH试纸上,与标准比色卡对照
(3)漏斗
(4)除去碘酸钾表面的可溶性杂质,并减小洗涤时碘酸钾的损失
(5)温度过高时双氧水会分解
(6)蓝
(7)得到不同浓度碘液的显示标准;控制测试液变量,保证各组实验中测试液浓度一致
(8)0.428;25.4;符合
【解析】解:(1)依据化合物中各元素的化合价代数和为零判断I的化合价,由于碘酸钾中钾的化合价是+1价,氧为﹣2价,计算可知碘的化合价为+5价,依据含碘盐中碘存在于碘酸钾中,所以此处的含碘盐中的碘指的是碘元素;(2)实验室中溶液pH的测量方法是用玻璃棒蘸取待测液滴在pH试纸上,与标准比色卡对照,所以此处的测量方法也不例外;(3)过滤操作中使用的玻璃仪器主要有烧杯、玻璃棒和漏斗;(4)洗涤晶体的作用去除晶体表面的可溶性杂质,由于高温时碘酸钾的溶解度较大,所以采用冰水进行洗涤可减小洗涤时碘酸钾的损失;(5)由于双氧水温度高时易分解,所以高温时会降低双氧水的利用率;(6)由于淀粉遇碘会变蓝色,所以溶液变蓝说明食盐的溶液中存在碘酸钾;(7)依据控制变量法实验的设计原理可知:步骤2是为了得到不同浓度碘液的显示标准,测试液滴数一致是为了创造相同的测试环境以便对照实验;(8)步骤3所得溶液颜色与3号试管一致且体积相同,推出两个试管中所含I2的量一样,且I2的量只与KIO3的含量有关,设该食盐溶液中碘化钾的含量是x,那么就得出这样一个等式2.14×10﹣3 g/L×0.05mL/滴×20滴=x×0.05mL/滴×10滴 解得x=4.28×10﹣3g/L即100mL食盐溶液中碘化钾的含量是0.428mg;
则碘的质量=0.428mgx ![]() =0.254mg
=0.254mg
∴m(1kg盐中碘含量)=0.254mgx ![]() =25.4mg
=25.4mg
又∵18mg<25.4mg<33mg
∴符合扬州地区要求.
所以答案是:(1)+5价;b;(2)用玻璃棒蘸取待测液滴在pH试纸上,与标准比色卡对照;(3)漏斗;(4)除去碘酸钾表面的可溶性杂质,并减小洗涤时碘酸钾的损失;(5)温度过高时双氧水会分解;(6)蓝色;(7)为了得到不同浓度碘液的显示标准;控制测试液变量,保证各组实验中测试液浓度一致;(8)0.428;25.4;符合;
【考点精析】本题主要考查了过滤操作的注意事项的相关知识点,需要掌握过滤操作注意事项:“一贴”“二低”“三靠;过滤后,滤液仍然浑浊的可能原因有:①承接滤液的烧杯不干净②倾倒液体时液面高于滤纸边缘③滤纸破损才能正确解答此题.


科目:初中化学 来源: 题型:
【题目】图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( ) 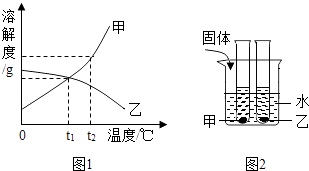
A.t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为甲>乙
B.将甲、乙两种物质的饱和溶液都从t2℃将至t1℃时,两种溶液中溶质的质量分数相等
C.向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小
D.向烧杯的水中加NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组气体中既能用浓硫酸干燥,又能用苛性钠干燥的是 ( )
A. H2、O2 B. C O 2、HCl C. SO 2、CO D. SO 2、CO 2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为甲乙两物质的溶解度曲线,下列说法正确的是( ) 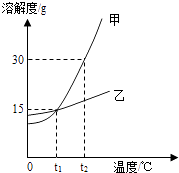
A.甲的溶解度大于乙的溶解度
B.t1℃时,甲、乙两物质饱和溶液中溶质的质量分数均为15%
C.要使接近饱和的乙溶液转化为饱和溶液,可以采用蒸发溶剂的方法
D.t2℃时,将50克甲物质放入100克水中,得到溶液的质量为150克
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】煤气中加入有特殊气味的乙硫醇可提示煤气是否泄漏.乙硫醇(用X表示)燃烧时发生的反应为:2X+9O2 ![]() 4CO2+2SO2+6H2O,则X是( )
4CO2+2SO2+6H2O,则X是( )
A.C4H12S2
B.C2H6S
C.C2H6O2
D.C2H6
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过对化学的学习,你已掌握了实验室制取气体的有关规律,请结合下图回答有关问题: 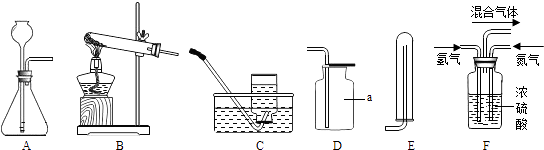
(1)图中标有a的仪器名称是 .
(2)实验室用氯酸钾制取氧气,反应的化学方程式为 , 可选择的收集装置是D或(填字母,下同).
(3)实验室用锌和稀硫酸制取氢气,应选择的发生装置是 , 反应的化学方程式为 .
(4)氨气是一种无色、有刺激性气味、极易溶于水的气体,可用于制氮肥、硝酸、药物和燃料等. ①实验室用加热氯化铵和熟石灰的固体混合物的方法制取氨气,则实验室制取并收集氨气应选择的装置组合是 .
②工业上用氮气和氢气合成氨气(反应的化学方程式:N2+3H2 ![]() 2NH3).
2NH3).
实验室模拟合成氨气的流程如下:
流程中“气体的混合”是在F装置中进行的,F装置的作用有三个:一是将氮气和氢气干燥;二是使氮气和氢气充分混合;三是 , 从而提高氮气和氢气的利用率.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com