
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | ① | 木条不复燃 | 常温下过氧化氢溶液不分解 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的小木条伸入试管中 | 木条复燃 | ② 加入水泥块能加快过氧化氢的分解速率 |
分析 (3)试验一:根据氧气具有助燃性进行分析;
实验二:根据木条复燃的现象分析;
(5)根据催化剂的定义分析需要验证的因素;
(6)根据催化剂满足的条件分析.
解答 解:(3)实验一:根据实验现象是木条不复燃,说明了是用木条在检验是否生成了氧气,对比实验二的操作,可以得出实验一的操作
实验二:根据实验现象:木条复燃,说明了氧气的存在,更说明加入水泥块后过氧化氢中有有氧气产生,
故答案为:
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入盛有过氧化氢的试管中 | 木条不复燃 | 常温下过氧化氢溶液不分解 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | 加入水泥块能加快过氧化氢的分解速率 |
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入盛有过氧化氢的试管中 | 木条不复燃 | 常温下过氧化氢溶液不分解 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | 加入水泥块能加快过氧化氢的分解速率 |
点评 在研究催化剂时,要从改变反应速率、反应前后的质量、化学性质等方面进行研究.


科目:初中化学 来源: 题型:解答题
 向烧杯中加入一定量的碳酸钠粉末,然后加入100g稀硫酸溶液,恰好完全反应.烧杯连同药品的起始质量为200g,用自动计时和称量装置每秒测量一次烧杯连同溶液的质量,所得质量与时间的关系如图所示,请完成下列问题:
向烧杯中加入一定量的碳酸钠粉末,然后加入100g稀硫酸溶液,恰好完全反应.烧杯连同药品的起始质量为200g,用自动计时和称量装置每秒测量一次烧杯连同溶液的质量,所得质量与时间的关系如图所示,请完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cl-、K+、Ba2+、NO${\;}_{3}^{-}$ | B. | CO${\;}_{3}^{2-}$、Na+、SO${\;}_{4}^{2-}$、K+ | ||
| C. | K+、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$、Ba2+ | D. | SO${\;}_{4}^{2-}$、Cu2+、Na+、OH- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 麻黄与麻黄碱均属于纯净物 | |
| B. | 麻黄碱的相对分子质量是166 | |
| C. | 麻黄碱是由四种元素组成的化合物 | |
| D. | 麻黄碱中氮、氧两种元素的质量比是1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
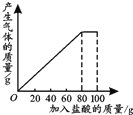 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象. | 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com