
【题目】向含有MgCl2和HCl的混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,所加NaOH溶液质量与生成沉淀的质量关系如下图所示。下列说法中正确的是( )
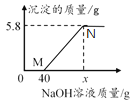
A. M点溶液中的溶质只有一种
B. 整个反应过程中,氯离子质量分数不变
C. 沉淀完全时,x的数值为80
D. N点溶液中氯化钠的质量为17.55g
【答案】D
【解析】
由图中信息可知,向含有MgCl2和HCl的混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,氢氧化钠先和盐酸反应,当盐酸完全反应后,再和氯化镁反应。A、氢氧化钠先和盐酸反应生成氯化钠和水,M点时,氢氧化钠和盐酸恰好完全反应生成氯化钠和水,M点溶液中的溶质是氯化镁和氯化钠,故A错误;B、整个反应过程中,盐酸和氢氧化钠反应生成氯化钠和水,氯化镁和氢氧化钠反应生成氢氧化钠和氯化钠,溶液中的氯离子质量不变,但溶液的质量增加,因此质量分数减小,故B错误;C、设:氯化镁消耗的氢氧化钠的质量为x,生成的氯化钠的质量为y。

![]() x=8g
x=8g
![]() y=11.7g
y=11.7g
氢氧化钠溶液的质量=![]() ,所以沉淀完全时,x的数值为40+80=120,故C错误;D、设:盐酸和氢氧化钠反应生成氯化钠的质量为z。
,所以沉淀完全时,x的数值为40+80=120,故C错误;D、设:盐酸和氢氧化钠反应生成氯化钠的质量为z。
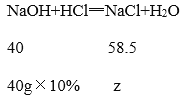
![]() z=5.85,所以N点溶液中氯化钠的质量5.85g+11.7g=17.55g,故D正确。故选D。
z=5.85,所以N点溶液中氯化钠的质量5.85g+11.7g=17.55g,故D正确。故选D。


科目:初中化学 来源: 题型:
【题目】五一假期,骑自行车出游符合“低碳出行”的理念,颇受一些年轻人的喜爱。

(1)普通自行车的辐条主要成分是铁,工业上用一氧化碳和赤铁矿(主要成分是氧化铁)冶炼铁的化学方程式为_____。
(2)在郊外野炊,把捡来的树枝架空,使其燃烧更旺,原理是_____。
(3)在郊外野炊,用“富硒大米”做饭是不错的选择。资料显示硒元素具有抗衰老、抑制癌细胞的功能。硒元素在元素周期表中有如图所示信息,下列有关说法不正确的是_____(填字母序号)。
A 硒属于金属元素
B 硒的原子核内有34个质子
C 硒的相对原子质量为78.96g
D 硒原子的原子核外有34个电子
(4)在一些城市扫描自行车上的二维码可租用“共享单车”,二维码的制作材料一般用PVC,PVC的化学式为(C2H3Cl)n,则PVC中碳元素和氢元素的质量比为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组做镁条在空气中燃烧实验时,发现生成物中有黑色固体。针对这一现象,他们猜想可能是镁与N2或CO2反应生成黑色固体。
针对猜想他们开展了如下探究活动。
【实验一】镁带与氮气的反应
(1)以下是获取氮气的方法及装置,其中得到氮气较纯的是______(填字母)
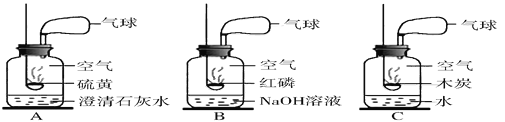
(2)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛N2的集气瓶中,瓶内壁附着一层淡黄色的固体。
(3)实验结论:镁与氮气在点燃的条件下发生化合反应,生成淡黄色的氮化镁。该反应的化学方程式是:______________________________________________。
(4)实验反思:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁?原因是_____________________________________ 。
【实验二】镁带与二氧化碳的反应
将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内产生氧化镁和一种黑色固体单质,该黑色物质是___________。(写出化学式,下同)
【探究结论】
镁在空气中燃烧产生的黑色固体是镁与空气中___________反应产生的。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸镁水合物是制备镁产品的中间体。
(制取MgCO3·3H2O)工业上从弱碱性卤水(主要成分为MgCl2)中获取MgCO3·3H2O的方法如下:
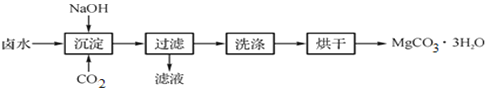
图1 获取MgCO3·3H2O的工艺流程
(1)沉淀过程的化学方程式为:MgCl2+CO2+2NaOH+2H2O![]() MgCO3·3H2O↓+2____。
MgCO3·3H2O↓+2____。
(2)沉淀过程的pH随时间的变化如图2所示,沉淀过程的操作为____(填字母)。
A 向卤水中滴加NaOH溶液,同时通入CO2
B 向NaOH溶液中滴加卤水,同时通入CO2
C 向卤水中通入CO2至饱和,然后滴加NaOH溶液,同时继续通入CO2
D 向NaOH溶液中通入CO2至饱和,然后滴加卤水,同时继续通入CO2
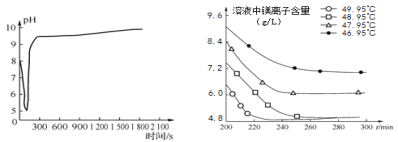
图2 沉淀过程的pH变化 图3 不同温度下溶液中镁离子含量随时间的变化
表1 不同反应温度下的水合碳酸镁
温度(℃) | 产物 |
46.95 | MgCO3·3H2O |
47.95 | MgCO3·3H2O |
48.95 | MgCO3·3H2O |
49.95 | Mg5(OH)2(CO3)4·4H2O |
(3)沉淀过程的溶液中镁离子含量随时间的变化如图3所示,不同温度下所得到沉淀产物如表1所示。则沉淀过程选择的温度为____,理由是____。
(测定MgCO3·3H2O的纯度)
利用下图所示装置(图中夹持仪器略去)进行实验,以确定MgCO3·3H2O的纯度。
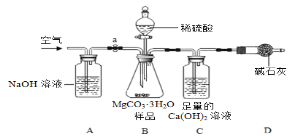
依据实验过程回答下列问题:
(1)实验过程中需持续____(选填“缓缓”或“迅速”)通入空气,其作用除了可搅拌B、C中的反应物外,还有____。D中碱石灰的作用为____。
(2)下列各项措施中,不能提高测定准确度的是____(填标号)。
A 在加入硫酸之前,应排净装置内的CO2气体
B 为了缩短实验时间,快速滴加硫酸
C 在A~B之间增添盛有浓硫酸的洗气装置
D 在C装置左侧导管末端增添多孔球泡
(3)实验中准确称取15.0 g样品三份,进行三次测定,测得中生成CaCO3沉淀的平均质量为10.0 g。请计算样品中MgCO3·3H2O的纯度________
(4)小明认为应将澄清石灰水换成Ba(OH)2溶液,其理由除了Ba(OH)2溶解度大,浓度大,使CO2被吸收的更完全外,还有____。
(5)若获取MgCO3·3H2O的样品中含有少量Mg5(OH)2(CO3)4·4H2O,则样中MgCO3·3H2O的纯度____(填“偏大”或“不变”或“偏小”)
查看答案和解析>>
科目:初中化学 来源: 题型:
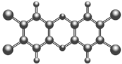
【题目】每年5月31日是“世界禁烟日”。香烟燃烧产生的烟气中含有多种对人体有害的物质,其中的二噁英毒性很强。它是一种无色无味的物质,化学式为C12H4Cl4O2,分子结构如下图所示。通常情况下,它极难溶于水、易溶于脂肪,所以容易在生物体内积累,难以被排出。
回答下列问题:
(1)二噁英属于_______(填“无机物”或“有机物”)。
(2)写出二噁英的物理性质:_________(写出一条即可)。
(3)1个二噁英的分子中含有_______个原子,二噁英中碳、氢两种元素的质量比为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质在水中形成的饱和溶液溶质质量分数随温度变化如下图所示,请回答下列问题:
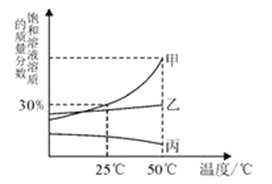
(1)25℃时,甲物质中的溶解度为______g(答案保留一位小数);
(2)从乙溶液中获得乙晶体的方法是_____________(填“蒸发结晶”或“降温结晶”)。
(3)将50℃甲的饱和溶液降温至25℃,溶液为________(填“饱和溶液”或“不饱和溶液”)。
(4)气体的溶解度随温度的变化规律与_________(填“甲”、“乙”或“丙”)相似。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】合理利用能源和保护环境是我们关注的问题。
![]() 目前人类使用的主要化石燃料包括煤、______、天然气。化石燃料燃烧会导致温室效应加剧。请说出温室效应加剧的一点危害______。
目前人类使用的主要化石燃料包括煤、______、天然气。化石燃料燃烧会导致温室效应加剧。请说出温室效应加剧的一点危害______。
![]() 抚顺的燃气改造工程,使更多的居民家中用上了天然气。天然气燃烧的化学方程______。
抚顺的燃气改造工程,使更多的居民家中用上了天然气。天然气燃烧的化学方程______。
![]() 化石燃料面临耗尽的危险,应合理开采、使用和开发新能源,埋于海底将来可能会替代化石燃料的新能源是______。
化石燃料面临耗尽的危险,应合理开采、使用和开发新能源,埋于海底将来可能会替代化石燃料的新能源是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①锌和稀硫酸;②石灰石和盐酸;③硝酸铵和水;④固体氢氧化钠和水
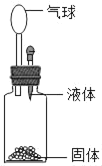
A. ①②B. ①②④C. ①④D. ①③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4nH2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料,某化学兴趣小组设计利用废弃铁锈合成草酸亚铁晶体并检验其热分解的产物及探究它的组成。
(一)制备草酸亚铁晶体(FeC2O4·nH2O)
资料1:FeSO4的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 15.6 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 | 59.8 |
资料2:草酸亚铁难溶于水,在酸性条件下稳定存在。
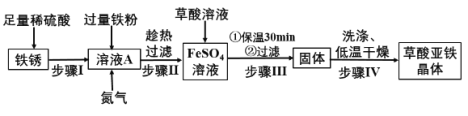
(制备流程)
(1)在实验室进行“过滤”操作时,需要的玻璃仪器有烧杯、漏斗和______,其作用是___
(2)步骤Ⅱ中趁热过滤的目的是______。
(3)草酸(H2C2O4)溶液加入FeSO4溶液中发生了复分解反应,请写出该反应的化学方程式为______。
(4)步骤Ⅲ中保温反应30min的目的是______。
(二)检验草酸亚铁晶体(FeC2O4·nH2O)热分解的产物及探究n的值
(实验装置)
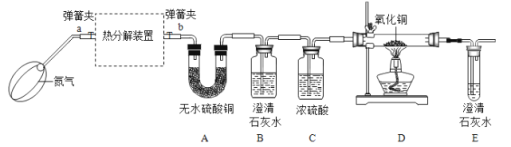
资料3:FeC2O4·nH2O加热至300℃完全失去结晶水;继续加热至400℃,剩余固体受热分解产生铁的氧化物、CO2和CO。
(实验分析)
(5)打开弹簧夹a、 b,先鼓入一段时间的氮气,然后再关闭a,加热分解装置的原因是______。
(6)若通过E装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解产生CO,则需在B和C装置之间增加盛有______(填试剂名称)的洗气瓶。
(7)装置D硬质玻璃管中出现的现象是______。
(8)取7.20gFeC2O4·nH2O,按上述实验步骤进行实验,测得热分解装置中固体质量随温度变化曲线如图所示:
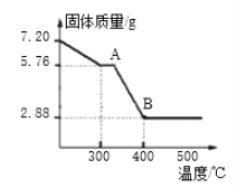
①FeC2O4·nH2O中n的值为______。(写出计算过程)
②若草酸亚铁晶体中混有杂质(杂质不参加反应),会导致测得的n的值______(选填“偏大”、“偏小”、“不变”)。/p>
③写出曲线中A至B发生反应的化学方程式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com