
����Ŀ����ʽ̼��ͭ��Cux��OH��y��CO3��z����һ����;�㷺�Ļ���ԭ�ϣ�ʵ������ȡ��ʽ̼��ͭ�IJ������¡�
��֪����Cu+4HNO3��Ũ����Cu��NO3��2+2NO2��+4H2O����2NO2+2NaOH��NaNO3+NaNO2+H2O
����һ����Na2CO3
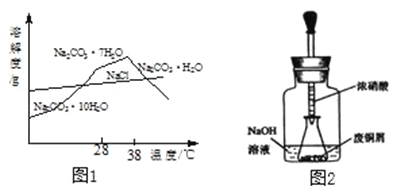
��Na2CO3��Һ��������NaCl���ᴿ���Na2CO3����IJ������£�����Ũ����38�����Ͻᾧ�����ȹ��ˣ�ϴ�ӣ�������ˮ����Na2CO3���塣�����ͼ1�ش�
��1��38�����Ͻᾧ��Ŀ����_____��
��2��ϴ��ʱ�����˵��Լ���_____��
a��ˮ b��ˮ c���� dCa��OH��2��Һ
���������Cu��NO3��2
��ͼ2���õι���ȡŨHNO3�����ӵ���ƿ�ڵķ�ͭм�У���ͭм����������ַ�Ӧ����ˣ��õ�Cu��NO3��2��Һ��
����������ʽ̼��ͭ���Ʊ�
����Թ��м���Na2CO3��Һ��Cu��NO3��2��Һ��ˮԡ������70�����ң���NaOHϡ��Һ����pH��8.5�������ã����ˣ�����ˮϴ�ӣ���ɣ��õ���ʽ̼��ͭ��Ʒ��
��3����ͼװ����NaOH��Һ��������_____����Ӧ�������ƿ����Һ�е�������NaOH��_____��_____����д��ѧʽ����
��4���������У�ˮԡ��������������_____��_____ �����ȡ��г�������ʯ�������⣩��ϴ�ӵ�Ŀ����_____��
��5��Ӱ���Ʒ��������Ҫ������_____��_____��
��6�����ȼ�ʽ̼��ͭ��Cux��OH��y��CO3��z����40 g CuO��3.6 g H2O����x��y��z��_____��
���𰸡��õ�Na2CO3H2O���壬���̼�����ˮ��ʱ�� a ����NO2 NaNO3 NaNO2 �ձ� �¶ȼ� ��ȥNaNO3 pH �¶� 5��4��3
��������
��1������ͼ��֪��38�����Ͻᾧ�õ���̼���ƾ��庬�ᾧˮ�٣�ΪNa2CO3H2O���壬���̼�����ˮ��ʱ�䡣
��2�������¶ȸ�ʱ��Na2CO3H2OС������ϴ��ʱ�ܼ�����ʧ������ϴ��ʱ���˵��Լ�����ˮ����ѡ��a��
��3��������Ϣ��֪��2NO2+2NaOH��NaNO3+NaNO2+H2O��������ͼװ����NaOH��Һ������������NO2��������Ϣ��֪�������ﻹ��NaNO3��NaNO2�����Է�Ӧ�������ƿ����Һ�е�������NaOH��NaNO3��NaNO2��
��4���������У�ˮԡ�������������� �ձ����¶ȼ� �������¶���38�������ã���ϴ�ӵ�Ŀ���� ��ȥNaNO3��
��5�����ݹ����п��Ƶķ�Ӧ������֪��Ӱ���Ʒ��������Ҫ������ pH�� �¶ȡ�
��6�����ȼ�ʽ̼��ͭ��Cux��OH��y��CO3��z����40 g CuO��3.6 g H2O����ͭԭ�Ӻ���ԭ�Ӹ�����Ϊ![]() ��5��4����Cu5��OH��4��CO3��z�����ݻ��������������ϼ۵Ĵ�����Ϊ��ɵã�+2����5+����1����4+����2����z��0��z��3��x��y��z��5��4��3��
��5��4����Cu5��OH��4��CO3��z�����ݻ��������������ϼ۵Ĵ�����Ϊ��ɵã�+2����5+����1����4+����2����z��0��z��3��x��y��z��5��4��3��
�ʴ�Ϊ��
��1���õ�Na2CO3H2O���壬���̼�����ˮ��ʱ�䡣
��2��a��
��3������NO2�� NaNO3��NaNO2��
��4���ձ����¶ȼƣ� ��ȥNaNO3��
��5��pH�� �¶ȡ�
��6��5��4��3��


 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д� ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ���������������ͼװ���Ƶ��������ͼʾ�ش��������⣺

��1��д���б�����������ƣ�a��_____��
��2��ʵ���п�����ʵ������Ϊ��A���������еķ�ĩ_____��B���Թ���ij���ʯ��ˮ_____��
��3����ȼβ���Ļ�ѧ����ʽ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС����һ����AgNO3��Al(NO3)3�Ļ����Һ��������ͼʵ�飬��֪��Һ�׳���ɫ��

(1)��������ϵμ�����ʱ____________(������������û����)���ݲ�����
(2)��Һ����һ��������Щ���ʣ�(д��ѧʽ)__________________
(3)��д����ʵ���������������Ӧ�Ļ�ѧ����ʽ��______________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭǮ����ʷ��������һ�ֹ㷺��ͨ�Ļ��ң���֪ͭ���۵���1083��4�棬�����۵���1534��8�档
��1������������ʽǶ�˵��Ϊʲô��ͭ�����������������_______��
��2������1����ѧ����ʽ˵�����Ľ�����Ա�ͭ��ǿ_______��
��3��ͭ��Ũ�����ڼ���ʱ��Ӧ��������ͭ�����������ˮ��д���÷�Ӧ�Ļ�ѧ����ʽ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�����ᴿ���ʵķ����У������ݵ�ԭ����ȷ����![]() ����
����![]()
ѡ�� | �����ķ�����ᴿ | ����ԭ�� |
A | ����Һ̬������ȡ���� | ���õ������������۵㲻ͬ |
B | ��ʯ�ͷ���õ�ʯ�Ͳ�Ʒ | ʯ���и��ɷֵ��ܶȲ�ͬ |
C | ��������غ��Ȼ�����ɵĻ���� | ����غ��Ȼ��Ʒֽ��¶Ȳ�ͬ |
D | ��ȥ�����е���ɳ | �Ȼ��ƺ���ɳ���ܽ��Բ�ͬ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ�ס������ֹ���������ˮ�е��ܽ�����ߡ�����˵��������ǣ�������
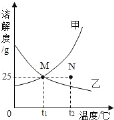
A. �����ʵ��ܽ�����¶ȵ����߶�����
B. ��t1��ʱ���ס��������ʵ��ܽ�����
C. ��t2��ʱ��N���ʾ�����ʵIJ�������Һ
D. ��t1��ʱ�������ʵı�����Һ�����ʵ�����������25%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Һ�������ճ�����������ء�
��1���������ʷ���ˮ�����γ���Һ����_____������ţ���
A ���� B ɰ�� C ��� D ����
��2���·��ϲ���ճ�����ۣ���ѡ��_____����������������ϴ�ྫ�������ɽ����ܽ����ȥ��
��3��ũҵ�ϳ����Ȼ�����Һѡ�ÿ������������ӣ���ȷ����ѿ�ʺ���ľ׳ʵ������Ҫ����2000 g��������Ϊ11%���Ȼ�����Һ������Ҫ��ȡ���������Ϊ_____ g��
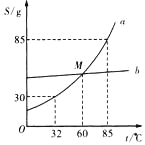
��4������a��b���ֹ������ʣ����ܽ����������ͼ��ʾ�����ͼʾ����������⡣
�ٵ�M��ʾ������Ϊ_____��
���ڱ���85�治���ǰ���£���b���ʵIJ�������Һת��Ϊ������Һ�ķ���Ϊ_____��
����32��ʱ����30 g��a���ʷ���50 gˮ�У�������Һ������Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ƻ���и���ƻ���ᣬ������ǿ���������͵��̴������ã�ƻ����ķ���ʽΪC4H6O5������㣺
(1)ƻ������___��Ԫ����ɡ�
(2)һ��ƻ���������___��ԭ�ӹ��ɡ�
(3)ƻ�������Է���������___��
(4)ƻ������̼���⡢������Ԫ�ص���������___(���������)��
(5)13.4gƻ�����к�CԪ������___�ˣ�(д��������̣��𰸾�ȷ��0.1)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��ͬѧ����һ���Է�����������ǩ��ͼ1����������Ȥ������ù��ķ������������ڲ��Ǻ�ɫ���壬����չ��̽����


���������ϣ��������ķ���ԭ���������ڿ����з������������ų�������
������1���������е������Ƿ���ȫ��������
�����룩�����������ȫ������ ��������۲��ֱ�����
��̽��1��ȡ��ɫ�������ձ��У���������ϡ���ᣬ�����ݲ�������ַ�Ӧ����ˣ���ҺΪ��ɫ������Ϊ��ɫ���û�ѧ����ʽ��ʾ��Һ��Ƶ�ԭ��____________________________________________��
����ʵ�������֪������_______������
������2����ɫ�����к���ʲô���ʣ�
��̽��2��ͬѧ�ǽ���������������ڳ��������ļ���ƿ�г��ȼ�գ��۲쵽��������ȼ�գ������⡣��ƿ��ע�����ʯ��ˮ��ʯ��ˮ����ǡ�˵����������______________���������֪ʶ�����ϣ�������֪������Ҳ�Ƿ������е�һ�ֳɷ֡�
����ͬѧ������֤�������д����Ȼ��ƣ�����ȡ��̽��1���еĻ�ɫ��Һ���μ�AgNO3��Һ���۲쵽__________________________������Ϊ�������д����Ȼ��ơ�
ijͬѧ��Ϊ��ʵ�鲻��֤����������һ�������Ȼ��ƣ�������_____________________________��
������3�����������Ȼ�����ʲô���ã�
��̽��3��ͬѧ�ǽ�����ϣ��ع����֪ʶ�����뵽����ʴ������ˮ�������йأ����������η��йأ���Ʋ�������ͼ2ʵ�飬�۲쵽B����������Ͽ졣
�����サ��������Ϊ���������Ȼ��Ƶ�������_________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com