
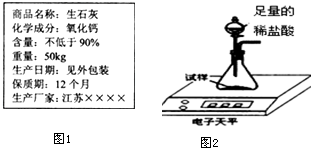
 石灰石有许多重要的用途.
石灰石有许多重要的用途.| 实验操作 | 实验现象 | 实验结论 |
| 第一步操作:取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有 氧化钙 |
| 第二步操作:再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有 碳酸钙 |
分析 【猜想与假设】根据猜测A、B的结论进行分析;
【设计并完成实验】根据操作步骤和现象,说明固体成分中一定含有氧化钙;再取少量固体于另一试管中滴加过量稀盐酸,有气泡生成,说明固体成分中一定含有碳酸钙;
【实验结论】根据【设计并完成实验】进行分析;
【定量测定】根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,固体减少的质量就是二氧化碳的质量,求出碳酸钙的质量,剩余的0.2g固体是不能溶解的杂质,然后计算氧化钙的质量分数;
【问题讨论】根据挥发出的水蒸气计入二氧化碳的质量进行分析.
解答 解:【猜想与假设】碳酸钙高温煅烧,得到氧化钙和二氧化碳;碳酸钙为白色固体,分解生成的氧化钙也为白色固体.所以固体的成分可能全部是碳酸钙和杂质;既有碳酸钙,也有氧化钙和杂质;全部是氧化钙和杂质;
碳酸钙在高温的条件下生成氧化钙和二氧化碳,取少量固体于试管中,加适量水震荡后静置,再滴几滴无色酚酞试液;溶液变红,说明固体成分中一定含有氧化钙;再取少量固体于另一试管中滴加过量稀盐酸,有气泡生成,说明固体成分中一定含有碳酸钙,所以
| 实验操作 | 实验现象 | 实验结论 |
| 第一步操作:取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有氧化钙 |
| 第二步操作:再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有碳酸钙 |
| 实验操作 | 实验现象 | 实验结论 |
| 第一步操作:取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有氧化钙 |
| 第二步操作:再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有碳酸钙 |
点评 本考点考查的是物质的鉴别,本题中有碳酸钙、生石灰和熟石灰的相互转化关系,生石灰转化成熟石灰时,会放出大量的热,要由现象得出正确的结论.解决本考点需要根据实验现象,综合分析,从而得出正确的结论.


科目:初中化学 来源: 题型:解答题
| 原子种类 | 原子核 | 核外电子数 | 相对原子质量 | |
| 质子数 | 中子数 | |||
| 氢 | 1 | 0 | 1 | 1 |
| 钠 | 11 | 12 | 11 | 23 |
| 铁 | 26 | 30 | 26 | 56 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作步骤 | 实验现象 | 结论 |
| 将产生的气体收集到试管中,伸入带火星的木条 | 木条复燃 | 该气体是O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg>Al>Fe | B. | Al>Mg>Fe | C. | Fe>Mg>Al | D. | Mg═Al═Fe |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
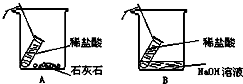 小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳和水、氯化钙;与氢氧化钠生成水和氯化钠)
小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳和水、氯化钙;与氢氧化钠生成水和氯化钠)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ①②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com