
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:初中化学 来源: 题型:选择题
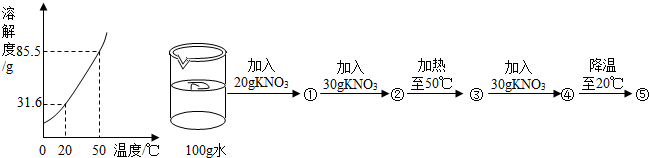
| A. | 保持温度不变,若在④中加入4.5 g KNO3固体可得到饱和溶液 | |
| B. | ②③⑤中溶质的质量分数相等 | |
| C. | ①③④均为不饱和溶液 | |
| D. | ④→⑤可析出53.9 g KNO3晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:选择题
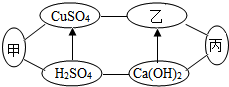 图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去).下列说法中不正确的是( )
图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去).下列说法中不正确的是( )| A. | 甲、乙、丙可能依次为Fe、NaOH、CO2 | |
| B. | 丙物质可能是氧化物或盐 | |
| C. | 当乙为NaOH时,它可由Ca(OH)2与Na2CO3反应生成 | |
| D. | 当甲为一种碱时,它与硫酸铜溶液的反应为复分解反应,且最多只能产生一种沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  食盐没有全部溶解就过滤 | |
| B. |  蒸发过程中晶体飞溅 | |
| C. |  蒸发所得的精盐较潮湿 | |
| D. |  蒸发皿中的精盐没有全部转移到称量纸上 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验序号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀硫酸的质量(克) | 20 | 20 | 20 | 20 |
| 充分反应后剩余固体的质量(克) | 17.2 | 14.4 | 12.0 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该物质属于有机化合物 | B. | 该物质中硫元素质量分数最小 | ||
| C. | 该物质由8种元素组成 | D. | 该物质的一个分子中含有77个原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com