

分析 (1)①若将二氧化碳通入澄清的石灰水中,二氧化碳和石灰水反应生成碳酸钙和水;溶液的碱性变小(氢氧化钙被消耗)去分析;
②由于氢氧化钠溶液和二氧化碳反应生成碳酸钠和水,要证明二氧化碳和氢氧化钠反应,只要证明反应生成了碳酸钠即可;
(2)①要证明塑料只含C,H,O三种元素,可让塑料在氧气中燃烧,测出生成的二氧化碳和水的质量,根据质量守恒定律,利用二氧化碳和水的质量可求出塑料中C、H、O三种元素的质量.根据题目要求和各装置的作用排出正确的顺序即可;
②根据A装置内以过氧化氢溶液为原料(MnO2为催化剂)制备氧气,产生水和氧气去分析;
③根据二氧化碳能使澄清的石灰水变浑浊.D装置增加的质量就是生成的二氧化碳的质量;根据质量守恒定律:塑料中碳元素的质量和生成的二氧化碳中碳元素的质量相等去分析.
解答 解:(1)①若将二氧化碳通入澄清的石灰水中,二氧化碳和石灰水反应生成碳酸钙和水;溶液的碱性变小,所以溶液的pH变小;故答案为:减小;
②由于氢氧化钠溶液和二氧化碳反应生成碳酸钠和水,要证明二氧化碳和氢氧化钠反应,只要证明反应生成了碳酸钠即可.可取少量反应后的溶液,滴入CaCl2溶液,产生白色沉淀,证明CO2和NaOH溶液确实发生了化学反应(NaCl溶液和氢氧化钠溶液、碳酸钠溶液都不反应,故不选;由于碳酸钠溶液和氢氧化钠溶液都显碱性,滴加酚酞溶液都显红色;故不选).故答案为:CaCl2溶液,取少量反应后的溶液,滴入CaCl2溶液,产生白色沉淀,说明溶液中含有碳酸钠,证明CO2和NaOH溶液确实发生了化学反应.
(2)①要证明塑料只含C,H,O三种元素,可让塑料在氧气中燃烧,测出生成的二氧化碳和水的质量,根据质量守恒定律,利用二氧化碳和水的质量可求出塑料中C、H、O三种元素的质量.其中A装置和特点是固体和液体反应且不需加热,故可用来制取氧气,此时氧气中含有一定量的水蒸气,故要除去(B装置中有浓硫酸,浓硫酸具有吸水性,可降去氧气中的水分),塑料在E中燃烧,产生的气体先被B吸收(根据B装置质量的增加可求生成水的质量),再通过D装置(装置内石灰水可吸收二氧化碳,可根据质量的增加求出二氧化碳的质量),为防止空气中的水分和二氧化碳进入D装置,故在D后可加G装置;故答案为:A→B→E→B→D→G;
②A装置内以过氧化氢溶液为原料(MnO2为催化剂)制备氧气,产生水和氧气,反应的方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③二氧化碳能使澄清的石灰水变浑浊.D装置增加的质量就是生成的二氧化碳的质量,二氧化碳中碳元素的质量=ag×$\frac{12}{12+16×2}$×100%=$\frac{3a}{11}$g;根据质量守恒定律:塑料中碳元素的质量和生成的二氧化碳中碳元素的质量相等.故塑料中碳元素的质量分数为:$\frac{3a}{11}$g÷mg×100%=故答案为:$\frac{300a}{11m}%$.
点评 本题考查了常见气体的制取、干燥、除杂、收集及反应原理的书写等.综合性较强,在利用氧气的性质测定塑料的组成元素时,要注意区分各步操作的作用和目的,利用质量守恒定律进行相关问题的分析.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
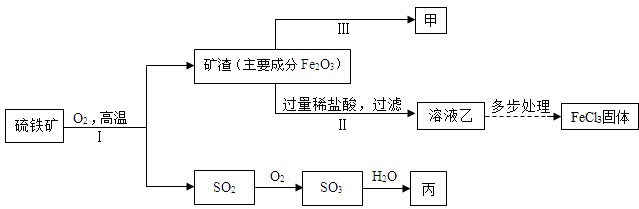
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 称取5.0g氯化钾,溶解在95mL水中,充分搅拌 | |
| B. | 量取5.0mL过氧化氢溶液,放入入95mL水中,充分搅拌 | |
| C. | 量取5.0mL浓盐酸,倒入95mL水中,充分搅拌 | |
| D. | 称取5.0g碳酸钙,放入95mL水中,充分搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
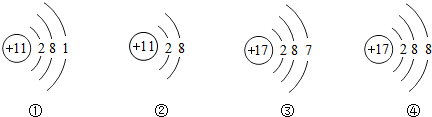
| A. | ①②属于同种元素 | B. | ②④具有相对稳定结构 | ||
| C. | ①③都容易失去电子 | D. | ②④形成的化合物为NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
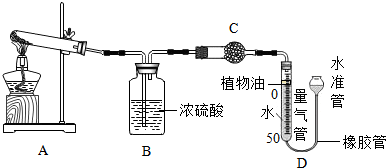
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
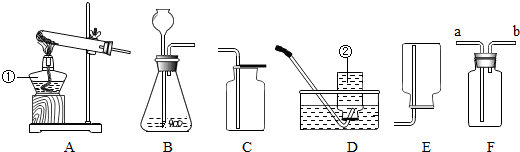
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
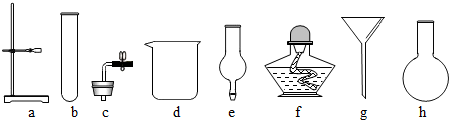
| A. | a b c d | B. | a b d f | C. | a c d e | D. | a b c e |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com