
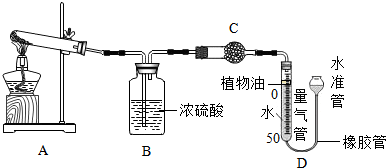
分析 ①使用或制取气体的实验要求先检查装置的气密性;
Ⅱ、根据浓硫酸的吸水性可以干燥气体;少量植物油可以防止二氧化碳溶于水;硫酸铜可以验证二氧化碳气体是否干燥完全;
Ⅲ、根据液面越低压强越小进行解答;
Ⅳ、根据能使生成的气体体积增加考虑;
解答 解:①改装置使用时必须密封进行,所以实验前一定要先检查装置的气密性;
Ⅱ、浓硫酸的吸水性可以除去二氧化碳中的水;少量植物油可以隔离二氧化碳和水,防止二氧化碳溶于水;硫酸铜可以验证二氧化碳气体是否干燥完全;
Ⅲ、液面越低压强越小,所以加热A时,随着碳酸盐样品分解,量气管内的液面逐渐下降,为防止量气管内气体压强过大,可将水准管缓慢下移;
Ⅳ、本实验主要通过测量二氧化碳的体积,通过密度已知可以计算二氧化碳的质量,进而计算碳元素的质量,
根据$\frac{{M}_{C}}{M盐}$=$\frac{{m}_{C}}{m盐}$
得${M}_{盐}=\frac{{m}_{盐}}{{m}_{C}}{M}_{C}$,据此公式进行分析;
a、应前量气管水面到0刻度处,反应后仰视读数,读数偏大,二氧化碳体积偏大,mC偏大,M盐偏小;b、样品未分解完全即停止实验,可导致实际测得气体的体积偏小,mC偏小,M盐偏大;c、量气管中未加植物油,二氧化碳溶于水,可导致实际测得气体的体积偏小,mC偏小,M盐偏大,故选bc;
答案:(1)检查气密性;
Ⅱ、吸收水蒸气;防止CO2溶于水;C;
Ⅲ、缓慢下移;
Ⅳ、b c.
点评 本题通过提出问题、做出猜想、设计实验方案、进行实验等环节,体现了科学探究的一般过程.但本题计算量较大,要求学生对知识掌握程度较高,是一道综合性较强的题目的难题.


科目:初中化学 来源: 题型:选择题
| A. |  食盐没有全部溶解就过滤 | |
| B. |  蒸发过程中晶体飞溅 | |
| C. |  蒸发所得的精盐较潮湿 | |
| D. |  蒸发皿中的精盐没有全部转移到称量纸上 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 第一次反应停止时B剩余0.9克 | B. | 第一次反应停止时C剩余0.9克 | ||
| C. | 参加反应A与C的质量比是5:3 | D. | 第二次反应停止时C剩余0.9克 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图所示,向盛水的烧杯中放入一小粒品红,一段时间后,烧杯中形成红色溶液,此实验能说明( )
如图所示,向盛水的烧杯中放入一小粒品红,一段时间后,烧杯中形成红色溶液,此实验能说明( )| A. | 分子处于不断运动之中 | B. | 分子之间有间隔 | ||
| C. | 分子可再分,原子不能再分 | D. | 分子大,原子小 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
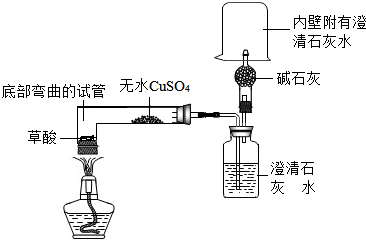 菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸含量明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究:
菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸含量明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com