
【题目】2019年1月,被称为“第一部中国自己的科幻大片”《流浪地球》受到极大关注。
(1)影片中幻想了因太阳氦闪,地球将被摧毁。氦气属于_____(填“单质”或“化合物”),你的判断依据是_____。
(2)影片中幻想了将木星上氢气点燃,达到使地球脱离木星控制的目的。氢气燃烧的化学方程式是_____。
(3)氢能是清洁能源之一,而石油是化石燃料之一。下列属于石油综合利用产品的是_____。
A 液化石油气 B.汽油 C 柴油 D 煤油
(4)偏二甲肼是一种运载火箭的推进燃料,其相对分子质量为60。取一定量偏二甲肼在氧气中完全燃烧,反应前后各物质的质量如下图所示,偏二甲肼在氧气中完全燃烧的化学方程式是_____。
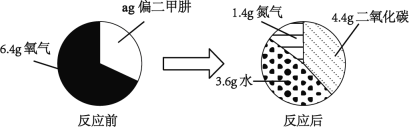
【答案】单质 氦气是一种元素组成的纯净物 ![]() ABCD C2H8N2+4O2
ABCD C2H8N2+4O2![]() 2CO2+N2+4H2O
2CO2+N2+4H2O
【解析】
(1)氩气是由一种元素组成的纯净物,属于单质;
(2)氢气与氧气在点燃的条件下反应生成水;化学方程式是:![]() ;
;
(3)液化石油气、汽油、柴油和煤油均属于石油综合利用的产品;
(4)根据扇形图,可以确定参加反应的偏二甲肼的质量1.4g+3.6g+4.4g-6.4g=3g,化学方程式中,偏二甲肼、氧气、氮气、水、二氧化碳的化学计量数的比是:![]() :
:![]() :
:![]() :
:![]() :
:![]() =1:4:1:4:2,然后根据化学反应前后原子个数相等和相对分子质量能确定偏二甲肼的化学式是C2H8N2,偏二甲肼与氧气在点燃的条件下反应生成氮气、水和二氧化碳;化学方程式是:C2H8N2+4O2
=1:4:1:4:2,然后根据化学反应前后原子个数相等和相对分子质量能确定偏二甲肼的化学式是C2H8N2,偏二甲肼与氧气在点燃的条件下反应生成氮气、水和二氧化碳;化学方程式是:C2H8N2+4O2![]() 2CO2+N2+4H2O。
2CO2+N2+4H2O。


科目:初中化学 来源: 题型:
【题目】实验室里收集了一些溶质为 FeSO4 和 CuSO4 的废液,从中回收金属铜和硫酸亚铁溶液,设计了如下方案:
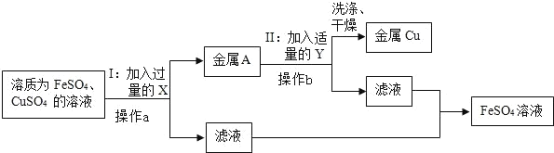
①步骤 I 中有关反应的化学方程式是 ___。
②步骤 II 中所加试剂 Y 的名称是 ___。
③加入过量 X 的目的是 ___。
④操作 a 和 b 的名称是 ___,所需要的主要玻璃仪器有烧杯、漏斗和 ___。
⑤上述步骤 ___(选填步骤编号)所包含的反应体现铁的活动性比铜强。
⑥步骤 II 中经过洗涤、干燥可以得到纯净的金属铜,洗涤时检验金属铜是否已洗净的方法是 ___
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法正确的是
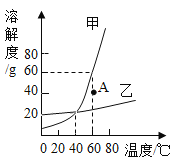
A. 甲、乙物质都适用降温结晶法使溶质从溶液中析出
B. 60℃时将40g甲物质加入50g水中能得到90g饱和溶液
C. 通过降温能使A点甲的不饱和溶液变为饱和溶液
D. 分别将甲、乙物质饱和溶液从60℃降至20℃,甲析出晶体较多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是目前使用最广泛的金属。
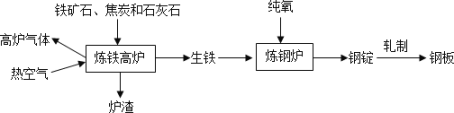
(一)工业上炼铁炼钢和轧制钢材的主要流程如图。
(1)高炉炼铁中生成一氧化碳的反应,用化学方程式表示:______。
(2)炼铁的固体原料需经过粉碎,其目的是______。
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是______。
(4)炼钢炉中,通入纯氧的目的是______。将钢锭轧成钢板,体现了金属的______性。
(二)工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4.为了测定铁红中的质量分数,某兴趣小组进行了如下实验。
(查阅资料)
①草酸(H2C2O4)固体与浓硫酸混合加热会产生一氧化碳,化学反应方程式为H2C2O4![]() CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
②NaOH溶液可以吸收二氧化碳。
③浓硫酸具有强烈的吸水性,可以除去气体中的水分。
④碱石灰可以吸收二氧化碳和水。
⑤氧化亚铁、氧化铁、四氧化三铁中铁的质量分数分别为77.8%、70%和72.4%。
(5)加热分解草酸晶体最.适.宜.的装置是________(填字母序号)。
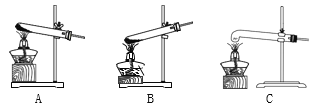
(问题讨论)用下图所示装置进行实验:
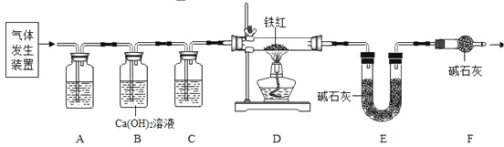
(6)实验前应先______
(7)进入D中的气体是纯净干燥的CO,则A、C中的试剂依次是________(填字母编号)a.浓硫酸b.澄清的石灰水c.氢氧化钠溶液
(8)B装置的作用是________
(9)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:①加热前____②停止加热后______
(10)写出D装置中主.要.发生反应的化学方程式________
(数据分析与计算)
(11)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①D中充分反应后得到Fe粉的质量为mg,则________<m<________(结果保留到0.1)
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是___。
(实验评价)
(12)反思1:本实验如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会________(填“偏小”、“不变”或“偏大”)。
反思2:请指出(问题讨论)中实验装置的一个明显缺陷______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】银白色的金属钠是化学实验室中常见的药品,其化学性质十分活泼。某化学兴趣小组的同学,进行如下探究活动。
[查阅资料]
将一小块银白色的金属钠放置在空气中会发生下列变化:
钠![]() 钠的氧化物
钠的氧化物![]() 氢氧化钠溶液
氢氧化钠溶液![]() 白色固体
白色固体
[查阅资料]
A.钠的氧化物有氧化钠(Na2O)和过氧化钠(Na2O2),都能与水反应,反应化学方程式
如:Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
B.CaCl2溶液呈中性;碳酸钠溶液能与CaCl2溶液发生复分解反应;
C.碳酸钠溶液与盐酸反应方程式有:
Na2CO3 +HCl=NaHCO3 +NaCl(盐酸量不足)
Na2CO3+2HCl=2NaCl+H2O+CO2↑(盐酸量过量)
探究一:钠的氧化物是Na2O还是Na2O2 ?
(1)为检验常温下钠与氧气反应的产物,是Na2O还是Na2O2,完成实验方案:
选取试剂 | 实验现象 | 实验结论 |
__________ | __________ | 产物为Na2O |
探究二:白色固体是NaOH还是Na2CO3 ?
(2) 钠在空气中放置一段时间得到白色固体的成分
猜想1:Na2CO3 猜想2:NaOH 猜想3:Na2CO3和NaOH
[实验1] 取少量白色固体加水配成溶液,再滴入几滴稀盐酸,无气泡产生。
化学小组认为:据此现象,还不能得出猜想2成立。理由是________________。
[实验2] 化学小组进行如下实验
实验操作 | 实验现象 | 实验结论 |
①取少量白色固体配成溶液,加入足量______ | __________ | 猜想3成立 |
②过滤,取少量滤液滴入___________ | __________ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关电解水实验(如图)的叙述中,不正确的是( )
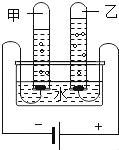
A. 试管甲中的气体可以燃烧
B. 该实验证明水是由氢元素和氧元素组成
C. 正极与负极产生的气体的质量比是1:8
D. 正极与负极产生的气体的体积比是1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图a是铯元素在元素周期表中的信息,图b是铝原子结构示意图,图c为元素周期表的一部分,X、Y、Z代表三种不同元素.
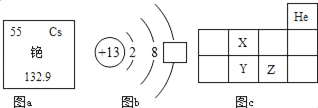
(1)由图a可知,铯元素它属于_____(填“金属”或“非金属”),该元素的原子核外电子数为_____,图中的132.9表示铯元素的_____.
(2)图b方框内的数字是_____;该原子在化学反应中容易_____(填“得到”或“失去”)电子,形成稳定结构,其离子符号为_____.
(3)有关图C的说法,正确的是_____(填序号).
A 原子序数:Z>Y B 核外电子数:X=Y C Y和Z同处于第二周期 D Z属于稀有气体元素
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱与氯化铵的联合制碱工艺,同学们查阅相关资料并进行模拟实验.
(查阅资料)
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示:
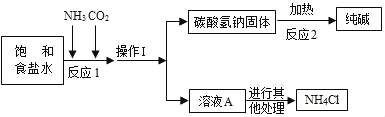
③氨气(NH3)是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
(理论分析)
(1)依据资料①可知相同条件下,NaHCO3的溶解度_____NH4Cl的溶解度(填“>”或“<”).
(2)NaHCO3受热分解制得纯碱及两种常见的氧化物,该反应的化学方程式是_____.
(模拟实验)验证侯氏制碱法能获得纯碱
步骤 | 蘸有稀硫酸 实验装置 | 实验操作及现象 | 解释与结论 |
1 |
| 从a管通入NH3,一段时间后,从b管通入CO2,溶液中有固体析出 | (1)蘸有稀硫酸的棉花的作用是_____ (2)通NH3的a管若伸到液面下,会造成的后果是_____ |
2 |
| 加热,导管口有气泡,澄清石灰水变浑浊 | 步骤1析出的固体是碳酸氢钠 |
3 |
| 滴加足量稀盐酸,有气泡产生,固体逐渐消失 | 步骤2加热后得到的固体是纯碱 |
(实验反思)同学们认为步骤3的结论存在不足.依据题中信息,设计实验确定步骤2加热后得到的固体成分,其方案是_____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com