
分析 根据金属是否容易生锈考虑本题;由赤铁矿石的质量、氧化铁的质量分数、生铁中杂质的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量;
根据题意提供信息,遵循质量守恒定律分析题意写出相关的化学方程式,根据铁元素的化合价+2、+3价写出生成物的两种金属氯化物的化学式,然后再根据式子两边各元素的原子个数相等配平方程式.
解答 解:金属活动性越强,越容易生锈,由“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜锈;铁器则锈迹斑斑,残存很少,可知铁最活泼,铜次之,金最不活泼.所以,三种金属的活动顺序由强到弱的顺序是 铁>铜>金;
设理论上可炼得含杂质10%的生铁的质量为x
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
20t×80% x(1-10%)
$\frac{160}{112}=\frac{20t×80%}{x(1-10%)}$
x=12.44t
由题意可知,Fe3O4与盐酸发生反应,生成氯化亚铁、氯化铁和水,该反应的化学方程式为Fe3O4+8HCl=FeCl2+2FeCl3+4H2O.
故填:金属活动性:铁>铜>金.金很不活泼,很难腐蚀;铁较活泼,易腐蚀;12.44;Fe3O4+8HCl=FeCl2+2FeCl3+4H2O.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实 验 | 1 | 2 | 3 | 4 |
| 加入样品质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②③ | B. | ①② | C. | ①⑤ | D. | ④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
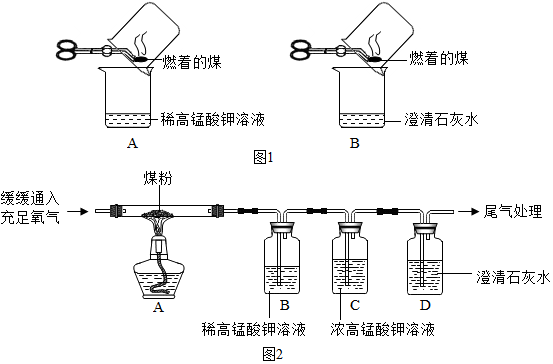
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
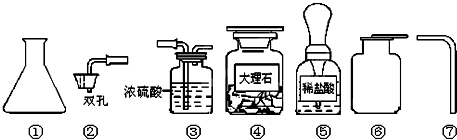
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用带火星的木条 | B. | 分别称取各自的质量 | ||
| C. | 倒入澄清的石灰水 | D. | 用燃着的木条 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
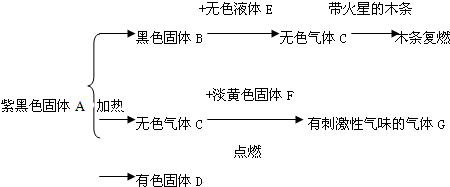
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com