
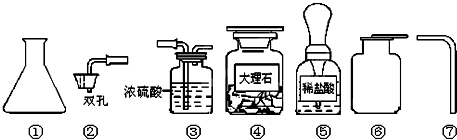
分析 本题从实验室制取制二氧化碳的反应原理,制取装置,收集方法等来解答.选择的仪器要满足实验要求,选择的药品要利于反应发生,制取二氧化碳一般用石灰石和稀盐酸,这样反应的速度比较适中,制取的气体中氯化氢气体也比较少,不用稀硫酸是因为生成的硫酸钙微溶与水,会覆盖在碳酸钙表面,阻止反应进行.通过控制变量的对比实验,可以得出影响反应速度的因素是反应物的浓度和反应物的接触面积.
解答 解:(1)因为制取二氧化碳气体用的是双孔橡皮塞,他们还必须向实验老师领取的仪器是 长颈漏斗或分液漏斗
(2)实验室制取CO2时发生反应的化学方程式为 2HCl+CaCO3=CaCl2+H2O+CO2↑.
(3)因为二氧化碳密度大,收集CO2时,检满的方法是 把燃着的火柴平放到集气瓶口,火柴若熄灭,证明已收集满二氧化碳;
(4)实验室制取大量CO2气体不能用浓盐酸和大理石为原料,因为 浓盐酸易挥发出氯化氢气体,会使收集的CO2不纯;也不能用稀硫酸和大理石为原料,因为 稀硫酸和大理石反应生成CaSO4微溶于水,会阻碍反应的继续进行.
(5)通过对比实验,可得出结论:影响大理石和盐酸反应产生CO2快慢的因素有 大理石与盐酸的接触面积和盐酸的溶质质量分数.
答案:(1)长颈漏斗或分液漏斗
(2)2HCl+CaCO3=CaCl2+H2O+CO2↑
(3)把燃着的火柴平放到集气瓶口,火柴若熄灭,证明已收集满二氧化碳
(4)浓盐酸易挥发,会使收集的CO2因含有氯化氢气体而不纯.稀硫酸和大理石反应生成的CaSO4微溶于水,会阻碍反应的继续进行.
(5)大理石与盐酸的接触面积和盐酸的溶质质量分数
点评 本题综合考查了二氧化碳的实验室制法,并进一步探究了反应原理,提高了同学们对实验室制取二氧化碳的认识.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
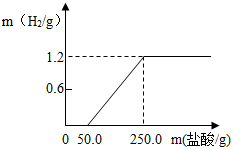 某兴趣小组从废铝锅底部剪一块铝片,将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如图(假设酸与氧化膜反应时没有H2产生,其它杂质不与酸反应).请回答:
某兴趣小组从废铝锅底部剪一块铝片,将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如图(假设酸与氧化膜反应时没有H2产生,其它杂质不与酸反应).请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
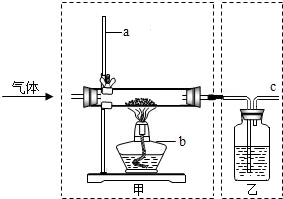 利用如图所示的装置,可进行气体性质的探究实验.甲的玻璃管中盛放黑色粉末(CuO或C),乙的洗气瓶中盛放无色溶液[澄清石灰水或NaOH溶液,NaOH的化学性质与Ca(OH)2相似,均能与CO2反应].
利用如图所示的装置,可进行气体性质的探究实验.甲的玻璃管中盛放黑色粉末(CuO或C),乙的洗气瓶中盛放无色溶液[澄清石灰水或NaOH溶液,NaOH的化学性质与Ca(OH)2相似,均能与CO2反应].| 实验内容 | 甲 | 乙 |
| 实验一 探究CO与CuO的反应 | 反应的化学方程式为: CO+CuO $\frac{\underline{\;\;△\;\;}}{\;}$CO2+Cu | 澄清石灰水的作用是: 检验是否有CO2气体产生 |
| 实验二(b换成酒精喷灯) 探究CO2与C的反应 | 反应的化学方程式为: CO2+C $\frac{\underline{\;高温\;}}{\;}$2CO | NaOH溶液的作用是: 除去(或吸收)CO2气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| X盐溶液 | Y盐溶液 | Z盐溶液 | |
| Ni | 无 | 无 | 有 |
| Mn | 无 | 有 | 有 |
| A. | X Mn Y Ni Z | B. | Z Ni Y Mn X | ||
| C. | Z Mn Y Ni X | D. | X Mn Ni Y Z |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KClO3 氯酸钾 WO3 三氧化钨 O3 氧气 | |
| B. | KMnO4 锰酸钾 H2O 水 S 硫 | |
| C. | CuSO4 硫酸铜 Al2O3 氧化铝 He 氦气 | |
| D. | CaNO3 硝酸钙 FeO 氧化亚铁 H2 氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com