
����Ŀ��ij��ѧ��ȤС���ڹ����ᡢ��λ�ѧ����ʱ��������Щʵ�����۲쵽����������Ҫ���иĽ������ʵ����֤��
����ȤС��С��ͬѧ������ᡢ���к�û���������������������ʵ�飺
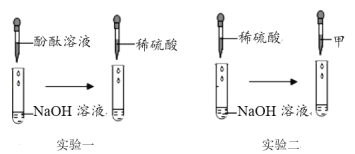
��1��ʵ��һ����NaOH��Һ���ȵ��뼸�η�̪��Һ�����ٵ���ϡ���ᣬ�۲쵽��Һ��____ɫ��Ϊ��ɫ��˵��������ܷ�����Ӧ���������Թ�������ε������NaOH��Һ������������۲쵽____________________________��֤���˵μӵ�ϡ���������
��2�����ա�֤����Ӧ��NaOH��ʧ�ˡ�����Ƕȣ���ͬѧ�������ʵ�������������ϡ�������NaOH��Һ���ٵ������Һ��ͬ��֤������ͼ��ܷ�����Ӧ������Һ������________��ָʾ�����⣩��
��3������ͬѧ�����Ĺ۵�������ɣ������������ᡢ���кͷ�Ӧ��û��������������ϡ������___________��Ӧ�Ϳɹ۲쵽���Ե�����
����ȤС��С��ͬѧ�����CO2ͨ��NaOH��Һ��Ҳ�����������������ʵ��������̽����
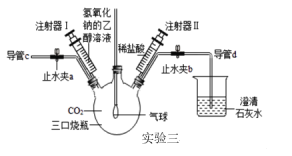
��װ�������Ӻã����������ã�ֹˮ��a��b�ѹرգ�������������ȥ��
[��������]
��CO2���Ҵ�����Ӧ����ʵ��������CO2���Ҵ��е��ܽ���Բ��ơ�
�ڳ�����NaOH�������Ҵ���Na2CO3�����Ҵ���
��4����ע���������������Ƶ��Ҵ���Һע�����CO2��������ƿ�У��������۲쵽��������_________________��д���÷�Ӧ�Ļ�ѧ����ʽ_______________________________________��
��5���ѵ���d�Ƴ�ʯ��ˮ����ֹˮ��a��b���ٴӵ���c����������ƿ�й���N2��Ŀ����_________________________������һ��ʱ����Ȱѵ���d�������ʯ��ˮ�У����Źر�ֹˮ��a���ٰ�ע�������е�ϡ����ע��������ƿ�ڣ��۲쵽������ƿ�в������ݣ�_____________����������Ƕ���֤��CO2��NaOH��Һ�����˷�Ӧ��
������ʦ��ָ���£�����ȤС�������ͬѧ������CO2����ͨ��һ��Ũ��һ������NaOH��Һ�У������ֻ�ʵ�鼼���ƶ���Ӧ��������Һ��pH���¶ȱ仯�������ͼ1��ͼ2��ʾ��
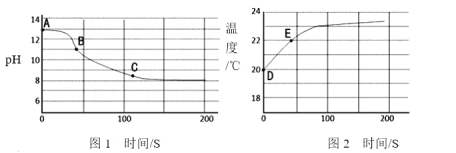
[��������] ��ʵ�������£�Na2CO3��Һ��NaHCO3��Һ��pH�ֱ�ԼΪ11.0��8.5��
��6��ͼ1�У�BC�η�����Ӧ�Ļ�ѧ����ʽΪ__________________________________________��ͼ2�У�DE���¶ȱ仯��ԭ����________________________________________________��
[��˼����]
��7����������������ķ�Ӧ��С��ͬѧһ����Ϊ����ͨ����Ӧ��ļ��ٻ�������������Լ�_________�仯�ȽǶ���֤��Ӧ�ķ�����������ͨ���ִ������ֶν������ݲⶨ��ʵ�ַ�Ӧ���̵ġ����ӻ�����
���𰸡��� ��һ�������Һ�ű�ɺ�ɫ ����ͭ �������� ���ɰ�ɫ������������� 2NaOH+CO2=Na2CO3 +H2O �ų�װ���ڵĶ�����̼ �ձ��еij���ʯ��ˮ����� Na2CO3+CO2+H2O=2NaHCO3 ������̼������������Һ��Ӧ�ų����� ����
��������
��1��NaOH��Һ�Լ��ԣ���̪��Һ��������Һ��졢�����Ի�������Һ����ɫ����NaOH��Һ���ȵ��뼸�η�̪��Һ�����ٵ���ϡ���ᣬ�۲쵽��Һ�ɺ�ɫ��Ϊ��ɫ��˵��������ܷ�����Ӧ���������Թ�������ε������NaOH��Һ������������۲쵽һ��ʱ�����Һ�ű�ɺ�ɫ��֤���μӵ�ϡ���������
��2��������֤����Ӧ��NaOH��ʧ��������Ƕȣ���ͬѧ�������ʵ�������������ϡ�������NaOH��Һ������Ӧ��2NaOH+H2SO4=Na2SO4+2H2O ���ٵ�������ͭ�����Ȼ�þ���Ȼ����ȣ���Һ��û�в�����ɫ������ͭ��������ɫ������þ���������ɫ����������������ͬ��֤������ͼ��ܷ�����Ӧ���ʼ���Һ����������ͭ��
��3������ͬѧ�����Ĺ۵�������ɣ������������ᡢ���кͷ�Ӧ��û��������������ϡ����������������Һ��Ӧ�Ϳɹ۲쵽������ɫ�������Ե�����
��4����ע���������������Ƶ��Ҵ���Һע�����CO2��������ƿ�У�������������̼���������Ʒ�Ӧ����̼���ƺ�ˮ��װ����ѹǿ��С��������̼�����ھƾ����ܣ��ʹ۲쵽�������Dz�����ɫ������������÷�Ӧ�Ļ�ѧ����ʽΪ��2NaOH +CO2=Na2CO3 +H2O��
��5���ѵ���d�Ƴ�ʯ��ˮ����ֹˮ��a��b���ٴӵ���c����������ƿ�й���N2��Ŀ�����ų�װ���ڵĶ�����̼������һ��ʱ����Ȱѵ���d�������ʯ��ˮ�У����Źر�ֹˮ��a���ٰ�ע�������е�ϡ����ע��������ƿ�ڣ��۲쵽������ƿ�в������ݣ�����ʯ��ˮ����ǣ���������Ƕ���֤��CO2��NaOH��Һ�����˷�Ӧ��
��6����֪��Na2CO3��Һ��NaHCO3��Һ��pH�ֱ�ԼΪ11.0��8.5��ͼ1�У�BC��pH��11��С��8.5�����Է�������̼���ƺͶ�����̼��ˮ��Ӧ����̼�����Ƶķ�Ӧ����ѧ����ʽΪ��Na2CO3+CO2+H2O=2NaHCO3��ͼ2�У�DE���¶ȱ仯��ԭ���Ƕ�����̼������������Һ��Ӧ�ų�������
��7����������������ķ�Ӧ��С��ͬѧһ����Ϊ����ͨ����Ӧ��ļ��ٻ�������������Լ������仯�ȽǶ���֤��Ӧ�ķ�����������ͨ���ִ������ֶν������ݲⶨ��ʵ�ַ�Ӧ���̵������ӻ�����


 ���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�п�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʢ��50g10%Ba��OH��2��Һ���ձ��������μ�ϡ��������������ͼ���������ʾ�ձ����������ı仯�������й����ı仯��������ϡ���������Ĺ�ϵ������ǣ�������
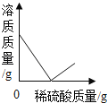
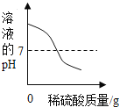
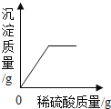
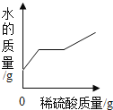
A�� B�� C�� D��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʯ��ʯ����ʯ�ҡ����ᡢ����������Һ������ͭ��Һ��ˮ��þ��������ѡȡ�ʵ�������������з�Ӧ�Ļ�ѧ����ʽ��
(1)�г������ɵĸ��ֽⷴӦ��______��
(2)���������ɵ��û���Ӧ��______��
(3)�кͷ�Ӧ��______��
(4)���Ϸ�Ӧ��______��
(5)�ֽⷴӦ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������л�ѧ���������֡�2������ʾ�����壬�ѷ��������������ں����ϣ�
��Mg2+��CO2 ��2CO����![]() ��2NO3��
��2NO3��
��1����ʾһ������������ɵ���_____��
��2����ʾ���Ӹ�������_____��
��3����ʾһ������������ԭ����Ŀ����_____��
��4����ʾ������ijԪ�صĻ��ϼ۵���_____��
��5����ʾ���Ӹ�������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʳƷ�뽡������Դ�뻷�������ϵ�Ӧ���뷢չ���벻����ѧ��������ѧ֪ʶ�ش��������⣺
![]()
��1������Ӫ���ḻ����������ı������ܡ������и������ۡ�ά����C��ά����B�������ơ����ȡ�
������ġ������ơ�������ָ________������ĸ��ţ���
A ԭ�� B ���� C Ԫ�� D ����
������ȱ�������ᵼ��__________��
���������ܸ������ṩ������������__________��
��2����Դ�뻷���ѳ�Ϊ���������ע�����⡣
�ٻ�ʯȼ�ϰ���_________��ʯ�͡���Ȼ������Ȼ������Ҫ�ɷ���__________��ʯ���ۺ����ô�������������ü�ֵ��ʯ�͵ķ�������___________�仯�����������ѧ������
�ڳ���ʹ�õ綯���г��������ڼ��ٻ�����Ⱦ���綯���г���ʻʱ��ؽ�_______��ת��Ϊ���ܡ�
��3�����ϵ�Ӧ���뷢չ�����ķ��������ǵ����
����������_______������ĸ��ţ���
A �ϳɲ��� B ���ϲ��� C ��������
�ڵ��ں���ë��������Ҫ�����²��ϣ��������ǵķ�����________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���۲����и�ͼ���ش��й����⡣
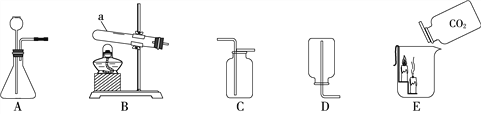
(1)����a��������______��
(2)ʵ������ȡCO2���䷴Ӧԭ�����û�ѧ����ʽ��ʾΪ____________���䷢��װ�ÿ�ѡ����ͼ�е�____(ѡ��װ����ţ���ͬ)���ռ�װ�ÿ�ѡ��____��
(3)ʵ����ʹ�ó���ʯ��ˮ���������̼�ķ�Ӧԭ�����û�ѧ����ʽ��ʾΪ_______________��
(4)�����ռ����Ķ�����̼����ͼE��ʾʵ�飬�۲쵽ȼ�ŵ��������¶�������Ϩ�����ֳ�������̼���ܶȱȿ������______�����ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����кϽ�![]() ������ϡ������ȫ��Ӧ������
������ϡ������ȫ��Ӧ������![]() ����������˵����ȷ����
����������˵����ȷ����![]() ����
����![]()
A. �Ͻ�ΪFe��Al B. �Ͻ�ΪA1��Zn C. �Ͻ�Ϊ���� D. �Ͻ�ΪFe��Zn
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����������Ʒ�к���������̼�������ʡ���ȡ20g��Ʒ���ձ��У�����180gˮʹ����ȫ�ܽ⣬����������μ���ϡ���������������������������������ϡ����������ϵ��ͼ��ʾ����ش��������⣺
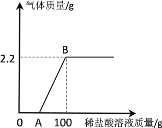
��1����ͼ��0��A�����������˵���������ȸ���Ʒ�е�_____���ѧʽ��������Ӧ��
��2��B��ʱ�����Һ��������Ϊ______ g��
��3������Ʒ���������ƵĴ���______����д��������̣���%��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ᡢ��������������������Ź㷺��Ӧ�á�
��1�������й�˵����ȷ����_____��
A ��ˮ������Ũ�������������
B ���ж����н������Ӻ�����������
C ������pHС��7����ˮ
D Na2CO3��Һ��ʹ��ɫ��̪��Һ���
��2����ѧ�����ǵ�������ϵ���С����Ƹ�����õķ��ͷ۵���Ҫ�ɷ�֮һ������_____������θ�����֢�����ú�����������ҩ�д����Ӧ�Ļ�ѧ����ʽ_____��
��3��С��ͬѧ���кͷ�Ӧ��ʵ��ʱ����ϡ������뵽װ���������ƹ�����Թ��У������Թܱ������ȸУ����������ϵó�������������ϡ���ᷴӦ��ų��������Ľ��ۡ�����С��������飺������һ��������������ϡ���ᷴӦ�ų��ģ�������_____��
��4��NaCl��Һ����������CaCl2��MgSO4���ʣ���ȥ���ʵIJ����ǣ������μ��������Ba��OH��2��Na2CO3��Һ�������ˣ�������Һ�м�������ϡ���ᣬȻ���������ᾧ��
������ʱ��Ҫʹ�ò���������������������ʲô_____��
����д������Ba��OH��2��Һ�����ã��û�ѧ����ʽ��ʾ��_____��
�����˺���Һ�г�NaCl�⣬������ʲô�ɷ�_____��
��5����10g���ֱ��ʵ�����������Ʒ�еμ�73g��ij����ǡ����ȫ��Ӧ�����������ʣ��Һ�������Ϊ80.8g����ԭ����������Ʒ���������Ƶ�����������_____
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com