
【题目】如图是某化肥包装袋上的部分说明:

(1)碳酸氢铵属化学肥料中的______ (填字母)
A.钾肥 B.氮肥 C.磷肥 D.复合肥
(2)碳酸氢铵应具有的性质是______(填字母)
A.易溶于水 B.有挥发性 C.受热易分解
(3)碳酸氢铵与熟石灰反应的方程式为NH4HCO3+Ca(OH)2═CaCO3+2X+NH3↑,则X的化学式是__;施用该类肥料时,要避免与___(填“酸”或“碱”)性物质混用,否则会减低肥效。
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:初中化学 来源: 题型:
【题目】下表为某品牌燕麦片标签中的一部分:
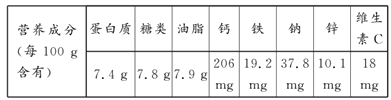
(1)燕麦片中能为人体提供能量的营养素有___________。
(2)燕麦片中含有___种人体所需的微量元素。
(3)人体健康离不开钙元素。下列有关钙元素的叙述中,不正确的是___(填序号)。
①人体中钙元素大部分存在于骨骼和牙齿中
②幼儿及青少年缺钙会得佝偻病和发育不良
③老年人缺钙会引发骨质疏松,容易骨折
④成年人比幼儿和青少年需要摄入更多的钙
(4)钙片的有效成分是碳酸钙,虽然碳酸钙难溶于水,但服用后可转化为可溶性钙盐被人体吸收,其原因是 _________________________(用化学方程式表示)。为了提高补钙效果,服用钙片时常需配合服用维生素D,据此可推知维生素D的功能是________。
(5)现有下列食物:①大米;②豆油;③鱼;④鸡蛋;⑤青菜;⑥西瓜。其中能提供丰富蛋白质的有____(填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
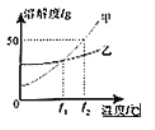
A.t1℃时,甲、乙两物质的溶解度相等
B.乙物质的溶解度大于甲物质的溶解度
C.t2℃时,乙的饱和溶液降温至t1℃,乙溶液变为不饱和溶液
D.t2℃时,甲物质的饱和溶液降温至t1℃,溶液中溶质质量一定不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】北京奥运会火炬、火种被送上海拔8848.43米的珠峰峰顶。象征着光明、和平、友谊、进步、和谐的奥林匹克圣火首次在地球之巅燃起,照亮了每个人的心灵之巅。而“奥运火 航天芯”再次奏响了“科技奥运”的主题。
(1)“祥云”火炬设计有回热管,即用铝箔将铜棒贴在燃料筒外侧,使火炬上下的热量能够交流,这主要是利用了金属铜的___________性。
(2)根据火炬、火种所处的环境不同,各种奥运火炬、火种灯采用的燃料都不相同。
①悉尼奥运会曾使用丁烷(C4H10)作为火炬的燃料,请写出丁烷完全燃烧的化学方程式:__________________________________________ ;
② “高原火种灯”使用的是航空煤油,它主要通过石油分馏获得,分馏属于____________变化(填“化学”或“物理”);
③珠峰火种灯选用了固体碳作燃料,并且完全采用了传统蜂窝煤煤炉的设计,即将固体碳做成碳柱,一节一节填充在容器内进行燃烧,这种设计的优点是:___________;
(3)“祥云”火炬的核心设计是“双火焰”燃烧系统,即使当外部火焰意外熄灭时,内部火焰仍能使其迅速再次燃烧,此过程中,内部火焰的作用是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过联想提出问题是探究的源泉,某合作学习小组开展了如下探究,请你协助他们完成:
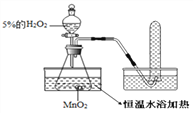
【提出问题】温度越高,分子运动越快;温度越高,化学反应也越快吗?
【实验探究】为了探究温度对H2O2分解反应速率的影响,某实验小组使用如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分数据如表所示:
实验1 | 实验2 | |
MnO2的质量/g | 0.5 | 0.5 |
5%的H2O2的体积 /mL | 40 | X |
恒温水浴加热/℃ | 40 | 80 |
收集一试管氧气所需要时间/ 秒 | 36 | 23 |
(1)实验2中X=____;
(2)在两次实验中,记录不同温度下收集同体积的氧气所需要时间的实验设计目的是______;还可以_______________________ 达到相同的目的,
【实验结论】通过两次实验的实验记录,你可以得出的实验结论是:_________________ ;
【实验拓展】请根据所学再举出一例与温度有关的实验结论:温度越高,_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以电解食盐水为基础制取氯气、氢氧化钠等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。由于粗盐含有少量MgCl 2 、CaCl 2 、Na 2 SO 4等杂质,不符合电解要求,因此必须经过精制。以粗盐为原料的“氯碱工业”流程如下:
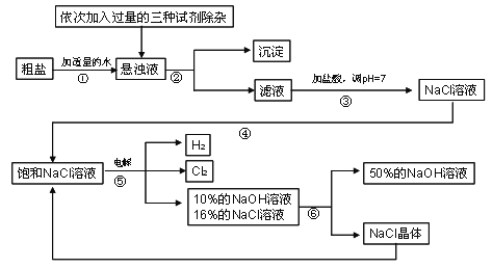
回答下列问题:
(1)氯气、氢氧化钠在工业上有广泛的用途。下列关于氢氧化钠的描述中,错误的是____________。
A.能去除油污,可做厨房清洁剂 B.易溶于水,溶解时放出大量的热
C.水溶液能使石蕊溶液变红 D.可用作某些气体的干燥剂
(2)操作②的名称是______________,操作④的名称是____________。
(3)操作①②间除杂质时所加的三种试剂是NaOH溶液、Na 2 CO 3 溶液、BaCl2 溶液(均过量),其顺序要求是:Na2CO3 溶液必须在BaCl2 溶液之______(填“前”或“后”)加入。有同学提出用______溶液代替BaCl 2 溶液可达到同样的目的。
(4)电解饱和NaCl溶液的化学方程式是__________________。
(5)该流程中可以循环利用的物质是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图判断,下列说法错误的是( )
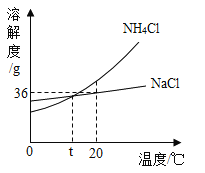
A. NaCl和NH4Cl的溶解度都随温度升高而增大
B. 将20℃时某NH4Cl溶液降温到0℃,其溶质质量分数一定减小
C. 20℃时,20gNaCl加入到50g水中,搅拌后不能全部溶解
D. t℃时,NH4Cl饱和溶液和NaCl饱和溶液溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,以下说法中错误的是

A. 实验开始先通一会儿CO,再用酒精喷灯加热
B. a处固体由黑色逐渐变为红棕色
C. 反应过程中可观察到b处的澄清石灰水变浑浊
D. CO有毒,通常在c处将其点燃或用气囊收集以防止污染空气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸锌可作为食品添加剂。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的FeO、CuO。工艺流程图如下:(假设每一步骤反应均完全)

⑴为提高矿石的溶解速度,操作1是___________ 。
⑵菱锌矿溶解后所得的溶液中金属阳离子有_____________种。
⑶反应1中H2O2转化为H2O,同时有Fe2(SO4)3生成,写出反应1中生成Fe2(SO4)3的化学方程式___________________________。
⑷结晶之前,溶液中除了硫酸锌,还一定存在的溶质是_________________。
⑸硫酸锌晶体的溶解度曲线如下图所示,若要获得ZnSO4·7H2O晶体,应控制结晶时的温度范围为____________________。

⑹流程中还可能得到一种紫罗兰色晶体(NH4)xFey(SO4)z·7H2O。已知该化合物中氮、铁元素质量比为1:4,则x:y :z=________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com