
分析 【分析猜想】根据已有的知识进行分析,硫酸铜的水溶液呈蓝色;
【实验结论】(2)根据题干信息可知,品红溶液褪色说明有二氧化硫生成,根据化学方程式的书写方法和原则来分析解答;
(3)两组实验的区别在反应物中硫酸的浓度不同,因此出现了不同的实验现象;
【拓展延伸】二氧化硫能与氢氧化钠反应生成亚硫酸钠和水,所以可用氢氧化钠溶液来进行吸收.
解答 解:【分析猜想】(1)含有铜离子的溶液颜色是蓝色的,该反应是由浓硫酸与铜发生的反应,且溶液变蓝,说明有硫酸铜生成,故填:CuSO4(硫酸铜);
【实验结论】(2)由题干信息可知,能使品红溶液褪色说明有二氧化硫生成,铜能与浓硫酸在加热时反应生成硫酸铜、二氧化硫和水,故填:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(3)铜不能与稀硫酸反应,可以与浓硫酸反应,说明化学反应与反应物的浓度有关,故填:浓度大小或质量分数大小;
【拓展延伸】二氧化硫能与氢氧化钠反应生成亚硫酸钠和水,故填:SO2+2NaOH═Na2SO3+H2O.
点评 本题为科学探究题,完成此题,可以依据题干提供的信息结合物质的性质进行.


科目:初中化学 来源: 题型:选择题
| A. | 用肥皂水鉴别硬水和软水 | |
| B. | 用灼烧的方法鉴别羊毛和合成纤维 | |
| C. | 用二氧化锰区别水和过氧化氢溶液 | |
| D. | 根据外观和是否溶于水鉴别食盐和白糖 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
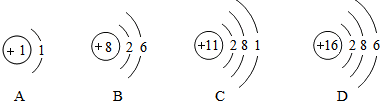
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
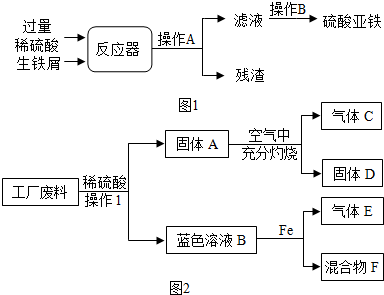
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑥ | C. | ①②④ | D. | ③⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 提出问题,白色固体是什么 | 实验操作 | 实验现象 | 实验结论 |
| 白色固体是氢氧化钙 | 将固体加入足量水中溶解,过滤,在滤液中加入Na2CO3溶液(不能用酸碱指示剂) | 产生白色沉淀 | 猜想成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氮气与二氧化碳-----点燃的木条 | |
| B. | 氧化钙与硝酸铵------加水,测量溶液温度的变化 | |
| C. | 尿素和硫酸铵--------加熟石灰,研磨 | |
| D. | 氧化铜与铁粉---------用磁铁吸引 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com