
| 序号 | 实验操作 | 主要实验现象 | 实验结论及解释 |
| ① | 打开a,关闭b,由长颈漏斗注入稀盐酸 | I.A中产生大量气泡 II.E中出现浑浊 | E中出现浑浊后,再点燃酒精灯的目的是:排出装置中的空气,防止空气的干扰 |
| ② | 当E中出现浑浊时,打开b,关闭a,点燃酒精灯 | I.D中Na剧烈燃烧,产生白烟.内壁附着黑色、白色固体 II.G中产生灰色沉淀 | D试管中的反应产物一定有C和CO |
| ③ | 取反应后D中少量白色固体于另一支试管中,加水溶解,再加入CaCl2稀溶液 | 产生白色沉淀 | D试管中的反应产物还有Na2CO3 |
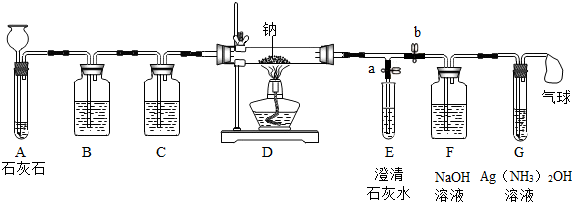
分析 题图所示实验操作过程:石灰石和盐酸制得的二氧化碳气体经过B、C装置净化、干燥后,依次通过D、F、G装置,其中装置E可自由控制二氧化碳的通入与否.
装置的作用:装置B净化吸收混有的氯化氢气体;装置C干燥二氧化碳;装置D中发生钠在二氧化碳气体中的燃烧,可通过点燃灯加热来控制;装置E装有澄清石灰水检验二氧化碳,使用开关a控制;装置F盛有氢氧化钠溶液吸收混合气体中的二氧化碳,使用开关b控制;装置G盛有银氨溶液[Ag(NH3)2OH],检验气体CO的存在;最后用气球进行尾气收集处理.
解答 解:(1)①打开a关闭b,控制二氧化碳气体进入装置E,二氧化碳通入澄清石灰水,生成不溶于水的碳酸钙,石灰水变浑浊.E中出现浑浊,二氧化碳气体通入了装置E,说明了装置内已充满二氧化碳,即装置内的空气全部排出.
故答:排出装置中的空气,防止空气的干扰;
②点燃酒精灯使装置D中的燃烧反应开始发生,打开b关闭a,使燃烧后气体依次通过装置F和G.钠与二氧化碳反应的反应物中仅含钠、碳、氧三种元素,由这三种元素组成的物质中呈黑色的只可能是单质碳,即装置D中生成的黑色固体为单质碳.装置G中氯化钯溶液出现黑色沉淀,结合资料④可知混合气体中含有CO.
故选C和CO;
③钠与二氧化碳反应生成的白色固体物质可能为氧化钠、碳酸钠等,加水溶解并加入石灰水,出现白色沉淀,说明白色固体物质中含有碳酸根,即含有碳酸钠.
故答:Na2CO3;
(2)实验反思
①装置B中NaHCO3饱和溶液可除去混杂在CO2中的HCl,写出该反应的化学方程式:NaHCO3+HCl=NaCl+CO2↑+H2O;故答案为:NaHCO3+HCl=NaCl+CO2↑+H2O;
②C装置中应装浓硫酸,若无装置C,对实验有影响的物质是水;故答案为:水;
③氢氧化钙和二氧化碳反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:Ca(OH)2+CO2═CaCO3↓+H2O.
④[Ag(NH3)2OH]与CO反应,生成灰色沉淀Ag、碳酸铵和氨气,该反应的化学方程式:3Ag(NH3)2OH+CO=3Ag+(NH4)2CO3和4NH3↑.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
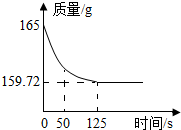 为了测定某种贝壳中碳酸钙的质量分数,取贝壳15克放入烧杯中,然后加入150克7.3%的盐酸溶液,立即将烧杯放在电子秤上称量.反应结束后,测得溶液PH为4.3.记录的烧杯内物质质量随时间的变化图线如下图所示(假设贝壳中其它物质不与盐酸反应).请分析并完成下列问题:
为了测定某种贝壳中碳酸钙的质量分数,取贝壳15克放入烧杯中,然后加入150克7.3%的盐酸溶液,立即将烧杯放在电子秤上称量.反应结束后,测得溶液PH为4.3.记录的烧杯内物质质量随时间的变化图线如下图所示(假设贝壳中其它物质不与盐酸反应).请分析并完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
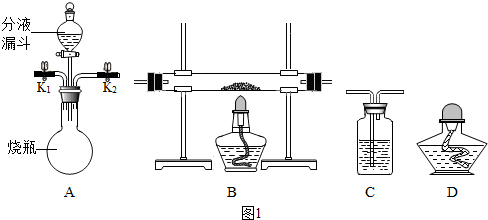
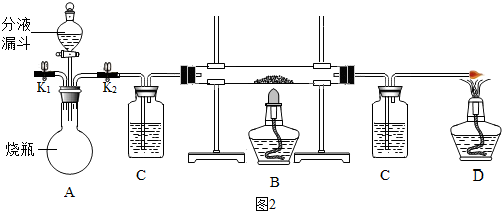
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com