
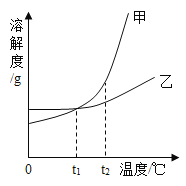
【题目】甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法正确的是( )
A.甲、乙的溶解度相等
B.要从含有少量乙的甲溶液中得到较多的甲,通常可采用蒸发结晶的方法
C.等质量的甲、乙分别配成t2℃时的饱和溶液,需要水的质量:甲小于乙
D.t1℃时,甲、乙的饱和溶液升温到t2℃后,溶质质量分数相等
【答案】CD
【解析】
A、溶解度比较应指明温度,否则无法比较,不符合题意;
B、由图可知,甲、乙的溶解度都随温度的升高而增加,且甲的溶解度受温度的影响较大,乙的溶解度受温度的影响较小,故要从含有少量乙的甲溶液中得到较多的甲,通常可采用降温结晶的方法,不符合题意;
C、由图可知,t2℃时,溶解度:甲>乙,故等质量的甲、乙分别配成t2℃时的饱和溶液,需要水的质量:甲小于乙,符合题意;
D、由图可知,t1℃时,甲、乙的溶解度相等,说明该温度下,甲、乙饱和溶液的溶质质量分数相等,甲、乙的溶解度都随温度的升高而增加,故t1℃时,甲、乙的饱和溶液升温到t2℃后,甲、乙变为不饱和溶液,溶质质量分数不变,故升温后,溶质质量分数相等,符合题意。
故选CD。


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:初中化学 来源: 题型:
【题目】盐酸、氢氧化钠是常见的酸和碱。
(1)盐酸溶液中阳离子符号是_____________,氢氧化钠的俗称是____________(写一种)。
(2)向稀氢氧化钠溶液中滴入酚酞溶液。当滴入稀盐酸至完全中和时,溶液的颜色变化是_________。
(3)根据化学方程式计算,含HCl 7.3g的稀盐酸可中和氢氧化钠的质量为多少________?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】莽草酸(C7H10O5)是从八角中提取的一种化合物,是合成治疗新冠肺炎的药物“奥司他韦”的原料。计算:
(1)莽草酸中共含有 种元素(写数字)。
(2)莽草酸的相对分子质量是 。
(3)莽草酸中氧元素的质量分数为 (结果精确到0.1%)。
(4)若莽草酸中含有4g氧元素,则莽草酸的质量为 g(结果精确到0.1)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以金红石(主要成分是TiO2)为原料生产金属钛的步骤主要有:①在高温下,向金红石与焦炭的混合物中通入氯气(Cl2),得到TiCl4和一种可燃性气体;②在稀有气体环境和加热条件下,用Mg与TiCl4反应得到Ti和MgCl2;下列说法不正确的是( )
A.①中的反应为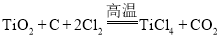
B.反应②中稀有气体的作用是隔绝空气
C.反应①②中钛元素的化合价均发生改变
D.反应②中金属的总质量保持不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下列实验装置,回答有关问题。
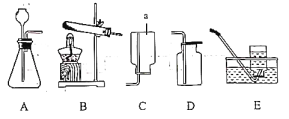
(1)写出图中仪器a的名称:_____。
(2)实验室用加热氯酸钾和二氧化锰的混合物制取并收集氧气,选用的装置为___(填字母),该反应的化学方程式为_____。
(3)实验室用石灰石和稀盐酸反应制取并收集二氧化碳,选用的装置为__(填字母),该反应的化学方程式为___。
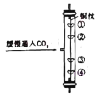
(4)如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球,观察到的现象是④比①先变红,②、③不变红,该实验能说明二氧化碳_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门以实验为基础的自然科学。
(1)活性炭常用于净水,其作用是_____(填序号,下同)、过滤水中的杂质。下列净化水的方法中,净化程度最高的是_____。
A吸附
B过滤
C蒸馏
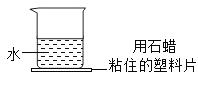
(2)往如图所示的烧杯中加入一种物质,搅拌后,发现塑料片滑落。加入的物质可能是_____或_____(填两种不同类别的物质)。
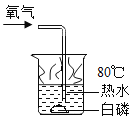
(3)如图所示实验,热水中未燃烧的白磷在通入氧气后燃烧,可得到的实验结论是_____。
(4)有一包“铁”的粉末,可能含有Fe、Fe2O3、Fe3O4中的一种或几种,现称取23.2g放在试管中,通入足量的一氧化碳并加热充分反应,将生成的气体全部通入足量的澄清石灰水,共得到40g碳酸钙固体,关于这包“铁”的粉末成分判断正确的是_____。(填字母)
A一定是纯净物
B一定有Fe、Fe2O3、Fe3O4三种
C如果有Fe,就一定有Fe2O3
D如果有Fe2O3,就一定有Fe2O4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧乙酸(CH3CO3H)是一种光谱高效消毒剂,不稳定,常温下易分解。制备过氧乙酸的化学方程式为: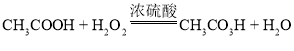 。取质量相等的乙酸(CH3COOH)和50% H2O2溶液均匀混合,再加入适量浓硫酸。一定条件下,测得溶液中过氧乙酸质量分数的数据如图。下列说法不正确的是
。取质量相等的乙酸(CH3COOH)和50% H2O2溶液均匀混合,再加入适量浓硫酸。一定条件下,测得溶液中过氧乙酸质量分数的数据如图。下列说法不正确的是
A.过氧乙酸中C、H元素的质量比为6:1
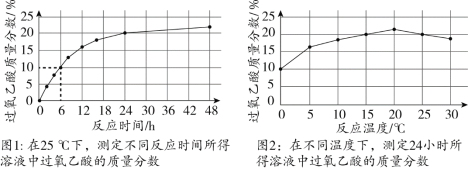
B.图1中,反应时间为6 h时,若溶液总质量为100 g,其中含有10 g过氧乙酸
C.图2中,与20℃相比,25℃时溶液中过氧乙酸质量分数下降的可能原因是温度升高,过氧乙酸分解得更多
D.综合图1和图2分析,制备过氧乙酸的最佳反应时间为24 h,最佳反应温度为25℃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向甲、乙两只烧杯中分别加入 100g 溶质质量分数为 7.3%的稀盐酸,然后取等质量的镁、铝单质,分别放入甲、乙两个烧杯中。充分反应后,发现甲烧杯中单质镁有剩余, 则有关该实验的说法正确的是( )
A.乙烧杯中单质铝一定没有剩余
B.铝剩余的质量一定比镁剩余的少
C.甲、乙烧杯中都产生了 0.2g 氢气
D.反应结束后甲、乙烧杯中物质的质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
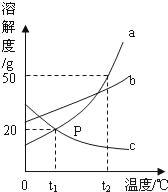
(1)P点的含义是_____;
(2)t2℃时25g a物质加入到50g水中不断搅拌,能形成75g饱和溶液吗?_____(填写“能”或“不能”);
(3)t2℃时,将等质量的a、b、c三种物质分别放入100g水中充分溶解,只得到一杯饱和溶液,则它是_____(填a、b、c)的饱和溶液;
(4)将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是_____(填写选项序号)。
A c>a=b B a=b>c C b>a>c D a>b>c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com