
用氯化钠和碳酸氢铵(NH4HCO3)可制备碳酸氢钠和氯化铵(NH4Cl),该反应可表示为:NaCl+NH4HCO3═NaHCO3+NH4Cl.
20℃时,按上述化学方程式中反应物的质量比,向100g水中加入11.7g NaCl
和15.8g NH4HCO3.请计算:
(1)理论上从溶液中析出晶体的质量为多少g?
(2)反应后所得溶液中溶质NH4Cl的质量分数是多少?(写出计算式即可).
资料:20℃时四种物质的溶解度如下,假设它们同时溶解在水中各自的溶解度不变.
| 物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 |
| 溶解度/g | 36.0 | 21.6 | 37.2 | 9.6 |
理论上从溶液中析出晶体的质量为7.2g;反应后所得溶液中溶质NH4Cl的质量分数是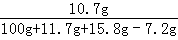 ×100%.
×100%.
解析试题分析:(1)根据化学方程式中质量关系可以知道:NaCl、NH4HCO3恰好完全反应,设生成的NaHCO3的质量为x,NH4Cl的质量为y
NaCl+NH4HCO3═NaHCO3+NH4Cl
58.5 79 84 53.5
11.7g x y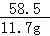 =
=
x=16.8g 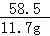 =
=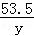
y=10.7g
根据题中的溶解度表可以知道,20℃时100g水中能够溶解碳酸氢钠的质量为9.6g,能够溶解氯化铵的质量为37.2g,所以理论上从溶液中析出的NaHCO3晶体的质量为16.8g﹣9.6g=7.2g;
(2)反应后溶液中溶质NH4Cl的质量分数为: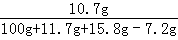 ×100%;
×100%;
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.


科目:初中化学 来源: 题型:计算题
工业上用煅烧石灰石(主要成分为CaCO3)制取生石灰,其生产流程图如下:
(1)某工厂用12t含碳酸钙为75%的石灰石,其中所含碳酸钙的质量是 t.
(2)上述石灰石理论上可以制得生石灰多少t?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某工厂废液中含有氯化钠、氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如下图所示。
回答下列问题:
(1)加入过量A溶解后,再进行操作a时玻璃棒的作用是 。
(2)工厂废液中加入过量A反应的化学方程式为 。
(3)固体乙的主要成分是 。
(4)铁红是炼铁的主要原料,用CO和铁红炼铁的化学方程式为 。
(5)某研究性学习小组的同学为了测定某钢铁厂生铁样品中铁的质量分数,在实验室中
称取生铁样品5.8g放入烧杯中,然后再加入足量的稀硫酸,使之充分反应后,共收
集到0.2g氢气(杂质不参加反应)。则该生铁样品中铁的质量分数为 。(列出计算过程,保留一位小数。)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
化肥的合理使用可以提高农作物的产量,兴化是农业大市,化肥的使用极其普遍。某农业生产公司部分氮肥的销售价格如下:硫酸铵[(NH4)2S04]800元/吨,尿素[CO(NH2)2]2400元/吨。某农民用800元钱去购买氮肥,为了使所购化肥得到的氮最多,你建议他应选购哪种氮肥(请写出计算过程)?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表。
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
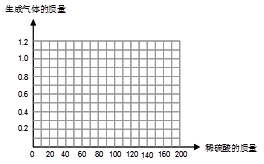
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某同学为了测定实验室中氯酸钾样品的纯度,取2.5g该样品与0.5g二氧化锰混合.加热该混合物t1时间后(杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热t2、t3、t4时间后剩余固体的质量,记录数据如下表:
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 2.12 | 2.08 | 2.04 | 2.04 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
“用微观的眼光看世界”是我们学习化学的重要思想方法,回答下列问题:
(1)稀硫酸和氢氧化钠溶液发生反应的微观过程如图甲所示.从微观角度分析该反应的实质 ;
(2)图乙所示属基本反应类型中的 反应;
(3)图甲中为了准确控制反应的进度,可先向氢氧化钠溶液中加入几滴无色酚酞溶液,当二者恰好完全反应时,溶液的颜色变化是 ,此时溶液中存在的粒子是 ;
(4)40克固态的氢氧化钠配制成溶液后,能与245克稀硫酸恰好完全反应,则稀硫酸的溶质质量分数是 。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
酸和碱发生的中和反应在日常生活和工农业生产中有广泛的应用.小强同学在做中和反应实验时,向盛有40g 10%的氢氧化钠溶液的烧杯中先滴入几滴酚酞,然后逐滴加入稀盐酸,当酚酞刚好由红色变为无色时,共滴加了36.5g稀盐酸.
(1)求稀盐酸中溶质的质量分数;(精确到0.1%,下同)
(2)求反应后所得溶液中溶质的质量分数(滴入酚酞的质量忽略不计).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com