
【题目】已知A~F是初中化学中常见的六种物质,它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“—”表示两种溶液间能发生反应)。又知A、B、D都由两种元素组成,且A、B所含元素各不相同;C、E均含三种元素,其中E常用来改良酸性土壤;F是一种能维持生命活动的单质(通常状况下为气体)。
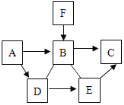
请按要求回答下列问题:
(1) E的化学式为________________。
(2) F的用途___________。
(3) A→D可以通过A分别与____种不同类型的物质反应来实现。
(4)能生成C,且反应物为两种盐的复分解反应的化学方程式为_____________________。
【答案】Ca(OH)2 炼钢、助燃等 三 CaCl2 + Na2CO3 =CaCO3↓ + 2NaCl
【解析】
E常用来改良酸性土壤,所以E为氢氧化钙;F是一种能维持生命活动的单质(通常状况下为气体),所以F为氧气;F(氧气)能转化为B,B由两种元素组成,B能与E(氢氧化钙)反应,B可能为二氧化碳,A能转化为B(二氧化碳),A中含有两种元素,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳, A可能是盐酸;D会转化成E(氢氧化钙),A(盐酸)能转化为D,D能与B(二氧化碳)反应,水与氧化钙反应生成氢氧化钙,水能与二氧化碳反应生成碳酸,所以D是水,B(二氧化碳)和E(氢氧化钙)都能生成C,氢氧化钙与二氧化碳反应生成碳酸钙和水,C可以是碳酸钙,经过验证,推导正确。
根据以上分析可知:
(1)E是氢氧化钙,化学式为Ca(OH)2;
(2)F是氧气,可用作炼钢、助燃等;
(3)A→D是酸转化为水,可以通过A分别与金属氧化物、碱、碳酸盐3种不同类型的物质反应来实现;
(4)能生成C,且反应物为两种盐的复分解反应是氯化钙和碳酸钠反应生成氯化钠和碳酸钙沉淀,化学方程式为:CaCl2+Na2CO3=CaCO3↓+2NaCl。


科目:初中化学 来源: 题型:
【题目】如图是A,B,C三种物质的溶解度曲线,下列说法正确的是( )
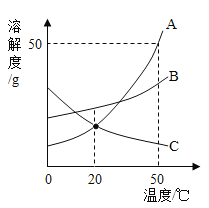
A. 将C的饱和溶液变为不饱和溶液,可采用升温的方法
B. 等质量的A,B溶液降温后,析出晶体的质量一定是A>B
C. t2℃时三种物质的饱和溶液中溶质质量分数的大小关系是A>B>C
D. t2℃时,将50gA放入50g水中,得到A的饱和溶液,其中溶质和溶液的质量比为1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置图,回答问题:
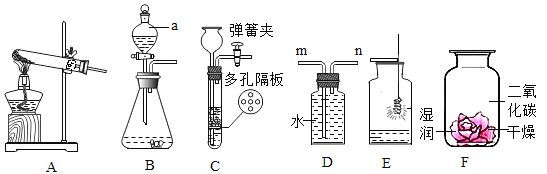
①仪器a的名称是_____。
②用氯酸钾和二氧化锰制取氧气。
(I)反应的化学方程式是______。
(II)用装置 D 收集氧气,则气体应从__________进(填“m”或“n”)。
(III)用装置 E 做“细铁丝在氧气中燃烧”的实验,未看到“剧烈燃烧,火星四射”现象, 可能的原因是_____(答出一条即可)。若实验成功,细铁 丝在氧气中燃烧的化学方程式____。
③用大理石与稀盐酸制取二氧化碳。
(I)发生装置可选用_____(在 A、B、C 中选)。
(II)一般不选用碳酸钠粉末替代大理石,原因是_____。
(III)如图 F 所示,探究二氧化碳与水反应时,将紫色石蕊试液浸泡过的小花,一半烘干放入盛有CO2的集气瓶中,观察到的现象是___________。其中干 燥的纸花要探究的问题是__________。
④欲测定③中稀盐酸的溶质质量分数。取 10g 溶质质量分数为 20%的氢氧化钠溶液,逐滴加入该盐酸,溶液的pH变化如右图所示。求:
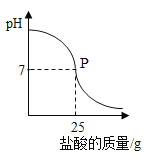
(I)P 点时,消耗氢氧化钠溶液中溶质的物质的量为__________mol。
(II)该稀盐酸的溶质质量分数。_______(根据化学方程式列式计算)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在化学变化中,物质的转化遵循质量守恒定律。一定质量的某物质甲(相对分子质量是90)在氧气中完全燃烧,消耗6.4g氧气,同时生成5.6g一氧化碳、4.4g二氧化碳和5.4g水,则对甲的说法正确的是( )
A.只含有碳、氢两种元素B.一定含有碳、氢元素,可能含有氧元素
C.碳元素质量分数为60%D.若相同质量的甲在9.6g氧气中完全燃烧,则只生成二氧化碳和水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析。
(资料1)草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为H2C2O4·3H2O![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
(问题讨论)用下图所示装置进行实验:
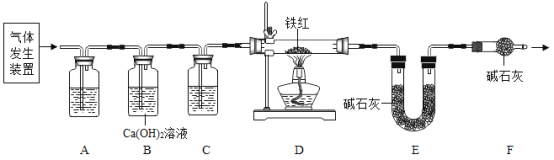
(1)实验前应先检查装置的气密性。
(2)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是_____(填字母编号)。
a 浓硫酸 b 澄清的石灰水 c 氢氧化钠溶液
(3)B装置的作用是________。
(4)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前将装置中的空气排出,防止发生爆炸。
②停止加热后_________。
(5)写出D装置中所发生反应的一个化学方程式____。
(数据分析与计算)
(资料2)铁的常见氧化物中铁的质量分数:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁的质量分数 | 77.8% | 70.0% | 72.4% |
(6)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①D中充分反应后得到Fe粉的质量为mg。
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是_____。
(实验评价)
本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会____(填“偏小”、“不变”或“偏大”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B两种固体(不含结晶水)物质的溶解度曲线,依图回答:
①____℃时,A、B两物质的溶解度相等;
②t1℃时,将A、B各m g分别加到均盛有50g水的两只小烧杯中,充分搅拌后,若其中有一个烧杯中有固体剩余,则该物质是____(填“A”或“B”);
③t3℃时,A物质饱和溶液的溶质的质量分数为____;在不改变溶质质量分数的情况下,将该A的饱和溶液变为不饱和溶液的方法是____;
④烧杯中盛有一定质量、温度为80℃、溶质为A的溶液,将其置于室温环境中,测定不同温度时析出固体A的质量.测定结果记录如下表.
溶液的温度/℃ | 75 | 65 | 50 | 35 | 20 |
析出固体A的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
不考虑水蒸发,则65℃时,该溶液是否为饱和溶液?____(填“是”、“否”或“无法判断”).
⑤根据如图A、B两种固体物质的溶解度曲线,下列说法错误的是____.
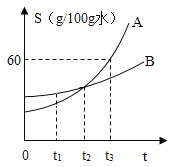
A t2℃时,A、B两物质的溶液中所含的溶质相同
B t2℃时,A、B饱和溶液的溶质质量分数相同
C t3℃时,A、B的饱和溶液降温至t2℃,A 析出的固体比B多
D t3℃时,A、B的饱和溶液降温至t2℃,A、B所含的溶剂质量不变.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是有关气体制取以及性质实验的装置,试回答下列问题:
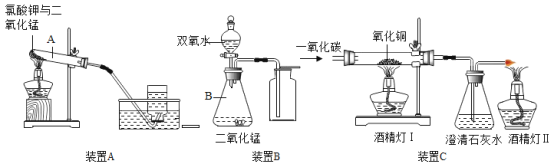
①写出编号仪器的名称:A.___,B___。
②用装置A.制取氧气,写出发生反应的化学方程式__,判断氧气已收集满的方法是__。反应结束时,若未将导管从水中移走就熄灭了酒精灯,可能的后果是___。
③若用B作制取氧气的发生装置,分液漏斗的作用是____。(填入相应字母)
A 便于添加试剂。
B 通过控制滴加试剂的速率,控制双氧水的反应速率。
C 通过控制滴加试剂的速率,使反应能保持较平稳地进行。
④ 写出装置C中一氧化碳和氧化铜反应的化学方程式____。关于装置C的实验,下列说法正确的是____。
A 酒精灯Ⅱ需要在气体纯净后方可点燃。
B 酒精灯Ⅱ的作用是将反应后气体中的一氧化碳点燃,防止有毒气体的排放。
C 实验结束时应先熄灭酒精灯,待冷却到室温后再停止通入一氧化碳。
查看答案和解析>>
科目:初中化学 来源: 题型:
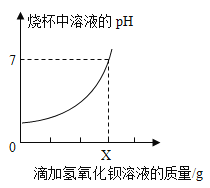
【题目】测定某品牌洁厕灵中硫酸质量。取20g该品牌的洁厕灵溶液于烧杯中,不断滴加25g溶质质量分数为17.1%的氢氧化钡溶液,反应过程中滴入氢氧化钡溶液的质量和烧杯中溶液pH变化的部分数据如下所示:
滴加氢氧化钡溶液的质量/g | 5 | 10 | X | 25 |
烧杯中产生沉淀的质量/g | 1.165 | 2.33 | 4.66 | 4.66 |
求:
①当烧杯中溶液的pH=7时,加入氢氧化钡溶液质量X=______g。
②测得20g该品牌的洁厕灵溶液中硫酸的质量是______g。(根据化学方程式计算)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某沿海工业区排放的污水中含有少量的![]() ,为了达到零污染的目标,将污水,进行如下工业流程处理:
,为了达到零污染的目标,将污水,进行如下工业流程处理:
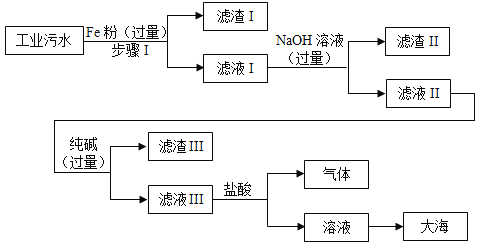
(1)得到滤渣I和滤渣II的操作中所用到的玻璃仪器有玻璃棒、烧杯和______。
(2)加入过量![]() 溶液的目的是______.
溶液的目的是______.
(3)在滤液Ⅲ中加入盐酸使得到的溶液呈中性,要使用______来测定溶液的酸碱度,确保盐酸不过量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com