
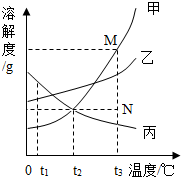
 如图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线.下列叙述错误的是( )| A. | t1℃时,三种物质的溶解度大小顺序为:丙>乙>甲 | |
| B. | t2℃时,甲、丙两种物质的饱和溶液中溶质的质量分数相等 | |
| C. | 若甲物质中混有少量的乙物质,可用蒸发结晶的方法提纯甲 | |
| D. | 若要将组成在N点的甲溶液转变为M点的甲溶液,可以采用恒温蒸发溶剂的方法 |
分析 A、据溶解度曲线可比较同一温度下不同物质的溶解度大小;
B、据饱和溶液中溶质的质量分数计算解答;
C、据溶解度曲线可知物质的溶解度受温度影响情况,进而分析提纯物质的方法;
D、曲线上的点所对应的溶液为此温度下恰好饱和的饱和溶液,而曲线下方的点则为此时的不饱和溶液.根据溶解度受温度的变化情况,可以判断要将组成在N点的A溶液转变为M点的溶液采取的方法.
解答 解:A、由溶解度曲线可知:t1℃时,三种物质的溶解度大小顺序为:丙>乙>甲,正确;
B、饱和溶液中溶质质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%,而t2℃时,甲、丙两种物质的溶解度相等,所以饱和溶液中溶质的质量分数相等,正确;
C、甲物质的溶解度受温度影响较大,乙物质的溶解度受温度影响较小,所以甲物质中混有少量乙物质,可用降温结晶的方法提纯甲,故错误;
D、甲物质的溶解度随温度的升高而增大,所以要将组成在N点的甲溶液转变为M点的甲溶液,可以采用恒温蒸发溶剂或添加溶质的方法,正确;
故选:C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


科目:初中化学 来源: 题型:选择题
| A. | 椒江区设立公共自行车,倡导市民多骑自行车,少开汽车 | |
| B. | 学校推行美术、音乐等书籍循环使用 | |
| C. | 部分学生稍微有点热就开空调、电风扇 | |
| D. | 废纸统一回收再生 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | 实验目的 | 方案 |
| A | 鉴别稀盐酸和稀硫酸 | 取样,滴加紫色石蕊,观察现象 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
| C | 除去CaO中的CaCO3 | 高温加热到固体质量不变 |
| D | 探究Mg、Ag、Cu金属的 活动性顺序 | 将两根光亮的镁条分别伸入 硫酸铜溶液和硝酸银溶液中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
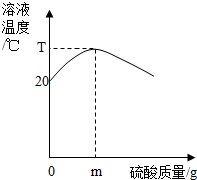 20℃时,在密闭(与外界不发生热交换)容器中,将400g 10%的氢氧化钠溶液和稀硫酸混合,反应过程中溶液温度与硫酸质量关系如图所示.下列说法不正确的是( )
20℃时,在密闭(与外界不发生热交换)容器中,将400g 10%的氢氧化钠溶液和稀硫酸混合,反应过程中溶液温度与硫酸质量关系如图所示.下列说法不正确的是( )| A. | 该反应是放热反应 | |
| B. | 恰好中和时溶液温度达到最高点 | |
| C. | 恰好中和时消耗硫酸的质量是m g | |
| D. | 若用浓硫酸代替稀硫酸,则恰好反应时溶液温度为T℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
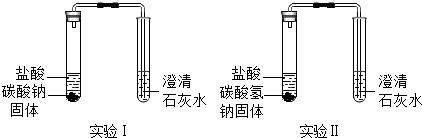
| 实验装置 | 实验现象 | 实验结论 |
| | 实验Ⅰ、Ⅱ中均观察到:白色固体逐渐减少,有气泡冒出;澄清石灰水变浑浊. | Na2CO3和NaHCO3都能与盐酸反应产生CO2;NaHCO3与盐酸反应的化学方程式是NaHCO3+HCl=NaCl+H2O+CO2↑. |
| t1/℃ | t2/℃ | t3/℃ | |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | 甲 | 乙 | 丙 | 丁 | 图例: |
| 化学式 | H2O | C | ? | H2 | |
| 微观示意图 |  |  |  | ? |
 ;
;查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实 验 操 作 | 实 验 现 象 | 结 论 |
| a.取少量样品于试管中,并加入过量的稀硝酸. | 有气泡生成. | 样品中有纯碱. |
| b.再向步骤Ⅰ中所得的溶液加入硝酸银溶液. | 有白色沉淀生成. | 样品中有氯化钠. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com