
【题目】利用下图装置完成实验。

(1)实验甲,粗略测定空气中氧气的含量。能证明氧气约占空气体积![]() 的实验现象是_____。
的实验现象是_____。
(2)实验乙,证明二氧化碳能与氢氧化钠发生反应,实验过程中观察到软塑料瓶变瘪。
①二氧化碳与氢氧化钠反应的化学方程式为_____。
②为了达到实验目的,还需要补做实验,实验操作是_____。
【答案】U型管左侧液面上升到刻度1处 2NaOH+CO2=Na2CO3+H2O 将乙中的氢氧化钠溶液换成等体积的水,重复上述实验(或取反应后溶液滴加足量稀盐酸)
【解析】
(1)实验甲,粗略测定空气中氧气的含量,白磷燃烧消耗氧气,装置被内压强变小,液面上升;能证明氧气约占空气体积![]() 的实验现象是:U型管左侧液面上升到刻度1处,
的实验现象是:U型管左侧液面上升到刻度1处,
(2)实验乙,证明二氧化碳能与氢氧化钠发生反应,实验过程中观察到软塑料瓶变瘪。
①二氧化碳与氢氧化钠反应产生碳酸钠和水的化学方程式为:2NaOH+CO2=Na2CO3+H2O。
②为了达到实验目的,还需要补做实验,需要确定二氧化碳是否溶于水,实验操作是:将乙中的氢氧化钠溶液换成等体积的水,重复上述实验(或取反应后溶液滴加足量稀盐酸)。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:
【题目】用适当的化学符号和数字来表示:
(1)人体中含量最多的金属元素______________;
(2)三个甲烷分子___________________;
(3)标出碳酸中碳元素的化合价____________;
(4)汽车尾气中的污染物之一二氧化氮_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用下列装置进行气体的制取实验,请回答下列问题:
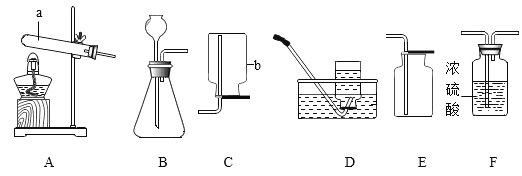
(1)写出标号仪器的名称:a _____________、b ______________。
(2)实验室制取氧气和二氧化碳的发生装置都可选用 B 装置的原因是______________, 如果将长颈漏斗改用分液漏斗的优点是______________。
(3)用B作为发生装置制取氧气,想要得到干燥的氧气,所选择装置的连接顺序为:B→_____→_____(填仪器字母序号)。
(4)实验室用大理石和稀盐酸制取二氧化碳,化学方程式是______________________,验证二氧化碳气体是否集满的方法是_________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】关于如图所示的电解水实验,下列说法正确的是( )
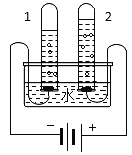
A.试管1中是氧气
B.得出水由氢气和氧气组成的结论
C.试管1和试管2中气体的质量比为2:1
D.用带火星的木条检验试管2中的气体能复燃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】石墨烯是一种由碳原子构成的碳纳米材料,一层层叠起来就是石墨,1mm厚的石墨大约包含300万层石墨烯。实际上石墨烯本来就存在于自然界中,只是难以剥离出单层结构。
石墨烯的制备方法之一是低温扩张法,把石墨粉、钠、液氨按照一定比例混合,在特定装置中进行剥离,然后用去离子水清洗至中性,再放入烘箱内烘干即得石墨烯。制得的石墨烯的比表面积越大,质量越好。科学家测定了烘干温度对制得的石墨烯的比表面积的影响如图所示。

石墨烯具有强度高、透光率高、导电性强、韧性好的特点,是构成其它新型碳材料的基本组成单元,如图所示。将含有石墨烯和碳纳米管两种纳米材料的水溶液低温环境下冻干,去除水分、保留骨架,制造出的一种超轻固体材料被称为“全碳气凝胶”,是迄今为止世界上最轻的材料。“全碳气凝胶”还是吸油能力最强的材料之一,吸收量可高达自身质量的900倍。随着石墨烯制备方法的研发,石墨烯必将广泛应用到各领域中。

依据文章内容回答下列问题。
(1)石墨烯属于______(填“单质”或“化合物”)。
(2)“1mm厚的石墨大约包含300万层石墨烯”,说明构成物质的微粒具有的性质________。
(3)石墨烯可用于制作新能源电池,主要利用石墨烯的________性。
(4)由图1可知:制备石墨烯时最佳的烘干温度是________。
(5)下列说法正确的是________。
A 自然界中不存在石墨烯
B 石墨烯可以制备多种新型碳材料
C 碳纳米管具有可燃性,充分燃烧生成二氧化碳
D “全碳气凝胶”可处理海上石油泄漏
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】84消毒液是生活中常用的一种消毒液,主要成分为次氯酸钠(NaClO)。实验小组对其进行研究。
(查阅资料)
Ⅰ. NaClO溶液呈碱性。
Ⅱ.消毒杀菌的原理是使菌体蛋白质变性,变性程度越大,消毒液消毒杀菌效果越好。鸡蛋清中的蛋白质发生变性反应时变为白色固体物质。
Ⅲ.ORP指84消毒液的漂白能力,ORP数值越大,84消毒液的漂白能力越强。
(进行实验)
实验1:制备84消毒液
某同学制作了一种84消毒液发生器(如图所示),用石墨作电极,电解饱和氯化钠溶液,即可制得消毒液。

实验2:在鸡蛋清中加入不同浓度的消毒液,静置15min现象如下表。
序号 | 2-1 | 2-2 | 2-3 | 2-4 |
实验 操作 |
|
|
|
|
实验现象 | 液体表面产生大量气泡,无其他现象 | 液体中产生大量白色固体 | 液体中产生少量白色固体 | 液体中产生极少量白色固体 |
实验3:探究84消毒液漂白性的影响因素
序号 | 3-1 | 3-2 |
实验操作 | 取烧杯倒入30mL浓度为1:100的84消毒液,将烧杯放置在距离光源 10cm处进行光照,测量ORP变化 | 取四个烧杯,分别倒入30mL浓度为1:100的84消毒液,并置于20°C、30°C、40°C、50°C水浴中加热,测量 ORP变化 |
测量数据 |
|
|
(解释与结论)
(1)实验1中,发生的主要反应如下,补全①的化学方程式。
①2NaCl+2H2O![]() 2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
(2)实验2的目的是_______。
(3)实验3-1的结论是_______。
(4)根据实验3-2的测量数据可知,影响84消毒液漂白性的因素有_________。
(反思与评价)
(5)由实验3可知,84消毒液储存时需注意________。
(6)生活中,84消毒液不能与洁厕灵(主要成分是盐酸)混合使用的原因是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们通过如图实验研究氢氧化钙的性质。
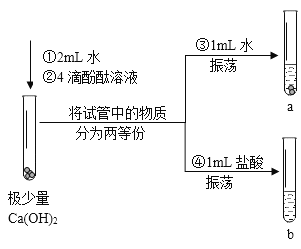
(1)Ca(OH)2属于________(填“酸”、“碱”或“盐”)。
(2)观察到试管a中有固体剩余,加热后固体________(填“消失”或“不消失”)。
(3)观察到试管b中固体消失、红色溶液变为无色,发生反应的化学方程式为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国古代纺织业常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白织物。
(资料)①K2CO3 + Ca(OH)2 = CaCO3↓ + 2KOH
②Ca(OH)2、K2CO3 和 KOH 的部分溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 50 | |
溶解度/g | Ca(OH)2 | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 |
K2CO3 | 107 | 109 | 110 | 114 | 121 | |
KOH | 97 | 103 | 112 | 126 | 140 | |
(1)20℃时,100 g 水中最多可溶解 K2CO3 的质量是__________g,溶质的质量分数为 50% 的 KOH 溶液属于 ___________溶液(填“饱和”或“不饱和”)。
(2)某温度时,向一定量的饱和氢氧化钙溶液中加入少量生石灰,恢复到原温度,某些量随时间变化的关系如图所示。则纵坐标可能表示的是____________(填序号)
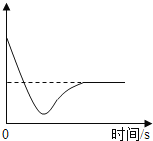
a溶质的质量 b溶质的质量分数 c 氢氧化钙的溶解度 d溶剂的质量 e溶液的质量
(3)20℃时,将 1.38 g K2CO3 固体放入 100 g 水中,并加入一定量的氢氧化钙,搅拌使其充分反应,恢复到原温度,过滤,得到质量为 1.5 g 的固体。所得滤液中的溶质是____________,加入氢氧化钙的质量是_________g。
(4)将纯净的氯化钠配制成溶液。20℃时,向 4 个盛有 200 g 水的烧杯中,分别加入一定质量的氯化钠并充分溶解。4 组实验数据如下:
实验序号 | ① | ② | ③ | ④ |
加入氯化钠的质量/g | 9 | 36 | 81 | 90 |
溶液质量/g | 209 | 236 | 272 | 272 |
若将②中得到的溶液稀释成质量分数为 0.9%的生理盐水,需加水的质量是________g。关于上述实验的叙述正确的是__________(填序号)。
a①②所得溶液是不饱和溶液
b③④所得溶液中,溶质的质量分数相等
c20℃时,200 g 水中最多溶解氯化钠的质量为 72 g
d20℃时,将④继续恒温蒸发 100 g 水,过滤,得到质量为 36 g 的固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类为了维持生命和健康,必须摄取食物以获得营养。
(1)六大基本营养素包括蛋白质、糖类、 、维生素、无机盐和水。
(2)葡萄糖(C6H12O6)中碳、氢、氧三种元素的质量比为 。
(3)葡萄糖中碳元素的质量分数为 。
(4)90g葡萄糖中所含氧元素的质量为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com