
【题目】某化学实验小组对“影响石灰石与盐酸反应速率的因素”进行了如下探究:
(进行实验)
室温下,选用20mL不同浓度的盐酸(4%和6%)分别与1g粉末状或块状的石灰石进行实验(固定夹持仪器略去)。
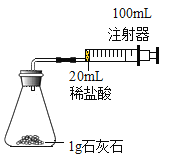
(1)按如图装置进行实验,在装药品前应检查该装置的气密性,具体方法是___________。开始实验时,应将20mL稀盐酸_______________(填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中。
(处理数据)
(2)实验小组进行实验后,获得的相关实验数据如表所示:
实验编号 | 盐酸浓度 (均取20mL) | 石灰石固体形状 (均取1g) | 二氧化碳体积(mL) (均收集前30s的气体) |
a | 4% | 粉末状 | 64 |
b | 4% | 块状 | 40 |
c | 6% | 粉末状 | 98 |
d | 6% | 块状 | 65 |
①要准确比较不同形状的石灰石对反应速率的影响,可采用的方法是____________(写一种);
②从上述实验中得出的结论是颗粒越小,反应的速率越大______________。
(3)如表是实验时记录生成的二氧化碳气体体积和对应的时间的一组实验数据(每间隔4s读数一次):
时间/s | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
气体体积/mL | 16 | 22 | 29 | 39 | 50 | 57 | 62 | 64 | 66 | 66 |
从如表数据可以分析得出,到20s后反应速率逐渐变慢,其主要原因是_____________。
(拓展延伸)
(4)比较不同形状的碳酸钙与稀盐酸反应的速率:利用如图1装置进行实验,同学们倾斜锥形瓶,使试管内的稀盐酸流入瓶中与碳酸钙发生反应,测得瓶内气压随时间的变化如图2所示。
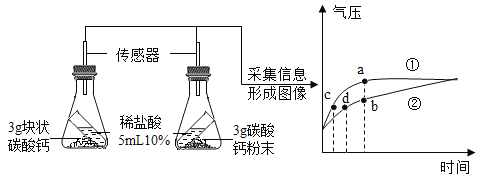
分析图象可知b点溶质______________(填化学式);c、d对比的目的___________________
【答案】将注射器活塞向外拉出一段,松开手一会后,若活塞又回到原位,证明装置气密性良好 快速 ab或cd 相同条件下,碳酸钙颗粒越小,反应的速率越大 随着反应的进行盐酸浓度减小,反应速率逐渐变慢 CaCl2、HCl 对比c、d点可知,相同的气压时,c所需的时间短,说明单位时间内产生的气体多,反应速率快
【解析】
(1)在装药品前应检查该装置的气密性,具体的做法是将将注射器活塞向外拉出一段,松开手一会后,若活塞又回到原位,证明装置气密性良好;开始实验时,因为盐酸和碳酸钙反应生成的二氧化碳会使装置内的压强增大,故应将20ml的稀盐酸快速的推入锥形瓶中,以保证盐酸能全部推入锥形瓶中。
处理数据
(2)①要比较不同形状的石灰石对反应速率的影响,需要盐酸的溶质质量分数相同,石灰石固体的颗粒不相同,比较相同时间内,收集气体体积大小,体积越大,说明反应速率越快,故可选择的实验编号是ab或是cd;
②根据实验编号ab或cd比较,同条件下,当颗粒大小不同时,颗粒越小,反应的速率越大。
(3)从表格数据可以分析得出,开始反应的速率大,后来的反应速率小,主要是因为随着反应的进行,反应物被消耗,浓度减小。
(4)曲线①单位时间内气压大,说明单位时间内产生的气体多,反应速率快,曲线①表示粉末状碳酸钙与稀盐酸反应,曲线②表示块状碳酸钙与稀盐酸反应,最终曲线①、②的气压相等,是因为反应物的量相同,最终产生的二氧化碳质量相等;分析图象可知b点时稀盐酸和碳酸钙已经反应了一段时间,但还未反应结束,故此时的溶质为生成的氯化钙和还未反应的氯化氢(碳酸钙虽剩余但为固体,不存在溶液中);c、d两点的纵坐标相同,横坐标不同,对比c、d点可知,相同的气压时,c所需的时间短,说明单位时间内产生的气体多,反应速率快。


科目:初中化学 来源: 题型:
【题目】已知甲酸(HCOOH)具有挥发性,在热的浓硫酸中分解生成一氧化碳和水。用下图所示实验装置制取CO,然后用CO还原Fe3O4,并检验气体产物。
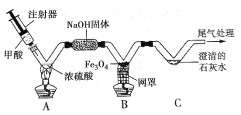
(1)氢氧化钠固体的作用是什么_______?
(2)写出B中Fe3O4发生反应的化学方程式_______。
(3)C中观察到的现象是什么_______?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活密切相关,化学就在我们身边。
(1)下列食物中主要富含蛋白质的是_____(填序号);

(2)生石灰常用作某些食品包装中的干燥剂,它的化学式为_____
(3)野炊后用沙土盖灭火种的主要灭火原理是_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属钼(Mo)可用于制作通信卫星的天线,由钼丝编织而成的天线具有“能屈能伸”的特性。工业上常用辉钼(MoS2)制取纯钼,反应分两步进行,过程如下:

(1)MoO3中钼元素的化合价为_____。
(2)“能屈能伸”说明金属钼具有良好的_____性。
(3)反应①是辉钼(MoS2)与氧气发生的氧化反应,产物是MoO3和一种含硫的氧化物(其中硫元素的化合价为+4),写出该反应的化学方程式:_____。
(4)为了防止反应①产生的硫的氧化物污染环境,可以使用_____吸收废气;反应②体现了H2的_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线,下列说法正确的是
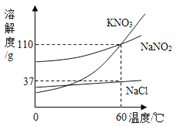
A. KNO3和NaNO2的溶解度相等
B. 60 ℃时,NaCl的饱和溶液的溶质质量分数为37%
C. 将接近饱和的NaNO2溶液变为饱和溶液,可采用降温的方法
D. 除去NaCl中少量KNO3,可在较高温度下制得浓溶液再冷却结晶、过滤、干燥
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
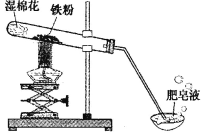
(1)试管尾部放一团湿棉花的目的是_______________。
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。 说明生成的气体是______________。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____________。
【实验探究】
实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为___________________________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是_______________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组用如图所示装置对铁生锈的条件进行了探究。
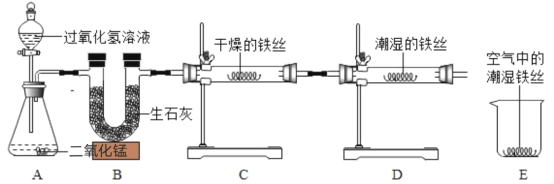
请回答:
(1)A中反应的化学方程式为__________________。
(2)B中生石灰的作用是___________。
(3)4分钟后观察:C处铁丝依然光亮,D处铁丝表面灰暗,E中铁丝依然光亮。对比铁丝表面的变化,能够说明铁生锈与水有关的是一组对比是装置_________(填编号);D、E处实验现象对比说明:决定铁生锈快慢的一个重要因素是____________________。
(4)将装置C、D中的铁丝分别放入盛有等体积相同浓度的稀盐酸的两支试管中,两个试管中现象的不同点是: ________________、__________________(答两点)。
(5)铝与氧气反应可以生成致密的氧化膜,阻止铝与氧气进一步反应,但铁制品确可以全部锈蚀,其原因是_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是木炭与氧化铜反应的实验装置图,下列说法错误的是( )
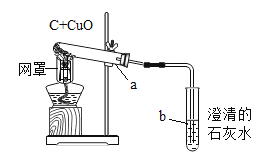
A.给酒精灯加网罩,目的是使火焰集中并提高温度
B.实验过程中,可观察到b中溶液变浑浊
C.为保证氧化铜被完全还原出来,氧化铜与木炭的质量比应该为160:12
D.实验结束后,先从b中移出导管,然后迅速夹紧胶管
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:铝能与氢氧化钠溶液反应,生成偏铝酸钠(NaAlO2) 和氢气;铁、铜不能与氢氧化钠溶液反应。把上述三种金属样品分别编号为X、Y、Z,若把X、Y、Z分别放入稀硫酸中,则X、Y溶解,Z不溶解,另取X、Y分别放入氢氧化钠溶液中,Y溶解,X不溶解,请回答:
(1)写出铝与氢氧化钠溶液反应的化学方程式。______________________________________
(2)Y与硝酸银溶液反应后溶液质量如何变化?______________________________________
(3)描述X与Z的硫酸盐溶液反应的现象。______________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com