
【题目】(8分)常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
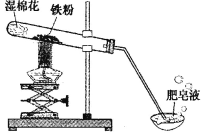
(1)试管尾部放一团湿棉花的目的是_______________。
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。 说明生成的气体是______________。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____________。
【实验探究】
实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为___________________________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是_______________________________。
【答案】 (1)提供水蒸气(2)H2(3)【猜想与假设】猜想二:剩余固体是Fe3O4
【实验探究】
实验操作 | 实验现象及结论 |
取少量黑色固体于试管中,加入足量的稀盐酸。 | 若固体全部溶解,没有气泡冒出,剩余固体是Fe3O4。若固体全部溶解,有气泡冒出,剩余固体是Fe与Fe3O4。 |
【实验结论】3Fe+4H2O高温Fe3O4+4H2↑【反思与交流】Fe2O3红棕色粉末
【解析】
![]() 试题分析: 根据题中的叙述可知(1)试管尾部放一团湿棉花的目的是提供水蒸气;(2)探究生成的气体用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。证明气体的密度较小且有可燃性,说明生成的气体是氢气;(3)探究试管中剩余固体成分【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。根据这一性质,可说明黑色物质是铁粉、四氧化三铁、或二者的混合物,故【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是四氧化三铁;【实验探究】实验操作为 ;取少量黑色固体于试管中,加入足量的稀盐酸。出现固体全部溶解,没有气泡冒出,剩余固体是Fe3O4。若固体全部溶解,有气泡冒出,剩余固体是Fe与Fe3O4。【实验结论】铁和水蒸气反应的化学方程式为3Fe+4H2O====Fe3O4+4H2↑;【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3红棕色粉末。
试题分析: 根据题中的叙述可知(1)试管尾部放一团湿棉花的目的是提供水蒸气;(2)探究生成的气体用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。证明气体的密度较小且有可燃性,说明生成的气体是氢气;(3)探究试管中剩余固体成分【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。根据这一性质,可说明黑色物质是铁粉、四氧化三铁、或二者的混合物,故【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是四氧化三铁;【实验探究】实验操作为 ;取少量黑色固体于试管中,加入足量的稀盐酸。出现固体全部溶解,没有气泡冒出,剩余固体是Fe3O4。若固体全部溶解,有气泡冒出,剩余固体是Fe与Fe3O4。【实验结论】铁和水蒸气反应的化学方程式为3Fe+4H2O====Fe3O4+4H2↑;【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3红棕色粉末。


科目:初中化学 来源: 题型:
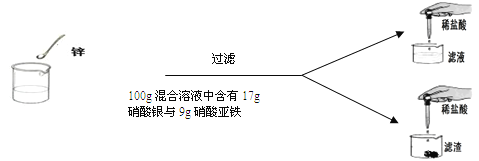
【题目】(7分)学过金属活动性后,秦思同学通过实验探究锌粉与硝酸亚铁和硝酸银两种盐溶液的反应。实验现象和数据如下:
第一次 | 第二次 | 第三次 | 第四次 | |
硝酸亚铁与硝酸银的混合溶液 | 100g | 100g | 100g | 100g |
锌粉 | 2g | 3.25g | m | 9.75g |
向滤液中加入稀盐酸后的实验现象 | 产生白色沉淀 | 无明显现象 | 无明显现象 | 无明显现象 |
向滤渣中加入100 g稀盐酸后的实验现象 | 无明显现象 | 无明显现象 | 产生气泡,溶液变为浅绿色 | 现象与第三次相同 |
(1)第四次向滤渣中加入稀盐酸后产生气泡的化学方程式为 ;
(2)根据第一次的实验现象,你认为此次滤液中的溶质是 ;
(3)根据已知条件列出求解第二次实验中置换出金属银的质量(x)的比例式 ;
(4)若第三次实验锌与两种盐溶液恰好完全反应,则m的质量为__________________;
(5)若向第三次反应后的滤液中加入一定质量的水,所得不饱和溶液中溶质的质量分数为10%,则加入水的质量为__________________;
(6)若用溶质质量分数为36.5%的浓盐酸配制第四次实验中与滤渣恰好完全反应所需的稀盐酸,则需要浓盐酸与水的质量比为_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)水和溶液在生命活动和生产、生活中起着十分重要的作用。
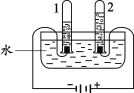
(1)下图实验中,当试管1中气体的体积为6mL时,试管2中气体体积约为 mL;电解时往往要加入少量稀硫酸或氢氧化钠,其作用是 。
(2)农业生产常用溶质的质量分数为10% ~ 20%的NaCl溶液来选种。现将300g 25%的NaCl溶液稀释为10%的NaCl溶液,需要加水的质量为 g。
(3)甲、乙两物质的溶解度曲线如图所示。20℃时,将等质量的甲、乙两种固体,分别加入盛有10 g水
的A、B试管中,充分溶解后,可观察到如图所示的现象。则20℃ t℃(填“>”、“<”或“=”)。
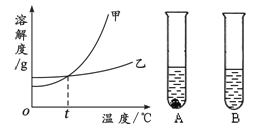
20℃时,对A试管进行如下操作,最终A试管中溶液溶质的质量分数一定发生变化的是 (填字母序号)。
a.加少量水 b.加入少量甲物质
c.升温到40℃ d.蒸发部分溶剂,恢复到20℃
e.加入少量40℃甲的饱和溶液,恢复到20℃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图判断,下列说法错误的是( )。

A.NaCl和NH4Cl的溶解度都随温度升高而增大
B.20 ℃时,20g NaCl加入到50 g水中,搅拌后将全部溶解
C.t ℃时,NH4C1饱和溶液和NaCl饱和溶液中溶质质量分数相等
D.将20 ℃时,某NH4Cl饱和溶液降温到t ℃,其溶质质量分数一定减小了
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图。t1℃时,在两支试管中分别加入等质量的两种物质,再分别加入等量的蒸馏水,充分振荡后,试管底部均有未溶解的固体。再将两支试管升温到t2℃(不考虑溶剂质量变化)。由t1℃到t2℃的过程中,下列说法正确的是

A.甲溶液中溶质的质量分数减小
B.装有乙物质的试管中剩余的固体增多
C.甲、乙两种物质的溶解度都增大
D.两支试管里剩余的固体质量相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用如图所示装置制取氧气,下列实验操作正确的是
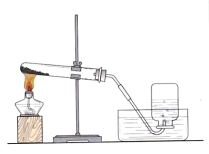
A.加热前,将集气瓶注满水,用玻璃片盖着倒立在盛水的水槽中
B.先将导管口移入集气瓶,再开始加热
C.收集O2后,将集气瓶移出水槽,然后盖上玻璃片
D.停止加热时,先熄灭酒精灯,再移出导气管
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)实验室部分装置如图所示,请回答下列问题。
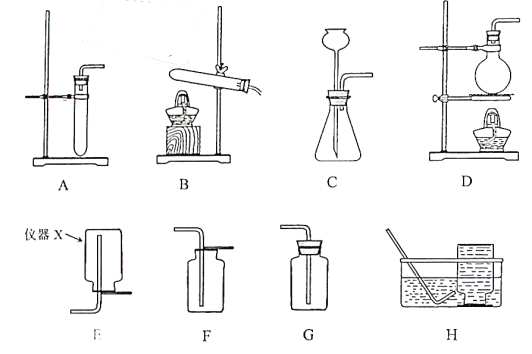
(1)仪器X的名称是 。
(2)实验室用CaCO3和稀盐酸制备CO2的化学方程式为 ,若需制备22g CO2,不计实验损耗,至少需要消耗 g CaCO3。
(3)①用大理石和稀盐酸制取CO2时,能作为发生装置的是 、 (填字母,下同)。
②若要制备多瓶CO2,并在制取过程中便于补充稀盐酸,发生装置应选择 ,收集装置应选择 。
(4)实验室通过加热亚硝酸钠和氯化铵的混合溶液制取并收集N2时,应选择 与
组合而成的装置。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】 0℃时,分别向盛有10g水的A、B两支试管中加入等质量的甲、乙两种固体,充分溶解后,观察到如图1所示的现象.图2表示的甲乙两种物质的溶解度曲线.
(1)20℃时, (填“A”或“B”)试管中的溶液一定是饱和溶液;
(2)图2中 (填“M”或“N”),表示乙物质的溶解度曲线
(3)要使B试管中剩余的固体继续溶解可采用的方法是 (答一种方法即可).
(4)将10℃时M的饱和溶液升温到20℃(假设水不蒸发),其溶质质量分数 (填“增大”、“减小”或“不变”).

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关水(H2O)的说法正确的是( )
A.水由氢元素和氧元素组成
B.水分子由两个氢原子和一个氧原子组成
C.水由氢原子和氧原子组成
D.水分子由一个氧元素和两个氢元素组成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com