
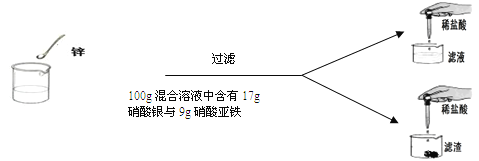
【题目】(7分)学过金属活动性后,秦思同学通过实验探究锌粉与硝酸亚铁和硝酸银两种盐溶液的反应。实验现象和数据如下:
第一次 | 第二次 | 第三次 | 第四次 | |
硝酸亚铁与硝酸银的混合溶液 | 100g | 100g | 100g | 100g |
锌粉 | 2g | 3.25g | m | 9.75g |
向滤液中加入稀盐酸后的实验现象 | 产生白色沉淀 | 无明显现象 | 无明显现象 | 无明显现象 |
向滤渣中加入100 g稀盐酸后的实验现象 | 无明显现象 | 无明显现象 | 产生气泡,溶液变为浅绿色 | 现象与第三次相同 |
(1)第四次向滤渣中加入稀盐酸后产生气泡的化学方程式为 ;
(2)根据第一次的实验现象,你认为此次滤液中的溶质是 ;
(3)根据已知条件列出求解第二次实验中置换出金属银的质量(x)的比例式 ;
(4)若第三次实验锌与两种盐溶液恰好完全反应,则m的质量为__________________;
(5)若向第三次反应后的滤液中加入一定质量的水,所得不饱和溶液中溶质的质量分数为10%,则加入水的质量为__________________;
(6)若用溶质质量分数为36.5%的浓盐酸配制第四次实验中与滤渣恰好完全反应所需的稀盐酸,则需要浓盐酸与水的质量比为_______________。
【答案】(1)Fe +2HCl=== FeCl2 + H2↑ 和Zn +2HCl=== ZnCl2 +H2↑
(2)硝酸银、硝酸锌、硝酸亚铁(或AgNO3、Zn(NO3)2、Fe(NO3)2)
(3)340:216=17g:x (或65:216=3.25g:x) (4)6.5g (5)96.1g (6)1:4
【解析】
试题分析:(1)根据金属的活动性:Zn、Fe、Ag,所以硝酸亚铁和硝酸银两种盐溶液中加入锌粉,发生反应的先后顺序:2AgNO3+Zn== Zn (NO3)2+2Ag,Fe(NO3)2+Zn== Zn (NO3)2+ Fe ,反应发生的程度完全取决于锌的量,根据前三次的实验现象,所以第四次向滤渣中加入稀盐酸后产生气泡的化学方程式为:Fe +2HCl=== FeCl2 + H2↑ 和Zn +2HCl=== ZnCl2 + H2↑
(2) 根据第一次的实验现象,在滤液中加入盐酸,有白色沉淀生成,说明第一个反应:2AgNO3+Zn== Zn (NO3)2+2Ag都没有完全发生,所以滤液中的溶质是:硝酸银、硝酸锌、硝酸亚铁
(3) 根据第二次的实验现象,在滤液中加入盐酸,没有白色沉淀生成,说明溶液中没有AgNO3,而在滤渣中加入盐酸无气体,说明第一个反应恰好反应完全,所以根据方程式:2AgNO3+Zn== Zn (NO3)2+2Ag中AgNO3和Ag的质量关系340:216,所以可列式:340:216=17g:x,也可以根据方程式中Zn和Ag的质量关系65:216,所以可列式:65:216=3.25g:x,
(4) 因为第二次实验表明AgNO3恰好完全,若第三次实验锌与两种盐溶液恰好完全反应,则表明第三次实验就是锌与9g硝酸亚铁反应,根据方程式:Fe(NO3)2+Zn== Zn (NO3)2+ Fe中Fe(NO3)2和Zn的质量关系180:65,而硝酸亚铁为9g,所以消耗Zn的质量为3.25g,故m的质量为=3.25g+3.25g=6.5g
(5)根据上面的分析第三次实验恰好2个反应完全发生,得到的是Zn (NO3)2溶液,反应消耗Zn的质量为6.5g,Zn (NO3)2得到的质量=6.5g÷65/189×100%=18.9g,由于加入的6.5g锌生成铁的的质量为2.8g,生成银的质量为10.8g,所以溶液的质量=100g+6.5g-2.8g-10.8g=92.9g,再抓住稀释过程中溶质的质量不变,可设加入水的质量为x,可列式为:18.9g=(92.9g+x)×10%,x=96.1g
(6)根据上面的分析,第四次滤渣中应含2.8g铁,以及过量的锌质量=9.75g-6.5g=3.25g 再根据反应Fe +2HCl=== FeCl2 + H2↑ 和Zn +2HCl=== ZnCl2 +H2↑,即可算出100g盐酸中所含的氯化氢质量为7.3g,即盐酸的质量分数为7.3g/100g×100%=7.3%,所以若用溶质质量分数为36.5%的浓盐酸配制这样的稀盐酸,需要浓盐酸与水的质量比为1:4


 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案科目:初中化学 来源: 题型:
【题目】(7分)请用所化学知识解释下列原理。
(1)水是生命之源,我们应该了解水、爱护水资源。有些村庄打深井取用地下水,食用前可用 区分地下水是软水还是硬水,常用 的方法来降低水的硬度,以防止结石病的发生。
(2)“釜底抽薪”涉及的化学原理是什么?
(3)有铁,氧化铜,稀硫酸三种物质,请用二种不同的方法制取铜,写出其中的一种方法(用化学方程式): , 。
(4)在检查胃部疾病之前,医生常让病人饮用一种含有硫酸钡的白色牛奶状液体,形象的称作“钡餐”,“钡餐”中的主要物质是硫酸钡,而不能用碳酸钡,其原因可用化学方程式解释为 。
(5)合成材料的应用和发展,大大方便了人类的生活,但是废弃塑料带来的“白色污染”也很严重,为了解决这个问题,我们可以采取的措施有 (答一条即可)。
![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E分别是稀盐酸、氢氧化钙溶液、水、氧化铜和二氧化碳中的一种物质.通常情况下A为固体。右图用圆和方框表示这五种物质,用两圆相切表示两种物质可以发生化学反应.用“→”表示一种物质能转化为另一种物质.请回答下列问题:

⑴在图中标出五种物质的化学式;
⑵B与C反应的化学方程式__________________________________;
⑶A与足量B反应的实验现象为______________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(2分)分类的方法,使化学学习和研究变得有规律。请从原子的结构特点与元素在周期表中的位置的关系的角度,将下列原子结构示意图平均分成两类。
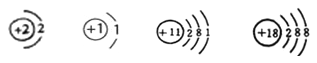
① ② ③ ④
(1) 你选择的原子结构示意图是 (填序号),
(2) 你的一种分类标准是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活中的下列做法违背科学原理的是( )。
A. 用纯碱(碳酸钠)除去面团发酵后产生的酸 B. 用pH试纸测定溶液的酸碱度
C. 用铁桶盛装稀硫酸 D. 用含有氢氧化铝的药物治疗胃酸过多引起的胃病
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)下图是某同学正在绘制的实验室制取二氧化碳的装置图。请回答下列问题:
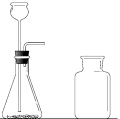
(1)将实验装置图补充完整;
(2)写出用该装置制取二氧化碳的化学方程式_____________;
(3)连接装置后要进行的操作是_________;
(4)检查集气瓶中是否已收集满二氧化碳气体,正确的操作方法是____ ;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组物质的名称、俗称、化学式完全对应的是( )
A.汞 水银 Hg B.氢氧化钠 纯碱 NaOH
C.酒精 甲醇 C2H5OH D.碳酸氢钠 苏打 NaHCO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】 染发时常用到的着色剂——对苯二胺,化学式为C6H8N2,是一种有毒化学药品,有致癌性,下列说法正确的是 ( )
A.对苯二胺中含有N2分子
B.对苯二胺中碳、氢、氮元素的质量比为6:8:2
C.对苯二胺由6个碳原子、8个氢原子和2个氮原子构成
D.对苯二胺中碳元素的质量分数表达式为![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
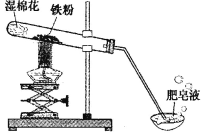
(1)试管尾部放一团湿棉花的目的是_______________。
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。 说明生成的气体是______________。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____________。
【实验探究】
实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为___________________________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com