
【题目】新能源汽车是未来汽车发展的方向之一。下列属于新能源的是____。
A 石油
B 天然气
C 太阳能
D 煤
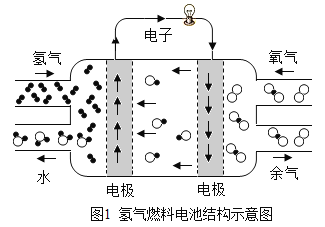
(1)一种新能源汽车以氢气燃料电池为动力,电池结构如图所示。结合图中信息判断,工作过程中,失去电子的物质是____ ,发生反应的总化学方程式为____,通入过量氧气的目的是____。
(2)新能源汽车制造时许多地方都应用铝合金。从铝土矿(主要成分是Al2O3、Fe2O3、 SiO2)中提取金属铝的流程如下:

①铝土矿中不与稀硫酸反应的物质是. ______ 。
②流程中进行“系列操作”的目的是______。
③含Al2O3 50%的铝土矿10.2t,理论上可制得金属铝的质量为______t。
(3)新能源汽车配备的安全气囊中装有“叠氮化钠”(NaN3)等固体粉末。一旦发生强烈碰撞,叠氮化钠迅速发生分解反应生成钠并放出氮气,使安全气囊打开。写出叠氮化钠在撞击条件下分解的化学方程式: ______。
【答案】C H2 ![]() 使氢气充分反应 SiO2 除去铁离子(或分离出氢氧化铝) 2.7
使氢气充分反应 SiO2 除去铁离子(或分离出氢氧化铝) 2.7 
【解析】
煤、石油、天然气属于常规能源,太阳能属于新能源,故选C;
(1)结合图中信息判断,工作过程中,失去电子的物质是H2;氧气和氢气反应生成水,化学方程式为:2H2+O2═2H2O;通入过量氧气的目的是使氢气充分反应;
(2)①Al2O3、Fe2O3都能和稀硫酸反应,SiO2不能和稀硫酸反应;
②要得到纯净的铝就要把其他杂质除去,流程中进行“系列操作”的目的是除去铁离子;
③理论上可制得金属铝的质量为x

x=2.7t
(3)叠氮化钠在撞击条件下分解成钠和氮气,化学方程式为:2NaN3![]() 2Na+3N2↑。
2Na+3N2↑。
故答案为:
C;(1)H2;2H2+O2═2H2O;使氢气充分反应;
(2)①SiO2;②除去铁离子;③2.7;
(3)2NaN3![]() 2Na+3N2↑。
2Na+3N2↑。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:初中化学 来源: 题型:
【题目】化学兴趣小组对“暖宝宝”的发热原理进行探究。
查阅资料:某品牌“暖宝宝”的主要成分为铁粉、水、食盐、活性炭、蛭石、吸水性树脂。食盐对铁粉生锈有催化作用;蛭石是一种优良的保温材料;吸水性树脂具有特强吸水、保水能力,且可反复释水、吸水。
实验探究:小组同学利用图1所示的装置,完成下列表格中的3个实验。测得锥形瓶内温度随时间变化的图像如图2所示。
实验 | 放入锥形瓶中的物质 |
1 | 5 g铁粉、1 g氯化钠 |
2 | 5 g铁粉、1 g氯化钠、1.5 mL水 |
3 | 5 g暖宝宝袋内物质 |

(1)实验1中温度几乎不变的原因是______。
(2)能证明实验2中物质发生反应的依据是_____。
(3)“暖宝宝”中活性炭的作用是_____。
(4)“暖宝宝”发热的原理是:①2Fe+O2+2H2O=2Fe(OH)2;②4Fe(OH)2+O2+2H2O=4Fe(OH)3;③2Fe(OH)3=Fe2O3+3H2O打开使用后的“暖宝宝”可观察到固体为红棕色,则该物质可能是___。
(5)将温度传感器改为湿度传感器,重复实验3,得到的数据如图所示。造成湿度逐渐增大的原因可能与“暖宝宝”中有关的成分是__。

(6)从能量转化角度,“暖宝宝”发热的实质是将____能转化为___能。
(7)“暖宝宝”贮存与使用时应注意的事项是____(写1种)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应。下图是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题:

(1)步骤①中发生的是_____变化(填“物理”或“化学”)。
(2)写出步骤③中发生反应的化学方程式_____。该反应开始后,停止加热反应仍持续进行,原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像与所对应操作相符的是
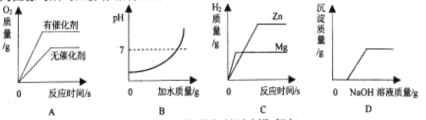
A.用两份等质量、等质量分数的过氧化氢溶液制取氧气
B.向一定质量分数的盐酸中不断加水
C.向等质量的锌片、镁片中分别加入足量的等质量分数的稀硫酸
D.向一定质量的氯化铜和稀盐酸的混合溶液中不断加NaOH溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】室温下,甲、乙、两三种固体分别溶于两支试管和一个烧杯的水中,现象图1所示,甲、丙还有剩余固体,乙固体全部溶解。升温到80°C时,发现甲固体全部溶解,乙固体析出, 丙固体没有明显变化。下列说法正确的是

A.甲溶液可能是不饱和溶液
B.表示乙物质的溶解度曲线是a
C.小于t1°C时丙物质的溶解度最大
D.将t2°C时甲、乙的饱和溶液降温至t1°C,所得溶液的溶质质量分数大小为甲=乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下表中氯化钠和碳酸钠在不同温度时的溶解度,判断下列说法不正确的是
温度/°C | 10 | 20 | 30 | 40 | |
溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
A.氯化钠的溶解度曲线和碳酸钠的溶解度曲线交点温度在20℃~30℃之间
B.20℃时,在50g的水中加入12.2 g碳酸钠,充分搅拌后得到的是饱和溶液
C.20℃时,无法配制溶质质量分数超过26.5%的氯化钠溶液
D.氯化钠中混有少量碳酸钠,可以采用降温结晶的方法除去碳酸钠
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学校化学兴趣小组设计如图所示实验探究燃烧的条件(生石灰是氧化钙的俗称)
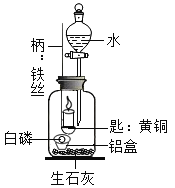
(1)实验用品中使用到的金属材料有_______(填一种即可)
(2)写出一个能证明铝的活动性比铁强的化学反应方程式:___________________。
(3)取一小块白磷放在一铝制的小盒中,然后放入装有生石灰的集气瓶内,点燃蜡烛,塞紧胶塞, 燃烧的蜡烛一会儿就熄灭了.蜡烛燃烧需满足的条件:①温度达到着火点;②______________________。
(4)待冷却后,打开分液漏斗活塞,向集气瓶中注入少量的水,立即关闭活塞,铝盒中的白磷燃烧,在该实验中,生石灰的主要作用是________________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】加热一定量的高锰酸钾固体,某变量y随时间的变化趋势如图所示。则纵坐标y表示的是( )
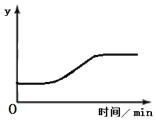
A. 生成氧气的质量
B. 固体中锰元素的质量
C. 固体中钾元素的质量分数
D. 固体中氧元素的质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水壶长时间使用后壶底会有白色固体附着,俗称水垢,某化学兴趣小组的同学设计实验研究水垢的成分,请你和他们一起探究。
[查阅资料]硬水中含有较多的可溶性的钙镁化合物,如Ca(HCO3)2、Mg(HCO3)2。它受热易分解,生成难溶性的化合物、气体等物质,造成水垢。

[提出问题]水垢的中含有碳酸钙吗?
[实验设计]小组同学设计了如图所示的实验装置,充分反应至不再有气泡产生为止,观察到A处试管中有白色固体残留,B处浓硫酸的质量增大,C处澄清石灰水变浑浊。装置中氢氧化钠溶液的作用是_____。
(1)小明同学认为一定有CO2、_____(填化学式)生成。小红从反应物的元素的组成分析,认为气体还可能有氧气或氢气,请你用设计一个简单实验帮助她判断_____。
(2)小明认为该白色固体是碳酸钙,请你帮他完成实验探究,填写下表:
实验步骤 | 实验现象 | 结论 |
_____ | _____ | 难溶物是CaCO3 |
[小结]水垢的中含有碳酸钙。
[实验反思]小明同学查阅资料得知硬水中的另一种可溶性物质碳酸氢镁的性质和碳酸氢钙相似,也会发生上述反应,请写出碳酸氢镁受热分解的反应方程式____。
(3)小明取50g水垢与稀盐酸反应,得出了图中的数据,通过计算可知:水垢中一定含有(填化学式)_____,理由是_____。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com