
【题目】(实验回顾)在烧杯中加入约 5mL 稀氢氧化钠溶液,滴入几滴酚酞溶液。用滴 管慢慢滴入稀盐酸,并不断搅拌。
(1)该实验证明了盐酸和 NaOH 溶液能发生化学反应,依据的现象是_____。
(2)反应的化学方程式为_____。
(探究活动 1)通过证明有水生成来证明酸和碱之间反应的发生。
(查阅资料)a.变色硅胶吸水后由蓝色变为红色;b.无水醋酸是一种酸,常温下为无色液体。
(设计实验)取变色硅胶、无水醋酸和氢氧化钠固体进行如图 1 所示的实验。
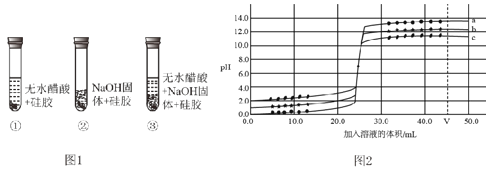
(1)加入试剂后,要迅速塞紧橡胶塞的原因是 _____。
(2)上述实验中能证明酸和碱反应有水生成的现象是_____。
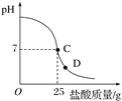
(探究活动 2)通过 pH 变化来证明酸和碱之间反应的发生。图 2 为三种不同浓度的氢氧化 钠溶液与对应浓度盐酸反应的曲线。
(1)该实验是_____(填字母)。
A 将盐酸加入氢氧化钠溶液中 B 将氢氧化钠溶液加入盐酸中
(2)三条曲线所示实验中,所用盐酸浓度最大的是_____(填“a”、“b”或“c”)。
(3)加入溶液体积为 VmL 时,所得溶液中溶质是_____(写化学式)。
(拓展延伸)某同学查阅资料得知常温下 pH 与溶液中 H+浓度有如下关系:
H+浓度(单位略) | 0.1 | 0.01 | 0.001 | 0.0001 | … |
pH | 1 | 2 | 3 | 4 | … |
(1)pH=6 时溶液中 H+的浓度为_____。
(2)下列说法正确的是_____(填字母)。
A H+浓度越大,pH 越小
B pH=1 的盐酸与 pH=3 的盐酸混合后,所得溶液 pH 为 2
C 测定盐酸的 pH 时,先将 pH 试纸用水润湿,再将待测液滴在 pH 试纸上
D 向两份相同的稀盐酸中分别加等体积的水和氢氧化钠溶液,溶液 pH 增大程度相同
(3)推测将 pH=5 的盐酸加水稀释至 1000 倍时,溶液的 pH_____(填字母)。
A 等于 6 B 等于 7 C 等于 8 D 以上都不对
【答案】溶液由红色变为无色(或溶液红色褪去) NaOH+HCl===NaCl+H2O 防止空气中的水和二氧化碳进入试管干扰实验 试管①②无明显变化,试管③中硅胶由蓝色变为红色 B a NaCl,NaOH 0.000001或1×10-6 A D
【解析】
[实验回顾]能说明恰好完全反应的实验现象是:溶液由红色刚好变成无色;氢氧化钠和盐酸反应生成氯化钠和水,反应的方程式是:NaOH+HCl═NaCl+H2O。
故填:(1)溶液由红色刚好变成无色;(2)NaOH+HCl═NaCl+H2O。
[探究活动1](1)加入试剂后,因为需要证明生成了水,所以要避免空气中的水分的干扰,所以要迅速塞紧橡胶塞;(2)能证明酸和碱反应有水生成的现象是 试管③中的变色硅胶由蓝色变为红色,试管①②中的变色硅胶不变色。
故填:(1)防止空气中的水分进入试管干扰试验;(2)试管③中的变色硅胶由蓝色变为红色,试管①②中的变色硅胶不变色;
[探究活动2]由于实验过程中pH变大,故将氢氧化钠溶液加入盐酸中,氢氧化钠溶液的浓度越大,溶液的pH上升越快,故所用氢氧化钠浓度最大的是a,加入溶液体积为VmL时,所得溶液呈碱性,其中溶质是氢氧化钠和氯化钠,
故填:(1)B;(2)a;(3)NaOH、NaCl;
[拓展延伸]由题中信息可知,pH=6时溶液中H的浓度为1×10-6;
A.H+浓度越大,pH越小,故正确;
B.只有pH=1的盐酸与pH=3的盐酸等质量混合时,所得溶液pH为2,故错;
C.测定盐酸的pH时,先将pH试纸用水润湿,会导致溶液的酸碱度发生改变,故错;
D.向两份相同的稀盐酸中分别加等体积的水和氢氧化钠溶液,后者溶液pH增大较多,故错。
故选A。
推测将pH=5的盐酸加水稀释至1000倍时,溶液呈酸性,故pH还小于7,故选D。
故填:(1)1×10-6;(2)A;(3)D。


 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E是初中化学常见的物质,它们相互转化的关系如图所示.

(1)如果A、B均是黑色固体,C是造成温室效应的主要气体,E是气态单质.则C的化学式为_____.
(2)E的用途可能是_____.
(3)A与B反应的基本类型是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定标有质量分数为32%的盐酸的实际质量分数,小明实验时先在烧杯中加入20 g 40%的氢氧化钠溶液,再逐滴加入该盐酸,测定出加入盐酸的质量与烧杯中溶液pH的关系如图。
(1)所用氢氧化钠溶液中溶质的质量为_____g。
(2)请认真看清上图信息后回答以下问题。
①当滴加盐酸到C点时,所消耗的盐酸中溶质的质量是多少?_____。
②该盐酸的实际质量分数是多少?(保留到0.1%)_____。
③导致盐酸溶液的溶质质量分数改变的原因是_____。
④当滴加盐酸到图像中D点时,烧杯中溶液的溶质是_____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源。
(1)海水制盐。从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加稍过量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发。正确的操作顺序是 (填字母)。加Na2CO3溶液的作用是除去 。
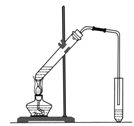
(2)海水淡化。下图是一个简易的蒸馏法淡化海水的装置。证明得到的水是淡水的方法是 。
(3)海水制镁。从海水中提取金属镁的过程如下图所示:
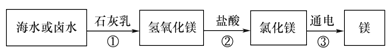
在上述转化过程中发生中和反应的是 (填反应顺序号)。海水中本身就含有氯化镁,则①、②两步的作用是 。
(4)海水“制碱”。氨碱法制纯碱是先通过化学反应生成NaHCO3和NH4Cl,NaHCO3结晶析出,再加热NaHCO3制得纯碱。
①氨碱法制纯碱中生成NaHCO3和NH4Cl的化学方程式为 ;
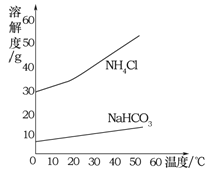
②反应中生成NaHCO3和NH4Cl的质量比为84∶53.5,NaHCO3和NH4Cl的溶解度曲线如图所示。请分析NaHCO3结晶析出而NH4Cl没有结晶析出的原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在密闭容器内进行的某反应,测得反应前(t0)、反应中(t1)、反应后(t2)不同时刻甲、乙、丙、丁四种物质的质量分数分别如下图所示。下列说法不正确的是
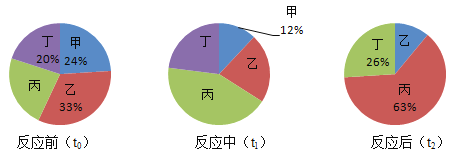
A. 该反应中,甲和乙是反应物,丙和丁是生成物
B. t1时刻,乙、丙、丁所占的质量分数分别为22%、43%和23%
C. 若甲和丁分别是镁和碳,则该反应中甲和丁的化学计量数之比1:2
D. 若反应前四种物质的总质量为100g,如果再增加12g甲,则甲与乙可恰好完全反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、X、Y、Z六种初中常见的物质,甲、乙、丙含有相同的金属元素,甲常作为补钙剂;X的固体常用于人工降雨,Y、Z都显碱性,但不属于同类别物质,Z俗称为纯碱。(“﹣”表示物质之间发生反应,“→”表示物质之间能一步转化)回答下列问题:
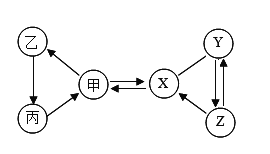
(1)Z的化学式为_____。
(2)写出乙→丙反应的化学方程式:_____,反应类型为_____(填基本反应类型),该反应过程中_____(填“放热”或“吸热”)
(3)①写出X+Y反应的化学方程式:_____。②写出Z→Y的反应的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在学习“酸碱中和反应”时,老师给大家变了一个魔术一使“水”变色的杯子。操作过程及现象如图13所示。
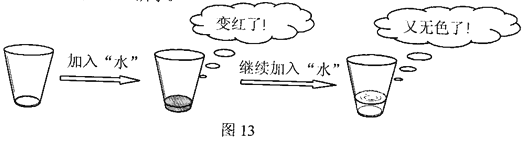
老师揭秘:“空”杯子底部事先涂抹了某种无色液体,无色的“水”是事先用两种无色溶液混合而成。请回答下列问题:
(1)“空”杯内涂抹的物质可能是 溶液。
(2)此过程中发生反应的化学方程式可能是 。
(3)最终溶液为无色,能否说明该溶液一定呈中性? _(选填“能”或“不能”),理由是 __。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图1所示转化关系涉及的物质均为初中化学常见的物质。其中常温下乙的水溶液pH>7,甲、乙、丙均含有元素X,元素X的原子结构示意图如图2所示。图中“→”表示相连两种物质之间的转化关系,“一”表示相连的两种物质可以发生反应,反应条件、部分反应物及生成物已略去。
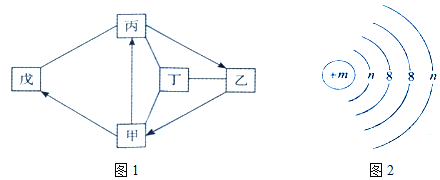
请回答下列问题。
(1)元素X的名称为______。
(2)丙和戊在一定条件下可以发生化合反应,其化学方程式为______。
(3)写出甲与丁反应的化学方程式______。
(4)乙在生产和生活中的用途是______(写一条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,在甲、乙、丙、丁四个盛有100g水的烧杯中,分别放入KNO3固体,充分溶解。下列关于甲、乙、丙、丁所得溶液的说法正确的是( )
温度℃ | t1 | t2 |
KNO3的溶解度(g/100g水) | 60 | 90 |
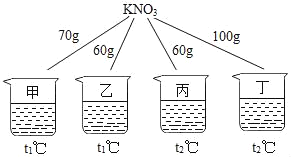
A. 溶液质量:乙=丙<甲<丁
B. 甲、乙、丙、丁均为饱和溶液
C. 将甲升温至t2℃,溶液质量增加
D. 将丁降温至t1℃,没有固体析出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com