
【题目】人类的衣、食、住、行离不开材料和能源。
(1)地球上的金属资源,除少数不活泼的金属外,大部分是以_____形式存在。工业上用赤铁矿(主要成分是 Fe2O3)和一氧化碳炼铁的化学方程式为__________。
(2)汽油是石油分馏的产品之一,汽油中主要含有_____元素,在汽油中加入乙醇作为汽车燃料的主要目的是节约化石燃料和_____,以氢能源为动力的汽车能真正实现“零排放”但氢能源目前还不能广泛使用的原因之一是_____。
【答案】化合物 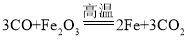 C、H 减少汽车尾气的污染 氢气的制取成本高或贮存困难
C、H 减少汽车尾气的污染 氢气的制取成本高或贮存困难
【解析】
(1)地球上的金属资源,除少数不活泼的金属外,大部分是以化合物形式存在。工业上用赤铁矿(主要成分是 Fe2O3)和一氧化碳炼铁,一氧化碳和三氧化二铁在高温条件下反应生成铁和二氧化碳,反应的化学方程式为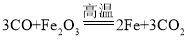 。
。
(2)石油中主要含有碳元素和氢元素两种元素,汽油是石油分馏的产品之一,汽油中主要含有C、H元素;乙醇的化学式为![]() ,完全燃烧生成二氧化碳和水,在汽油中加入乙醇作为汽车燃料的主要目的是节约化石燃料和减少汽车尾气的污染,以氢能源为动力的汽车能真正实现“零排放”但氢能源目前还不能广泛使用的原因是氢气的制取成本高、贮存困难。
,完全燃烧生成二氧化碳和水,在汽油中加入乙醇作为汽车燃料的主要目的是节约化石燃料和减少汽车尾气的污染,以氢能源为动力的汽车能真正实现“零排放”但氢能源目前还不能广泛使用的原因是氢气的制取成本高、贮存困难。


科目:初中化学 来源: 题型:
【题目】向盛有10g49%稀硫酸的烧杯中加入5.6克的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列说法正确的是( )
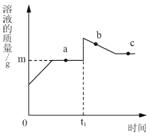
A. 取a点是溶液,加入锌粉,有气体放出
B. b点时,溶液中溶质只有一种
C. c点时,烧杯中固体一定是铜
D. m=12.7
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铜是铜锌合金。可塑性好,耐腐蚀,许多金色饰品就是用它来制作的。现称取20.0 g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至没有气泡产生为止。请结合下列图示计算。

(1)该20.0 g黄铜样品中含锌的质量为________。
(2)完全反应时生成气体的质量为________g。
(3)计算所得溶液中溶质的质量分数为__________(结果精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种。同学们为了确定该粉末的成分,进行如下探究。请你参与探究并回答问题。
(提出猜想)假设l:红色粉末是铜粉; 假设2:红色粉末是氧化铁粉; 假设3:红色粉末是____。
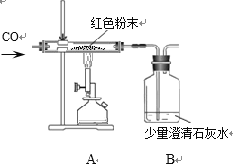
(实验探究)某同学为进一步确定红色粉末的组成,称取该粉末5.0g装入硬质玻璃管中,按下图装置在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
反应前 | 反应后 | |
Ⅰ组 | 玻璃管和红色粉末的总质量为37.3 g | 玻璃管和固体物质的总质量为36.1 g |
Ⅱ组 | 洗气瓶和所盛溶液的总质量为180.0 g | 洗气瓶和瓶中物质的总质量为183.1 g |
(交流讨论)
(1)应该选择___________组的实验数据来计算确定组成.最终计算结果表明:该红色粉末的组成是假设____(填序号)成立。
(2)写出A装置中发生反应的化学方程式________________________;实验中观察到A装置中的现象为____________________。
(3)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处?请判断并说明理由:________________________________。
(反思评价)
(1)从环保角度,该装置有严重不足之处。你认为应该如何改进?____________________。
(2)实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的空气已排尽的方法是_________________________。
(3)工业上用2000t含氧化铁75%的赤铁矿,可炼出含铁97%的生铁_________________吨?(结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碱式氧化镍(化学式为:NiOOH)可用作镍氢电池的正极材料。工业上以某废液(主要溶质为:硫酸镍,其化学式为:NiSO4,另外还含有一些其他杂质。)为原料生产NiOOH 的步骤如下:
步骤 I:向废液中加入 Na2CO3 溶液生成沉淀,过滤,洗涤,得到固体 NiCO3。
步骤 II:向固体 NiCO3 中加入稀硫酸,固体溶解,得到硫酸镍溶液。
步骤 III:调节硫酸镍溶液的 pH,可将硫酸镍转化为氢氧化镍沉淀(化学式为:Ni(OH)2), 过滤并洗涤沉淀。
步骤 IV:将氢氧化镍沉淀置于空气中加热,生成碱式氧化镍(化学式为:NiOOH)。 请回答以下问题:
(1)NiOOH 中 Ni 的化合价为:_____。
(2)写出向废液中加入 Na2CO3 溶液生成 NiCO3 沉淀的化学方程式_____。
(3)步骤 I 和步骤 II 的作用是:_____。
(4)步骤 IV中生成了碱式氧化镍和水,请写出步骤 IV中发生反应的化学方程式:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学小组取形状和大小均相同的镁片,锌片,铝片、铁片,分别与5%的稀硫酸反应,测得反应速度由大到小的顺序是:镁>锌>铁>铝。为什么实验结果与金属活动性顺序不完全一致呢?小组同学猜想可能的原因,设计了如下探究实验。(说明:实验中所用酸的体积相等且足量)
实验序号 | 操作 | 反应速度 | |
Ⅰ | 取形状和大小均匀相同的镁片、铝片、铁片、锌片,________。放入试管中,分别同时加入 | 5%的稀硫酸 | 镁>锌>铁>铝 |
Ⅱ | 10%的稀硫酸 | 镁>锌>铁>铝 | |
Ⅲ | 5%的稀盐酸 | 镁>铝>锌>铁 | |
Ⅳ | 10%的稀盐酸 | 镁>铝>锌>铁 | |
(1)上述实验中横线处的操作是__________。设计实验Ⅰ、Ⅱ的目的是____________________。
(2)对比实验_____(填序号),初步判断铝与酸反应的速度在排序中出现变化的原因可能与_____有关,某同学向铝与不同浓度稀硫酸反应的试管中加入等量氯化钠固体,发现反应速度均明显变快,从微观角度分析,原因是_______________。
(3)实验后,同学们绘制了本次探究实验中铝与稀盐酸反应的下列图象,其中正确的是_____(填字母序号),判断依据为____________________。
A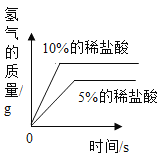 B
B 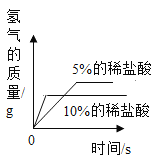 C
C
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁是一种用途很广的金属,目前世界上60%的镁是从海水(溶质主要含NaCl和MgCl2等)中提取的,主要步骤如下:
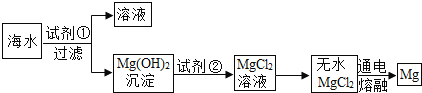
(1)工业生产中,加入试剂①发生反应的化学方程式为______,试剂②的名称为______;
(2)写出无水MgCl2在熔融状态下电解制取金属镁的化学方程式______,该反应属于基本反应类型中的______反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知金属锰(Mn) 的活动性位于铝和锌之间,请预测硫酸锰(MnSO4)的化学性质,说明预测的依据,并设计实验验证。经查阅资料,锰的化合物相关性质如下:
物质 | MnO | Mn(OH)2 | MnCl2 | Mn(NO3)2 | MnSO4 | MnCO3 |
在水中的溶解性 | 不溶于水的草绿色粉末 | 难溶于水的白色固体 | 可溶于水形成淡红色溶液 | 溶于水形成淡红色溶液 | 溶于水形成淡红色溶液 | 难溶于水的粉红色固体 |
限选试剂:MnSO4溶液、(NH4)2CO3溶液、Na2SO4溶液、BaCl2溶液、NaOH溶液、稀盐酸、镁条、铜片。
预测 | 预测的依据 | 验证预测的实验操作与预期现象 |
①能够与含Ba2+的可溶性盐反应 | MnSO4溶液中含 | 取少量MnSO4溶液于试管中,_____,如果观察到_____,则预测成立。 |
②能够与_____(填物质类别)反应 | _____。 | 取少量MnSO4溶液于试管中,_____,如果观察到_____,则预测成立。 |
③能够与_____(填物质类别)反应 | _____。 | 取少量MnSO4溶液于试管中,_____,如果观察到_____,则预测成立。 |