
【题目】根据下列实验装置图回答问题:
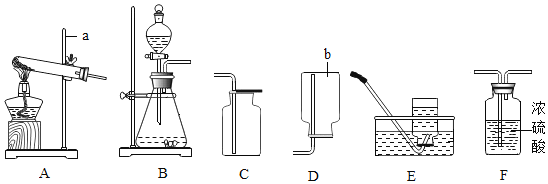
(1)写出a仪器、b仪器的名称:____、____。
(2)实验室可用过氧化氢溶液和少量二氧化锰混合快速制取氧气,二氧化锰在此反应中起____作用,若利用该反应制取并收集一瓶干燥的氧气,应选择上列装置中的B、____和C。
(3)实验室制取CO2反应的化学方程式为____,实验结束后,从反应残留物中提取固体溶质时,按如下流程操作:
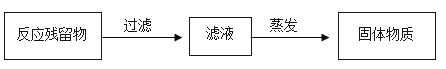
过滤所用的玻璃仪器除烧杯、玻璃棒外,还有____(填仪器名称),在蒸发过程中,当____时,停止加热,利用蒸发皿的余热使滤液蒸干。
(4)Cu2(OH)2CO3是碱式碳酸铜的化学式,它是一种绿色粉末,俗名铜绿,受热条件下会分解成三种氧化物,其受热分解的化学方程式为____。若用实验证明加热碱式碳酸铜有新物质生成,应将干燥的碱式碳酸铜放入___装置进行反应,观察到__,证明生成物之一为水。
【答案】铁架台 集气瓶 催化 F ![]() 漏斗 蒸发皿中出现较多量固体
漏斗 蒸发皿中出现较多量固体 ![]() A 试管口有小液滴形成
A 试管口有小液滴形成
【解析】
(1)a为固定装置的铁架台,b为收集气体的集气瓶;
(2)利用过氧化氢和二氧化锰制备氧气时,二氧化锰加速过氧化氢的分解,起到催化作用;过氧化氢溶液和二氧化锰制取氧气为固液反应物,反应条件则不需要加热,所以发生装置为B,制备干燥氧气不能用排水法收集,选择向上排空法收集,因此收集装置为C,过氧化氢溶液带有水蒸气,所以需要干燥,浓硫酸具有吸收性,且不与氧气反应,所以可以干燥生成的氧气,利用C收集干燥的氧气,所以还需要F,吸收水蒸气;
(3)实验室采用大理石与稀盐酸制备二氧化碳,大理石主要组分为碳酸钙,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,书写化学方程式注意配平及气体符号,所以化学方程式为![]() ;过滤除了利用烧杯盛取滤液,玻璃棒引流外,还需要漏斗进行过滤;蒸发时不得将液体蒸干,当蒸发皿中出现较多固体时,停止加热,利用余热将水分蒸干,得到固体;
;过滤除了利用烧杯盛取滤液,玻璃棒引流外,还需要漏斗进行过滤;蒸发时不得将液体蒸干,当蒸发皿中出现较多固体时,停止加热,利用余热将水分蒸干,得到固体;
(4)根据化学式可以得出三种氧化物为氧化铜、水和二氧化碳,所以分解的化学方程式为![]() ;碱式碳酸铜为固体,反应条件为加热,所以需要选择固体加热装置,所以为A,试管口向下倾斜,可以在试管口观察是否有液滴生成,判断生成物是否含有水。
;碱式碳酸铜为固体,反应条件为加热,所以需要选择固体加热装置,所以为A,试管口向下倾斜,可以在试管口观察是否有液滴生成,判断生成物是否含有水。


 智能训练练测考系列答案
智能训练练测考系列答案科目:初中化学 来源: 题型:
【题目】铁、铝、铜是人类使用最多的三种金属。
(1)铝具有很好的抗腐蚀性能是因为其表面易形成一层致密的保护膜,该保护膜的成分是_____(填化学式);
(2)“湿法炼铜”的原理是硫酸铜溶液与铁反应,该反应的化学方程式为_____,该反应属于_____反应(填基本反应类型);
(3)工业用磁铁矿炼铁的化学方程式是_____;
(4)向FeSO4、CuSO4 的混合溶液中投入一些铝粉,充分反应后过滤,向滤渣中加入少量稀硫酸有气泡产生。则滤液中一定不含_____(填溶质的化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Mg(OH)2是一种新型的阻燃剂,在温度达到380°C时吸收热量并分解产生水,同时生成的氧化镁附着于可燃物的表面阻止了进一步燃烧。
(1)Mg(OH)2 受热分解化学方程式是________________;工业常用氯化镁溶液与烧碱溶液制取Mg(OH)2,化学方程式是___________________。
(2)某同学用氨水在实验室模拟制取Mg(OH)2的过程:一定温度下,往含一定量氯化镁的溶液中加入适量氨水( 氨水易挥发),再经过滤、洗涤得到Mg(OH)2晶体。为探究获得较高Mg(OH)2晶体转化率条件,该同学进行如下对比实验,数据如下:
实验编号 | 氯化镁溶液溶质质量分数 | 反应温度/°C | Mg(OH)2转化率/% |
a | 10% | 30 | 27.06 |
b | 15% | 30 | 56.77 |
c | 15% | 40 | 69.64 |
d | 15% | 60 | 54.30 |
e | 20% | 60 | 50.60 |
①实验b和c的目的是______________________。
②由实验可知,能够得到最多Mg(OH)2的条件是溶质质量分数_______和温度__________°C。
③在氯化镁溶液溶质质量分数都是15%的情况下,60°C 时Mg(OH)2的转化率比40°C时低的原因是________________。
(3)根据燃烧的条件可知,Mg(OH)2能做阻燃剂的原因是________________(填编号)。
①清除可燃物 ②使温度 降低到着火点以下 ③隔绝空气
(4)氯化镁溶液通过循环利用,理论上转化率可以达到100%。若生产了2.9吨Mg(OH)2,理论上需要原料20%的氯化镁溶液_______________吨。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】南通地铁的正式开建,标志着南通进入“地铁时代”。

(1)地铁列车车体大量使用的镁铝合金属于____________(填“金属材料” 或“合成材料”),镁铝合金的优点是_____________。
(2)地铁建造过程中需要使用大量的钢铁。工业炼铁可利用一氧化碳与氧化铁反应,写出该反应的化学方程___________________。
(3)地铁信息传输系统中使用的光导纤维和电子芯片的关键材料分别为二氧化硅(SiO2)和晶体硅(Si)。将二氧化硅转化为硅的过程属于________________(填“物理变化”或“化学变化”)。
(4)地铁施工过程中产生的废水、废浆以及机械漏油等,都会对水体产生污染。使用活性炭可对污水进行处理,这是利用了活性炭的 __________________性。
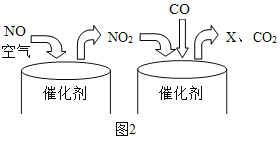
(5)地铁施工工程车的尾气中含 NO、CO。尾气经过如图所示催化转化后,可实现达标排放。写出该反应的化学方程式:____________________,其中发生还原反应的物质为 _______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了证明氢氧化钠和稀盐酸反应有新物质生成,兴趣小组的同学进行了下列实验:
(实验目的)证明氢氧化钠溶液与稀盐酸发生了反应且生成了新物质。
(实验原理)___________ (用化学方程式表示)。
(药品仪器)
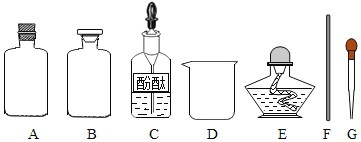
(实验步骤)
①取______(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色。
②用G_______(填仪器名称)向①所得的溶液中滴加稀盐酸,直至红色刚好消失。
③向②所得溶液中继续滴加稍过量稀盐酸,溶液保持无色。
④用F蘸取③所得溶液,在酒精灯上灼烧,有白色固体产生。
(思考拓展)
(1)步骤③的目的是:__________。
(2)进一步确认步骤④所得的白色固体不是氢氧化钠,不能选用的试剂有:_________。
ACuSO4溶液 BNa2CO3溶液 C无色酚酞试液 D(NH4)2SO4溶液
(3)已知酚酞试液在不同pH时的变色情况如下表。
pH | <8.2 | 8.2~10.0 | >10.0 |
颜色 | 无色 | 红色 | 无色 |
小文同学发现向某氢氧化钠溶液中滴加酚酞试液, 发现溶液瞬间变红但立即又变成无色,他接着逐滴加入稀盐酸,某一时刻溶液变红了,没有褪色,继续滴加稀盐酸,后褪至无色。小文认为该氢氧化钠溶液刚开始时滴加酚酞试液出现异常现象的原因,可能是氢氧化钠溶液浓度过大导致的,请你设计实验方案帮助他证明猜想:_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某能量型饮料及标签中的部分成分,请回答下列问题;

(1)该饮料提供了人体所需六大营养素中的水、糖类和______。
(2)该饮料中的钠元素由氯化钠提供,则配制100mL饮料氯化钠的质量是______mg。
(3)饮料瓶的材料是PET,化学式为(C10H8O4)n,它属于______(填“有机化合物”或“无机化合物”)。在饮料瓶的生产过程中,以下做法合理的是______
a加高烟囱排放废气 b采用新技术加强污水处理 c采用“光伏发电”和“煤改气工程”提供能量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质用于实验室制取气体,可以直接采用如图所示装置的是( )

A. 用氯酸钾和二氧化锰制取氧气 B. 用锌块和稀硫酸制取氢气
C. 用过氧化氢溶液和二氧化锰制取氧气 D. 用木炭与氧化铜反应制取二氧化碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验是进行科学探究的重要方式。
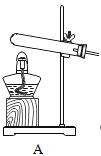
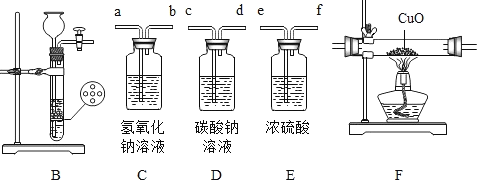
(1)写出一个用 A 装置来制取O2的反应的化学方式:__________________。
(2)某兴趣小组的同学用 B 装置选择锌粒和浓盐酸来制取氢气并探究其还原性。现要 得到一瓶纯净、干燥的氢气,则从发生装置产生的气体沿导管口之间的连接顺序 是__________(填导管口字母)。将收集好的气体通入F装置,发生反应的化学方程式是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学实验中要研究纯净物的组成、结构、性质等,常常需要把混合物进行除杂、分离和提纯等。为了将氯化钠和氯化钙两种固体混合物分离,设计了下列实验方案:

试回答下列问题:
①操作②中加入过量Na2CO3的目的是___________,发生反应的化学方程式为____________。
②甲同学认为,上述所得的NaCl固体不纯,要得到较纯净的NaCl固体,需增加一步实验,他的做法是___________。
③为进一步探究混合物中氯化钠的质量分数,同学们分别提出了两个方案,方案1所选数据是称得混合物A的总质量还有沉淀B的质量;方案2所选数据是混合物A的总质量还有实验改进后所得的氯化钠固体的质量。试判断哪个方案所选的数据不合理并说明理由___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com