
根据下图四个化学实验,回答问题:(提示:Cu与Zn的合金称为黄铜)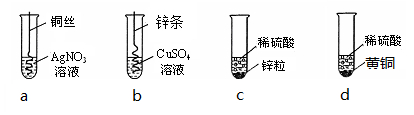
(1)描述实验a中的实验现象 。
(2)要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是 (填实验序号)。
(3)在c实验后的剩余溶液中,一定有的溶质是 ,可能有的溶质是 ,为了确定可能有的溶质,可加入 (填选项序号)
Ⅰ.氯化钡溶液 Ⅱ.氢氧化铜 Ⅲ.氢氧化钠溶液 Ⅳ.锌粒
(4)为了测定d中稀硫酸的溶质质量分数,取20g该黄铜样品于烧杯中,向其中分4次加入该稀硫酸,充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
| | 加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) |
| 第1次 | 25 | 16.75 |
| 第2次 | 25 | 13.5 |
| 第3次 | 25 | m |
| 第4次 | 25 | 12.0 |
(1)铜片表面有银白色物质析出
(2)a b
(3)ZnSO4 H2 SO4 ⅡⅣ
(4)12
解析试题分析:根据金属活动性顺序的应用,位于氢前面的金属能把酸中的氢置换出来生成氢气;位于前面的金属能把位于后面的金属从化合物的溶液中置换出来;锌与硫酸反应生成的是硫酸锌,故溶质一定有硫酸锌,可能还有硫酸;硫酸能是氢氧化铜溶解,能与锌反应生成气体。
设H2 SO4x mol
20-16.75/65=0.05
Zn + H2 SO4→ ZnSO4+H2↑
1 1
0.05 mol x mol  =
= 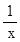 x =" 0.05" mol
x =" 0.05" mol
0.05×98/25=0.196(或19. 6%)
考点:据金属活动性顺序


 53随堂测系列答案
53随堂测系列答案科目:初中化学 来源: 题型:填空题
过去的暖气片由铸铁制成,是因为铁具有良好的 性,但它易生锈,所以逐渐被铝合金暖气片取代.铝合金更耐腐蚀,原因是 .金属的广泛用途主要由性质决定,如图是某同学设计的实验,他想要探究的问题是 ,其中发生反应的化学方程式为 . 
查看答案和解析>>
科目:初中化学 来源: 题型:问答题
金属在生产生活中有着广泛的应用.
(1)据有关报道,每年因锈蚀而报废的铁制品约占年产量的20%~40%,铁制品生锈的条件是 .
(2)写出用稀盐酸除铁锈的化学方程式 .
(3)同学们通过实验来验证Cu、Fe、Ag三种金属的活动性顺序.实验室提供的药品有:
Cu(NO3)2溶液、AgNO3溶液、Fe(NO3)2溶液、稀盐酸、铜丝、铁丝、银丝.
Ⅰ、小华同学设计并完成了如下实验:
①把铁丝插入装有稀盐酸的试管中; ②把铜丝插入装有稀盐酸的试管中;
③把银丝插入装有稀盐酸的试管中; ④把铜丝插入装有AgNO3溶液的试管中.
观察到①中的实验现象是 ,④中的化学方程式是 .你认为小华所做的实验 (填序号)是多余的.
Ⅱ、后来,小贝只选用了上述药品中的三种,通过两步实验,也达到了实验目的.他选用的三种药品是 (写出一种药品组合即可).
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
学习了金属的化学性质后,某兴趣小组进行了如下实验:将足量镁条加入到氯化铜溶液 中,观察到镁条表面有气泡产生,同时有红色固体附在镁条表面。
【提出问题】产生气体是什么物质? 有红色固体又是什么物质?
【查阅资料】在金属活动性顺序里,位于氢后面的金属Cu,在常温下虽然不能与稀盐酸、稀硫酸反应,但可以与稀硝酸反应,其化学方程式为:
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO ↑ +4H2O
反应生成的NO是无色、难溶于水的气体,在常温下与空气中的O2迅速化合生成 N02,N02是红棕色、有刺激性气味的有毒气体。
【作出猜想】猜想一:气体可能是氢气、红色固体是金属氧化铁;猜想二:气体可能是氢气、 红色固体是金属铜;猜想三:气体可能是二氧化碳、红色固体是金属铜。
【交流讨论】大家思考后,一致认为猜想一和三不合理,其理由是_____________________。
【实验与结论】
| 实验步骤 | 现象 | 结论 |
| (1)取少量红色固体于一支洁净的试管中,加入稀盐酸 | __________________________________ | 猜想一不成立 |
| (2)①用尖嘴导管将气体导出并引燃,同时在上方放一块干冷的玻璃片 ②取少量红色固体于一支洁净的试管中,加入稀硝酸 | 该气体能燃烧,且玻璃片上有______出现 红色固体溶解,得到蓝色溶液同时看到试管上部有红棕色气体产生 | 猜想二成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
在生活中经常曝出某品牌金饰品掺假的事件,引起学生的好奇,某化学兴趣小组在老师的帮助下,对几种常见金属饰品所含的金属进行了相关的探究活动.
【提出问题】(1)怎样鉴别真假黄金?(2)怎样确定钯的金属活动性?
【查阅资料】
(1)假黄金通常是黄铜(Cu﹣Zu合金) (2)钯(Pd)呈银白色,有金属光泽,可用作饰品
【实验药品】钯、铂(Pt)、稀盐酸、硝酸银溶液和氯化钯(PdCl2)溶液
【实验探究】
(1)鉴别黄金样品的真假:取黄金样品于试管中,滴加稀盐酸后,观察黄金样品表面有气泡产生,该气体是 (填名称),说明此样品为 (填“真”或“假”)黄金.
(2)探究钯的金属活动性:依据生活经验,同学们猜测钯的活动性可能与银和铂相近,于是他们利用上述药品进行如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 把钯浸入硝酸银溶液中 | 无明显现象 | 钯的活动性比银 |
| 把铂浸入氯化钯溶液中 | | 钯的活动性比铂强 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
勇往直前学习活动小组的同学正在做一个探究实验,他们准备了以下实验用品:铁
架台、干燥洁净的几支试管、洁净无锈的4枚铁钉、植物油、久置的蒸馏水、胶塞、棉花和干燥剂氯化钙,还可以选用其他物品。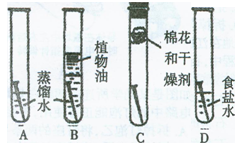
【分析思考】他们探究的问题是(1)_______________;
【实验准备】小冰检查实验用品时,发现有一种不符合实验要求,请你写出这种用品(2)_________________,
并提出你的解决办法(3)_________________________;
【实验观察】一切用品按要求准备就绪,同学们按照图
示进行了探究实验,B中植物油的作用是(4)________
________________________________________________,10天后,他们会观察
到的实验现象是(5)_________________________________________________。
【实验总结】铁生锈的条件是(6)_____________________________________。
【实验拓展】爱思考勤实践的小城补充了D试管中的实验,发现这只试管中的
铁钉锈蚀最严重,根据此实验和学过的金属的化学性质,小城知道,使用铁制
品时,要尽量避免与(7)___________物质接触;
【实验感悟】金属的锈蚀每时每刻都在发生着,金属的防护刻不容缓!
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
小红发现,金店里有两种不同的“白金”,单价相差悬殊,小红很好奇,打算进行研究。
【查阅资料】市场上所谓的“白金”通常有两种,一种是金、镍、铜、锌的合金,称为白色金;另一种是铂金,铂是一种银白色的贵重金属,用于耐腐蚀的化学仪器及首饰等,俗称“白金”,元素符号Pt。小红结合化学课上学习的金属活动性顺序,展开了下列实验活动。
(1)鉴别两种白金,她的方法可能是________________________;
(2)探究Zn、Ni(镍)、Cu的活动性顺序。
【做出假设】对三种金属的活动性顺序提出可能的假设①Zn>Ni>Cu;②Zn>Cu>Ni你觉得还有其他的可能性吗?请把它们写出来(一种即可)
假设:③______________________…………
【查阅资料】小红同学查阅了部分含镍化合物的溶解性如下表所示,且得知镍能与酸反应。
| | OH- | NO3- | SO42- | Cl- |
| Ni2+ | 不 | 溶 | 溶 | 溶 |
| 金属 | Ni | Zn | Cu |
| 与盐酸反应的现象 | 气体产生缓慢, 金属逐渐溶解 | 气体产生迅速, 金属迅速溶解 | |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
(12分)以下是甲、乙两同学对有关镁与盐酸反应的系列研究。
研究一:镁与盐酸反应过程中的能量变化以及反应速率的变化:
(1)反应中试管外壁发烫,说明镁与稀盐酸反应是 反应(填
“吸热”或“放热”)。
(2)实验测得镁片产生气体的速率(v)与时间(t)的关系如图所示,
则t1~t2时间内反应速率逐渐加快的主要原因是 。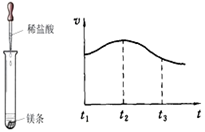
研究二:反应后所得溶液的酸碱性探究:
(3)甲同学反应后用pH试纸测定试管中溶液的酸碱性,发现pH小于7,说明甲同学所得溶
液呈 性(选填“酸”“碱”或“中”)。
甲同学:猜想Ⅰ:稀盐酸过量,使溶液pH小于7;猜想Ⅱ:氯化镁溶液pH小于7。为
验证猜想,甲同学需测定 溶液的酸碱性,实验表明该溶液显弱酸性。
(4)乙同学重复甲同学实验时,发现反应后所得试管中溶液pH大于7。发现实验与甲同学实
验不同的是,反应后的试管中镁条有剩余。乙同学猜想可能是镁与热水反应生成了碱性
物质。乙同学为验证猜想,在滴有两滴酚酞的热水中放入一段打磨过的镁条,观察到溶
液很快变为红色,同时还观察到镁条表面有气体生成,收集并点燃该气体,发现能燃烧,
请根据实验现象写出镁与水反应的化学反应方程式 。
(5)金属氯化物溶液pH值大小与金属的活动性有关,如氯化钠溶液显中性,氯化镁溶液显弱酸性,则氯化钾溶液显 性。
(6)活泼金属能与水在一定条件下反应。实验发现钠与冷水剧烈反应,产生大量的气体。由
此可见金属与水反应与金属的活动性顺序 (填“有关”或“无关”)。
研究三:金属活动性强弱与原子结构的关系:
下图为镁原子、钙原子和钡原子结构示意图。已知其中Ba的活动性最强,据此推测,金属的活动性除与原子的最外层电子数有关,还与 有关。
研究四:确定镁条的成分:
称取3.2g表面被氧化的镁条, 放入100g稀盐酸中恰好完全反应,生成气体0.2g。求:
(7)此镁条中金属镁的质量。(写出计算过程,共3分)
(8)反应后所得溶液中溶质的质量分数 。(计算结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
粗盐中含有难溶性杂质和多种可溶性杂质(氯化镁、氯化钙等).某同学为了提纯粗盐,设计了如图所示的实验方案:(友情提示:碳酸镁微溶于水)
(1)用化学方程式回答,步骤②的主要目的是
(2)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中任意一种就能将两种可溶性杂质除去,你认为这种方法 (选填“可行”或“不可行”),理由是
(3)有同学认为原实验方案不完善,做出这种评价的依据是
(4)为了完善原实验方案,你的做法是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com