
【题目】钙被称为人体中的“钢筋混凝土”。
(人体中的钙)
(1)人体缺钙不会导致_____(填字母,下同)。
A.佝偻病 B.侏儒症 C.骨质疏松
(2)人体中钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其中磷元素化合价为_____。
(单质钙)
提出问题:钙的化合物很多,为什么我们很少提起单质钙呢?
思考猜想:钙的化学性质活泼。
实验验证一:如图1所示
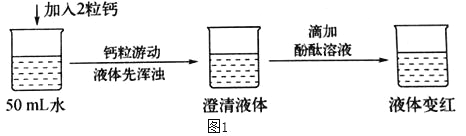
查阅资料:在一个化学反应中,有元素化合价升高,同时就有元素化合价降低。
(3)实验结论:①写出钙与水反应的化学方程式_____。
②该反应_____(填“吸收”或“放出”)热量。
(干燥剂中的钙)
提出问题:一包生石灰干燥剂,使用一段时间后可能有哪些固体?
猜想假设:固体中含有氧化钙、氢氧化钙、碳酸钙。
实验验证二:
(4)取固体样品加入水中,若温度明显升高,则含有_____;滴加酚酞后液体变红;继续加足量稀盐酸,如观察到_____,则固体中含有碳酸钙。
(5)小明认为无法判断是否含有氢氧化钙,理由是_____。
(6)为了进一步确定固体样品的成分及质量,实验小组利用如图2所示的装置(夹持仪器省略)进行实验。
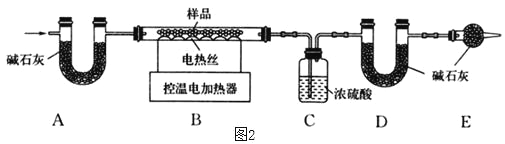
查阅资料:氢氧化钙加热至580℃、碳酸钙加热至825℃分别分解生成两种氧化物。
①实验前首先要_____,再装入药品。
②装置E的作用是_____。
③控温电加热器使装置B中反应完全,再通一段时间空气,测得反应前后装置C、D分别增重18.0g和22.0g,将装置B中反应后剩余的固体氧化物加入足量水中溶解,蒸发所得固体(不含水)增重36.0g,求原固体样品中各成分的质量__________。(请写出计算过程)
【答案】B+5 。Ca+2H2O=Ca(OH)2+H2↑ 。放出氧化钙 ;有气泡产生氧化钙与水反应生成的氢氧化钙溶液也呈碱性 。检查装置的气密性 ,防止空气中的CO2和H2O进入D 。氢氧化钙的质量为74g,含碳酸钙的质量为50g,含氧化钙的质量为28g。
【解析】
根据生石灰的性质,碱、盐的化学性质,化合物中元素化合价的代数和为零进行分析。根据实验得到的数据结合物质的性质进行计算。
(1)人体缺钙会导致佝偻病和骨质疏松,不会导致侏儒症,故选B;
(2)钙元素显+2价,氧元素显﹣2价,氢氧根显﹣1价,设:磷元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)×10+6x+(﹣2)×4×6+(﹣1)×2=0,则x=+5;
(3)①钙粒加入水中,钙粒的游动说明有气体生成,反应后的溶液能使酚酞变红说明的碱性物质生成,根据质量守恒定律可知该碱性物质是氢氧化钙,该反应中钙元素的化合价由0价变成了+2价,化合价升高,在一个化学反应中,有元素化合价升高,同时就有元素化合价降低。水中的氧元素化合价为-2价,氧元素的化合价已是最低不可能再降低,化合价降低的只可能是氢元素,氢元素在水中的化合价是+1价,可降低为0价,氢气的化合价为0价,所以钙与水反应生成氢气和氢氧化钙,化学方程式是Ca+2H2O=Ca(OH)2+H2↑;
②钙粒加入水中,开始时溶液变浑浊,降温后变成澄清溶液,氢氧化钙溶解度随着温度升高而减小,因此该反应属于放热反应;
(4)氧化钙与水反应生成氢氧化钙,该反应是放热反应。取固体样品加入水中,若温度明显升高,则含有氧化钙;由于生成的氢氧化钙溶液显碱性,滴加酚酞后液体变红;碳酸钙与盐酸反应生成氯化钙、水和二氧化碳。继续加足量稀盐酸,如观察到有气泡产生,则固体含有碳酸钙;
(5)氧化钙与水反应生成的氢氧化钙溶液也呈碱性,因此无法判断是否有氢氧化钙;
(6)①由于该实验需测定生成的气体质量,所以实验前首先要检查装置的气密性,再装入样品;
②碱石灰能吸收二氧化碳和水。装置D中的作用是吸收二氧化碳,空气中二氧化碳和水蒸气进入装置D会影响实验结果。装置E是为了防止空气中的二氧化碳和水蒸气进入装置D,影响实验结果;
③根据“查阅资料:氢氧化钙加热至580℃、碳酸钙加热至825℃分别分解生成两种氧化物”可知氢氧化钙分解生成氧化钙和水,碳酸钙分解生成氧化钙和二氧化碳。浓硫酸具有吸水性,碱石灰能吸收二氧化碳。控温加热使装置B中反应完全,再通一段时间空气,测得反应前后装置C、D分别增重18.0g和22.0g,则氢氧化钙分解生成水的质量为18.0g,碳酸钙分解生成二氧化碳的质量为22.0g,设:氢氧化钙的质量为x,分解生成的氧化钙的质量为y,碳酸钙的质量为z,分解生成的氧化钙的质量为m,则
Ca(OH)2![]() CaO+H2O
CaO+H2O
74 56 18
x y 18.0g
![]() x=74g
x=74g
![]() y=56g
y=56g
CaCO3 ![]() CaO+CO2↑
CaO+CO2↑
100 56 44
z m 22.0g
![]() z=50g
z=50g
![]() m=28g
m=28g
将装置B中反应后剩余的固体氧化物加入足量水中溶解,蒸发所得固体(不含水)增重36.0g,设:参加反应的氧化钙的质量为n,则
CaO+H2O= Ca(OH)2 固体增加质量
56 74 74﹣56=18
n 36.0g
![]() n=112g
n=112g
则原固体样品中CaO的质量为112g﹣56g﹣28g=28g。由以上分析可知,原固体样品中含氢氧化钙的质量为74g,含碳酸钙的质量为50g,含氧化钙的质量为28g。
答:原固体样品中含氢氧化钙的质量为74g,含碳酸钙的质量为50g,含氧化钙的质量为28g。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】如图是某同学“自制汽水”的配料表,请回答下列问题:

⑴除水以外,新鲜果汁中还富含的营养物质是__________。
⑵下列可用于测汽水酸碱度的是(________)
A.紫色石蕊试液 B.无色酚酞试液 C. pH试纸
⑶制汽水的过程中,小苏打与柠檬酸反应产生二氧化碳,请再举一例小苏打的用途_____。写出二氧化碳与石灰水反应的化学方程式_______。
⑷塑料瓶可用来盛装汽水,在塑料中添加土豆淀粉制成的“土豆农膜”是一种新型可降解塑料,下列有关说法正确的是(________)
A.塑料瓶用的是聚氯乙烯塑料
B.该材料有助于解决农村“白色污染”问题
C.土豆农膜比普通塑料农膜容易降解
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了下图实验,已知溶液甲呈蓝色。

(1)向固体乙上滴加盐酸时____________(填“有”或“没有”)气泡产生。
(2)溶液甲中一定含有哪些溶质?(写化学式)__________________
(3)请写出该实验过程中所发生反应的化学方程式。______________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、D、F均为单质,其中D、F为金属单质,D的合金是使用最多的金属材料;B为黑色氧化物,C是一种常见的酸,E是相对分子质量为160的蓝色溶液.
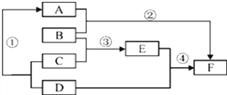
(1)请写出下列物质的化学式:B________________,D______________________.
(2)上述反应中,不属于置换反应的是_______(填序号).
(3)请写出反应④的化学方程式:___________________________________.
(4)请写出C的一种用途 ______________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是不含结晶水的a、b、c 三种物质的溶解度曲线,下列说法正确的是( )
A. t2℃时,向100g物质b的饱和溶液中加入80g物质a,充分搅拌后,最终得到180g溶液
B. 将t2℃时a、b两种物质的饱和溶液降温到t1℃时,析出晶体的质量:a>b
C. 用等质量的a、b、c三种固体配制成t2℃时的饱和溶液,所得溶液质量的大小关系是:c溶液>b溶液>a溶液
D. 将t1℃时三种物质的饱和溶液升温到t2℃时,所得溶液中溶质的质量分数的大小关系是:b>a=c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】共享单车采用手机扫描二维码来解锁,而手机通常采用高能的锂(元素符号为Li)电池作为电源。
(1)锂原子的原子结构示意图如图所示![]() ,在化学反应中容易______而成为锂离子,其离子符号为______。
,在化学反应中容易______而成为锂离子,其离子符号为______。
(2)某种锂电池放电时的总反应为Li+MnO2=LiMnO2。LiMnO2中锰元素的化合价为__________。
(3)金属锂除了制造锂电池外,还可以用于储存氢气,其原理是金属锂与氢气化合生成白色粉末状的氢化锂(LiH),氢化锂与水反应生成氢氧化锂和氢气。写出氢化锂与水反应的化学方程式___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】关于铝元素相关知识的学习流程如下。

回答下列问题:
(1)铝的相对原子质量是___________,铝离子的符号为__________。
(2)元素的__________(填“化学”或“物理”)性质主要与原子的最外层电子数关系密切。
(3)依照上述流程填空:___、___、___、___、___
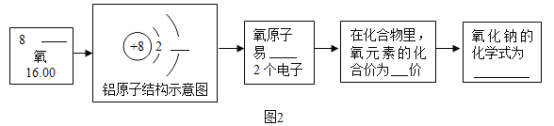
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某反应的微观示意图,下列说法不正确的是( )
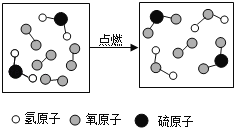
A.反应物中有单质
B.该反应为置换反应
C.生成物的分子个数比为1:1
D.参加反应的![]() 和
和![]() 的质量比为17:24
的质量比为17:24
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是教材中验证质量守恒的定律的实验,请回答相关问题:
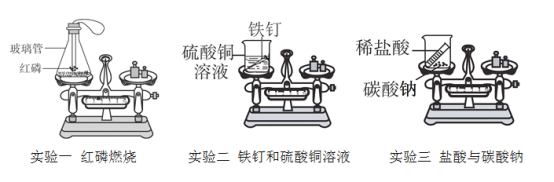
(1)实验一,先将胶塞上的玻璃管末端加热至红热,再接触瓶内红磷,其目的是________;
(2)实验二,铁与硫酸铜(CuSO4)溶液作用生成硫酸亚铁(FeSO4)和铜,写出该反应的化学方程式 ________;
(3)实验三,碳酸钠与稀盐酸反应的化学方程式为Na2CO3+2HCl═2NaCl+CO2↑+X,其中X的化学式为________,这个反应后烧杯中物质的质量减少的原因是________;
(4)为了验证质量守恒定律,在选择化学反应和装置时应注意的问题是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com