
【题目】金属材料在生活中有广泛的用途。
(1)下图是铁锅的示意图,铁锅手柄使用的塑料具有______________性 (填“热塑”或“热固”)。

(2)铝锅轻便、耐用,其原因是_____________(写一条即可)。
(3)铁制品保存不当,极易生锈,其生锈条件是铁与___________共同接触。
(4)废旧铁锅、铝锅等金属制品不要随意丟弃,应回收利用,这样做的意义是________________。
(5)厨房中的下列物品所使用的材料属于金属材料的______________(填字母)。
A钢化玻璃
B不锈钢炊具
C纯棉手套
D保鲜膜
(6).某同学在实验室进行了两个有关金属性质的实验:
实验I:取硫酸铝溶液加入装有铁粉的试管中
实验Ⅱ:取硫酸铜溶液加入装有铁粉的试管中
在上述两个实验结束后,该同学将实验I和Ⅱ的物质全部倒入同一个烧杯中,发现烧杯内的红色固体明显增多。一段时间后过滤,向滤渣中滴加盐酸,结果没有气泡产生。那么,滤液中所含金属离子的情况可能是________(填序号)。
①A13+
②Al3+、Fe3+
③A13+、Fe2+
④Fe2+、Cu2+
⑤A13+、Fe2+、 Cu2+
【答案】热固 铝的表面常温下易形成一层致密的氧化物薄膜,阻止内层铝继续被氧化 空气中的氧气和水 保护金属资源 B ③⑤
【解析】
(1)根据热固性是指在加热时,进行化学反应而固化,此反应是不可逆的,再加热也不能软化,热塑性可反复加热软化,冷却固化可知,铁锅手柄使用的塑料具有热固性,故填写:热固;
(2)铝锅轻便说明铝的密度较小,铝锅耐用是因为铝的表面常温下易形成一层致密的氧化物薄膜,阻止内层铝继续被氧化,因此,铝锅轻便、耐用,其原因是铝的密度比一般金属偏低,且铝的表面常温下易形成一层致密的氧化物薄膜,阻止内层铝继续被氧化,故填写:铝的表面常温下易形成一层致密的氧化物薄膜,阻止内层铝继续被氧化;
(3)铁制品在潮湿的空气中,容易生锈,因此,生锈条件是铁与空气中的氧气和水蒸汽接触,故填写:空气中的氧气和水;
(4)废旧铁锅、铝锅等金属制品不要随意丟弃,应回收利用,这样可以保护金属资源,故填写:保护金属资源;
(5)A、钢化玻璃属于无机非金属材料制成的,故不符合题意;
B、不锈钢炊具主要是由铁和碳等元素组成,属于金属材料中的铁合金,故符合题意;
C、纯棉手套是由天然纤维制成的,故不符合题意;
D、保鲜膜是由乙烯为母料通过聚合反应制成,属于有机高分子材料,故不符合题意,故填写:B;
(6)铝的金属活动性比铁强,因此硫酸铝与铁不反应,硫酸铝一定存在于滤液中,铁的金属活动性比铜强,所以,硫酸铜与铁反应,实验结束后,该同学将实验I和Ⅱ的物质全部倒入同一个烧杯中,发现烧杯内的红色固体明显增多,说明铁与硫酸铜发生反应置换出了铜,同时生成氯化亚铁,滤液里一定含有氯化亚铁,向滤渣中滴加盐酸,结果没有气泡产生,说明滤渣中没有氢前面的金属,即没有铁,但硫酸铜是否反应完,要看硫酸铜的量,当硫酸铜完全反应,滤液中所含金属离子是:A13+、Fe2+,当硫酸铜过量,滤液中所含金属离子是:A13+、Fe2+、 Cu2+,故填写:③⑤。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】某补钙剂的主要成分是碳酸钙,欲测定该补钙剂中碳酸钙的质量分数,某同学进行了如图 1 的操作,所加稀盐酸的质量与生成气体的质量关系如图 2 所示。(已知:其他成分不参与反应)
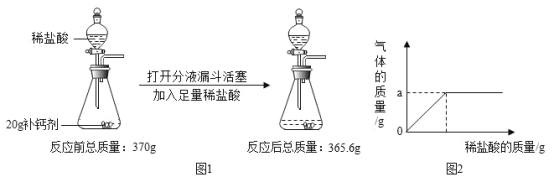
(1)图 2 坐标中 a 的数值为 ;实验中,装置的气密性对测定结果 (选填“有”或“无”)影响。
(2)实验中,要用溶质质量分数为 36.5%的浓盐酸,配制 100g 溶质质量分数为14.6%的稀盐酸,配制过程中需要加入水的质量为 。
(3)计算该补钙剂中碳酸钙的质量分数。(根据化学方程式计算,写出完整步骤)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年11月8日,在美国加利福尼亚州北部发生山火,此次山火截至11月25日已造成85人死亡,249人失踪。
(1)据专家分析,加州山火频频发生的原因之一为当地一种灌木,其叶片中富含油脂,从燃烧的条件分析,该叶片为山火的发生提供了_______________。
(2)在降雨的帮助下目前山火已基本扑灭,降雨有助于灭火的原因是___________。
(3)干粉灭火器是常用的灭火器之一,其中干粉的主要成分是碳酸氢钠(NaHCO3),它受热易分解生成碳酸钠(易溶于水)、水和二氧化碳,请写出该反应的化学方程式:____________,该反应是___________反应(填基本反应类型)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为某些物质间的转化关系(部分反应条件省略)。A、B、E、F、G均为气体,B能使稀高锰酸钾溶液退色,E、F组成元素相同,且F有毒,G是一种最轻的气体;乙、丁均为黑色的固体氧化物,反应④是工业炼铁的原理;反应②是光合作用。

(1)化学式:G_________,丙____________.
(2)反应①、④的化学方程式:①_________________;④________________________
(3)甲一定含有的元素是____________________.
(4)Fe与蓝色溶液的反应属于____________________反应(填基本反应类型)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙的溶解度(见下表)及溶解度曲线(如下图)。下列说法不正确的是
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | 甲 | 26.3 | 28.2 | 31.4 | 31.4 | 30.0 | 28.2 |
乙 | 30.6 | 28.2 | 26.8 | 31.4 | 37.5 | 42.0 | |
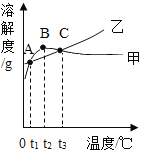
A.甲、乙为易溶物质
B.t2值介于20~40℃
C.甲、乙饱和溶液从t3降温到t2,溶质的质量分数都变小
D.等质量的甲,乙饱和溶液从t1升温到t3,为使其溶液恰好饱和,继续添加的甲、乙固体质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某 10g 碳酸钙样品含有杂质,与足量的稀盐酸反应生成二氧化碳的质量为 4.4g,则该样品中可能含有的杂质是( )
A.Na2CO3B.K2CO3
C.MgCO3D.KHCO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组利用下图装置探究制取气体的原理、方法及性质。结合装置图,回答下列问题
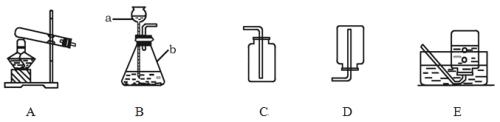
(1)写出图中标号仪器的名称:a ,b ;
(2)实验室用加热高锰酸钾制取氧气,可选用的发生装置是 (填上图字母)。
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),应选择的发生装置是 ____________(填上图字母)。
(4)该小组设计了如下图所示的实验装置,既可用于制取气体,又可用于探究物质性质。
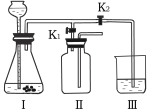
①当打开K1、关闭K2时,利用I、Ⅱ装置,可进行的实验是________(填字母)。
a.大理石与稀盐酸反应制取二氧化碳
b.锌与稀硫酸反应制取氢气
②当打开K2、关闭K1时,可以利用工、Ⅲ装置制得二氧化碳并验证其性质。实验室制取二氧化碳的化学方程式是 ;
③若要证明二氧化碳能与水发生反应,应向烧杯的水中加入 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源,与生活生产关系密切。保护水环境、珍爱水资源,是每个公民应尽的责任和义务。
(1)为了防止水的污染,下列做法有利于保护水资源的是_____(填编号)
①抑制水中所有动、植物的生长;
②不任意排放工业废水;
③大量使用化肥农药
④生活污水经过净化处理后再排放。
(2)天然水中含有许多杂质,自来水生产过程中,常用过滤的方法除去水中悬浮的杂质,同时还必须进行消毒。ClO2是一种新型的自来水消毒剂,工业上用Cl2与NaClO2制取ClO2,另外得到一种常见的盐,写出该反应的化学方程式:_______。
(3)在化学实验和科学研究中,水也是一种常用的试剂,水分在特定条件下容易得到一个H+,形成水合氢离子(H3O+),下列对上述过程的描述不合理的是_________
A 氧元素发生了改变
B 微粒的组成发生了改变
C 微粒的化学性质发生了改变
D 与水分子比水合离子的电子数发生了改变
(4)肥皂主要成分硬脂酸钠(C17H35COONa):
①肥皂是一种有机酸的钠盐,在肥皂水中滴入盐酸会发生复分解反应出现沉淀,这沉淀物是__________________(写化学式);
②用肥皂水鉴别软水和硬水的原理是:肥皂水还能与硬水中的Ca2+或Mg2+反应生成沉淀,而不能产生气泡。硬脂酸钠与氯化钙反应的化学方程式为________。
③现有肥皂水溶液和三种等体积的待测溶液:A.蒸馏水B.0.1%氯化钙溶液 C.1%氯化钙溶液。试回答:检验这三种溶液应选用的方法是:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用数字和化学符号表示下列意义:
(1)2个硫原子___;
(2)3个氢分子___;
(3)氧化镁中镁元素的化合价为+2___;
(4)5个亚铁离子_________;
(5)10个硫酸根离子________;
(6)碳酸钠________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com