
 ij��ɫ���������к����������ƺ�̼�������������ʣ�ȡ14.6g�û�������������ε���10%��������Һ���������ռ���CO2���壨���跴Ӧ��CO2��ȫ�ݳ���4.4g
ij��ɫ���������к����������ƺ�̼�������������ʣ�ȡ14.6g�û�������������ε���10%��������Һ���������ռ���CO2���壨���跴Ӧ��CO2��ȫ�ݳ���4.4g���� ����̼������ϡ���ᷴӦ�Ļ�ѧ����ʽ���ɶ�����̼���������̼���Ƶ�����������������������ٸ��ݻ������̼���ƺ�������������֮�ͣ�����������Ƶ���������������������ϡ���ᷴӦ�Ļ�ѧ����ʽ���������������������������ߣ�
��� �⣺��1����������̼���Ƶ�����Ϊx����̼���Ʒ�Ӧ����������Ϊy��
Na2CO3+2HCl=2NaCl+H2O+CO2��
106 73 44
x y��10% 4.4g
$\frac{106}{x}$=$\frac{73}{y��10%}$=$\frac{44}{4.4g}$
�õ� x=10.6��y=73g
���������Ƶ�����Ϊm=14.6g-10.6g=4g
��2�������������Ʒ�Ӧ����������Ϊz
NaOH+HCl=NaCl+H2O
40 36.5
4g z��100%
z=36.5g
���Լ�������������Ͳ���������̼������֮��Ĺ�ϵ����Ϊ��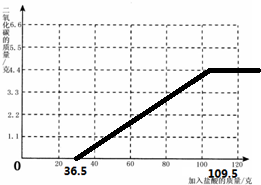
���� ������Ҫ����ѧ�����û�ѧ����ʽ����������������ʽ�ۺϷ����ͽ��ʵ�������������������ѧ�����������˼ά��ȣ�ǿ����ѧ������֪ʶ��������


 ���б�ˢ��ϵ�д�
���б�ˢ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
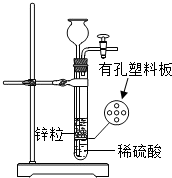 ͼΪʵ������ȡ�����ķ���װ�ã���Һ��պò���п���Ӵ���������Һ�ɼӣ�Ҫ�õ������Ҳ�Ӱ����������ȡ�����ɴӳ���©���м��������Լ���һ���ǣ�������
ͼΪʵ������ȡ�����ķ���װ�ã���Һ��պò���п���Ӵ���������Һ�ɼӣ�Ҫ�õ������Ҳ�Ӱ����������ȡ�����ɴӳ���©���м��������Լ���һ���ǣ�������| A�� | �٢ڢ� | B�� | �٢ڢ� | C�� | �٢ڢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ�Т٢� | B�� | ֻ�Т� | C�� | ֻ�Т� | D�� | ȫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����50%�Ķ������� | B�� | ������ | ||
| C�� | ��ˮ������ͭ���� | D�� | ����ˮ�����һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com