
【题目】学习了盐酸的性质后,小军归纳出盐酸的五条化学性质(如图)。
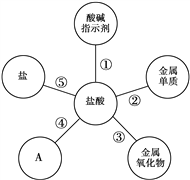
(1)为了验证性质①,小军将紫色石蕊溶液滴加到盐酸溶液中,溶液变______色;
(2)图中A所表示的物质类别是___________;试写出一个盐酸与该类别物质发生反应的化学方程式__________________________;
(3)为了验证性质⑤,可选用的物质是_______(填一种即可);
(4)镁和锌可以用来验证盐酸的性质②。现在小军要探究镁和锌与盐酸反应的快慢,下列因素不影响镁和锌与盐酸反应快慢的是_______(填序号);
A.盐酸的质量分数 B.温度
C.反应容器的大小 D.两种金属的形状
写出锌与盐酸发生反应的化学方程式_________________。
【答案】 红 碱, NaOH+HCl==NaCl+H2O(符合条件即可); 符合条件的盐即可; C Zn + 2HCl == ZnCl2 + H2↑
【解析】(1)紫色石蕊溶液遇盐酸变红。(2)盐酸有五条化学性质:与指示剂反应、与金属单质反应、与金属氧化物反应、与碱反应、与盐反应,故填碱。酸碱反应生成盐和水。(3)实验室可用稀盐酸与大理石(大理石主要成分是碳酸钙)反应来制取二氧化碳,CaCO3 + 2HCl == CaCl2 + H2O + CO2↑,可填碳酸钙。(4)A.盐酸的质量分数越大,反应速度越快,不符合题意;B.温度越高,反应速度越快,不符合题意;C.反应容器的大小与反应速度无关,符合题意;D.反应物之间接触面积越大,反应速度越快,不符合题意。故选C。锌与盐酸发生反应生成氯化锌和氢气。


 口算能手系列答案
口算能手系列答案科目:初中化学 来源: 题型:
【题目】氮元素广泛存在于自然界中,与人类生产和生活有着密切联系。
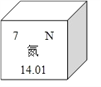
(1)在元素周期表中,氮元素的信息如图所示,氮元素在第______周期;
(2)氮元素的原子序数为7,其离子结构示意图为________;
(3)氮元素是蛋白质的重要组成元素之一,下列食物中,富含蛋白质的是______(填字母序号);
A.牛肉 B.鸡蛋清 C.西红柿 D.馒头 E.花生油
(4)农业生产中常用的化肥有氮、磷、钾肥,下列物质中属于氮肥的是___(填字母序号).
A.磷矿粉 B.熟石灰 C.草木灰 D.氨水 E.尿素
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用适当的化学方程式说明或解释下列问题:
(1)用石灰浆粉刷墙面,干燥后变得坚硬_______________________________
(2)服用Al(OH)3的药丸治疗胃酸过多症_________________________
(3)生活中铝锅表面易形成有较强的抗腐蚀性的氧化膜 _____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】完成下列变化的化学方程式,并按要求填空。
(1)镁条在空气中燃烧 _______________,点燃镁条时使用的夹持仪器是________。
(2)实验室用6%的过氧化氢溶液与二氧化锰混合制氧气_____________,6%的过氧化氢溶液中氢元素的质量分数为____________。(计算结果精确到0.1%)
(3)氨水与硫酸反应_______________________,生成的盐可用作________肥(填写化肥种类)。
(4)一氧化碳在高温下与氧化铁反应_______________,反应前后气体的化学计量数之比为_______________。
(5)受到猛烈撞击时,硝酸铵会迅速分解生成一氧化二氮气体和另一种氧化物___________,一氧化二氮中氮元素的化合价为____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水与人类的生活和生产密切相关。
(1)我国药学家屠呦呦因研制新型抗疟药青蒿素和双氢青蒿素而获得了诺贝尔奖。东晋名 医葛洪《肘后备急方》中就有青蒿素抗疟的记载:“青蒿一握,以水二升渍,绞取汁,尽服之”。这里的“水”作_____。上述水煎青蒿治疗疟疾,药性很不稳定,效果很差,屠呦呦改用乙醇提取,控温 60℃,药性显著提高,说明青蒿素具有的性质是(答一条):_____ 。
(2)利用下图甲所示装置净化河水,下列说法错误的是_____
A.活性炭层可除去异味和色素 B.此净化水的过程主要发生的是物理变化
C.此装置可以将硬水软化 D.利用此装置净化得到的水不宜直接饮用

(3)电解一定量的水(如上图乙),当负极端产生 10mL 气体时, 理论上在正极端产生气体的体积为_____mL。
(4)能说明水是由氢元素和氧元素组成的实验是_____(填序号)
A.氢气在氧气中的燃烧 B.氢气在氯气中的燃烧
C.水的净化 D.水的电解
(5)下图是 a、b、c 三种固体物质的溶解度曲线

①t2℃时,将等质量的 a、b 两种物质加水溶解配制成饱和溶液,所 得溶液质量的大小关系为:a_____b(填“>”、“<”或“=”)。
②t1℃时,将 60g 物质 a 的饱和溶液升温至 t2℃(溶剂量不变),至 少需要加入______g 物质 a 才能重新达到饱和状态。
③将 t2℃时 a、b、c 三种物质的饱和溶液降温至 t1℃,溶液中溶质 质量分数的大小关系是_____。
(6)若要配制 245g 溶质质量分数为 10%的稀硫酸,需要溶质质量 分数为 98%的浓硫酸(密度为 1.84g/cm3)_____mL(计算结果
保留一位小数)。实验室用浓硫酸配制稀硫酸的主要步骤有:计算、_____、混匀、 冷却至室温装瓶并贴上标签。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某反应前后分子变化的微观示意图如图所示,下列说法错误的是( )
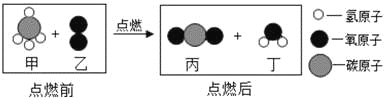
A. 生成物均为氧化物
B. 甲是有机物,乙、丙、丁是无机物
C. 点燃前,要先检验甲的纯度,防止爆炸
D. 参加反应的甲、乙微粒个数比为1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】地沟油中含有一种强烈致癌物黄曲霉素B2(C17H14O6),长期食用会引起消化道癌变,请回答:
(1)黄曲霉素B2的相对分子质量为 ;
(2)黄曲霉素B2中碳、氢、氧三种元素的原子个数比为 ;
(3)15.7g黄曲霉素B2中含有 g氧元素.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图是a、b、c、三种物质的溶解度曲线,回答下列问题:
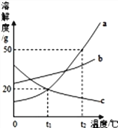
(1)t2℃,将30gA物质放入50g水中充分溶解得到溶液质量为_________。
(2)要从a、b、c混合物中分离出a,最好采用_______________方法。
(3)将t2℃时,等质量a、b、c三种饱和溶液降温到t1℃,所得溶液的质量由大到小的顺序是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学社团的同学发现,不同物质的变化常伴随着相同的实验现象。但从化学的角度去研究,会发现其有本质的区别。

【现象分析】
实验一:向盛有一定量氢氧化钠固体的试管里加入一定量的水,迅速用带导管的橡皮塞塞紧试管口,并将导管另一端通入盛有水的试管中,振荡左侧试管(如右图)。
实验二:用氧化钙代替氢氧化钠重复一次上述实验。
上述两个实验的相同现象之一是__________;
上述两个实验中,其中一个实验发生了化学变化,其化学方程式是__________;另一个实验没有发生化学变化。
【本质归纳】相同的实验现象,既可以由物理变化引起,也可以由化学变化引起。
【探究运用】在探究白色粉末的组成时,要研究相同实验现象的本质区别。
实验三:有一包白色粉末可能含有硫酸钡、碳酸钠和氢氧化钙中的一种或几种,取一定量该粉末加入到盛有足量水的烧杯中,搅拌,静置,观察到烧杯中有白色不溶物。
小奇同学查阅资料,得出碳酸钠的水溶液显___________(填“酸性”、“中性”或“碱性”)。
小明同学认为,白色粉末中一定含有硫酸钡;
小意同学认为小明的结论不准确,其理由是________________________________。
针对上述两位同学的观点,小燕同学进一步设计如下实验方案进行探究:

(1)步骤②中发生化学反应的方程式是_________________________________;
(2)步骤③中,加入酚酞溶液后,若溶液E为无色,则原白色粉末的组成是________(填化学式,下同);步骤③中,加入酚酞溶液后,若溶液E为红色,则滤液A中一定含有的溶质是_________。
(3)小鹏同学只做了一个实验,他取少量滤渣B,加入过量的稀硝酸,观察到___________现象,说明原白色粉末中含有碳酸钠、氢氧化钙二种固体。
(4)小鹏同学为进一步测定白色粉末的组成,进行了定量研究。他称取白色固体粉末10g,进行如流程所示实验,测得滤渣B的质量为5g,请你帮小鹏计算一下白色粉末中各成分的质量为________。(请写出具体计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com