
【题目】【2016年湖南省邵阳市】如图是汽车尾气有害物质转化的微观示意图:
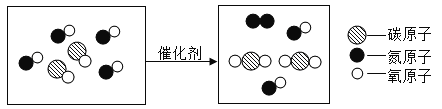
据图回答:
(1)该反应共涉及 种分子。
(2)在![]() 中“
中“![]() ”与“
”与“![]() ”的质量比是 (填最简整数比)。
”的质量比是 (填最简整数比)。
(3)写出该反应的化学方程式 。
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:初中化学 来源: 题型:
【题目】【2016年山东省威海市】 探究影响化学反应速率的因素
(1)发现和提出问题
镁在空气中能够剧烈燃烧,铁丝在氧气中能够剧烈燃烧,而真金不怕火炼,这说明决定物质之间能否发生反应以及反应速率的内因是 。
蜡烛在氧气中燃烧比在空气中燃烧剧烈,这一事例中影响化学反应速率的因素是 ;夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率。温度如何影响反应速率呢?
(2)猜想与假设:温度越高,反应速率越快。
(3)收集证据
实验药品:颗粒大小相同的锌粒;两份相同溶质质量分数、不同温度的稀硫酸(20℃、40℃)。
供选仪器:药匙、气体发生装置2套(气密性良好)、量筒2支、分液漏斗、秒表、胶头滴管、水槽、大试管2支。
利用上述仪器种药品,补充完成下表的实验报告。

该实验可以观察或测量的量有多种,除了上述观测点外,可以观察或测量的量还有(写一条) 等。
(4)结论与解释:从微观的角度分析“温度越高,应速率越快”的原因是 。
(5)拓展分析:根据其他测定方法,实验小组的同学绘制了锌粒与稀硫酸反应产生氢气的速率随时间变化的曲线,如图5所示。请据图分析:
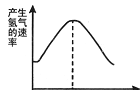
时间0—t内,反应速率逐渐加快的主要原因是 ,
时间t以后,反应速率逐渐减慢的主要原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关原子、分子、离子的说法正确的是( )
A.分子是保持物质性质的最小粒子 B.原子是化学变化中最小的粒子
C.分子可分,原子不可分 D.由离子构成的物质带有电荷
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】区别下列各组物质所选择的方法(或试剂)不正确的是( )
A.酱油和食醋——闻气味 B.呼出气体和吸入空气——澄清的石灰水
C.汞和氧化汞—— 看颜色 D.氮气和二氧化碳——燃着的木条
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对于下列几种化学符号,有关说法正确的是( )
①H②Fe2+③Cu④P2O5⑤Fe3+⑥NaCl
A.能表示一个分子的是①④⑥
B.表示物质组成的化学式是③④⑥
C.②⑤的质子数相同,化学性质也相同
D.④中的数字“5”表示五氧化二磷中有5个氧原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】【2016年山东省临沂市】某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分。
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是 。
Ⅰ.CaO Ⅱ.Ca(OH)2 Ⅲ.CaCO3 Ⅲ.Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是 。
【实验与事实】
实验 | 现象 | 解释或结论 | |
实验一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | Ca(OH)2微溶于水,其水溶液显碱性,能使紫色石蕊溶液变蓝色,不 变色说明水垢中一定没有 |
实验二 | 按如图所示方案进行实验
| 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 石灰水变浑浊,说明有CO2生成, 则水垢中一定含有 |
【原理与呈现】请用化学方程式表示实验二中有关反应的化学反应原理: , 。
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用 来检测饮用水是硬水还是软水。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】【2016年广东省 】小明在课外阅读中得知:氢氧化铜受热会分解生成氧化铜【Cu(OH)2==CuO+X】,于是用CuSO4溶液与KOH溶液反应制取氢氧化铜,并对氢氧化铜进行加热。
(1)生成物X的化学式为___________。
(2)制取氢氧化铜的化学方程式为______________________。
(3)小明在加热氢氧化铜时,发现蓝色固体先变成黑色;继续高温灼烧黑色固体变成红色,同时有气体产生。为弄清这种红色固体的成份,进行了如下的探究:
【查阅资料】Cu和Cu2O均为红色固体,且Cu2O+H2SO4=Cu+CuSO4+H2O。
【提出猜想】红色固体是:Ⅰ.Cu Ⅱ.Cu2O Ⅲ.______________________。
【进行实验】
操作 | 现象 | 结论 |
①取灼烧后的红色固体1.44g于试管中,加入足量稀硫酸,加热并充分震荡,静置。 | 溶液由无色变蓝色,固体减少。 | 1.44g红色固体一定有:______________________ |
②过滤、洗涤、干燥 | 得红色固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com