
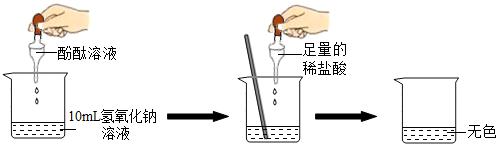
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量AgNO3的溶液 | 出现白色沉淀 | 稀HCl过量 |
| 方案二 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 稀HCl过量 |


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:初中化学 来源: 题型:
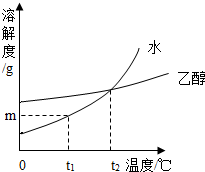
| A、物质甲能溶解在水和乙醇中 |
| B、t1℃时,物质甲在水中的溶解度为mg |
| C、t2℃时,物质甲在水中与在乙醇中的溶解度相同 |
| D、将t2℃时物质甲的水溶液降温至t1℃一定有晶体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| ① | 取四支试管,各取少量的A、B、C、D溶液,分别滴加紫色石蕊试液 | B溶液变红色,D溶液变成蓝色.A、C溶液都呈 | B是 D是 |
| ② | 另取两支试管,各取少量的A、C溶液,分别先滴入硝酸钡溶液后再滴入稀硝酸溶液. | A是硫酸钠溶液 C是 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
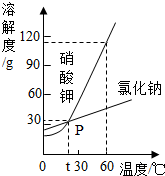 溶液在日常生活、工农业生产和科学研究中具有广泛的用途,与人们生活息息相关.以下是氯化钠和硝酸钾在不同温度时的溶解度及溶解度曲线.
溶液在日常生活、工农业生产和科学研究中具有广泛的用途,与人们生活息息相关.以下是氯化钠和硝酸钾在不同温度时的溶解度及溶解度曲线.| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com