
����Ŀ��FeSO47H2O��һ����Ҫ��ʳƷ���������Ӽ���ij��ҵ������Ҫ�ɷ���Fe2O3��������CaCO8��SiO2���Ȳ�����ˮҲ������ϡ���ᣩ��ʵ�����ô˷����Ʊ�FeSO47H2O��������ͼ1��

���������ͼ�ش��������⣺
��1��ϡ�������ĩ�е���������Ӧ�Ļ�ѧ����ʽΪ______________________
��2�������ڵ�������_______ ��
��3�����ⶨ��������ֻ����CaSO4��SiO2������Ϊʵ����___����ܡ����ߡ����ܡ����÷�ĩ״��ʯ��ʯ��ϡ���ᷴӦ��CO2.
��4���������ۺ���Ҫ����Ϊ���������ܽ⣬____________________ ��д��Fe��Fe2��SO4��3��Ӧ�Ļ�ѧ����ʽΪ__________________��
��5�������������ܽ��������ͼ2�����ᾧ��Ϻ��˳����壬��������ˮϴ��2��3�Σ��ñ�ˮϴ�ӵ�Ŀ���ǣ�

���ȥ������渽�ŵ����ʣ���___________________________________��
���𰸡� Fe2O3+3H2SO4=Fe2��SO4��3+3H2O�� ���ˣ� �� �����ݲ�������Һ��Ϊdz��ɫ�� Fe+Fe2��SO4��3=3FeSO4 ������������������ܽ⣻
��������(1)ϡ�������ĩ�е���������Ӧ��������������ˮ����ѧ����ʽΪ��Fe2O3+3H2SO4=Fe2(SO4)3+3H2O��(2)����Ŀ��ͼ���Կ��������������������Һ�壬�����Һ��������������������ǹ��ˣ�(3)��ҵ������Ҫ�ɷ���Fe2O3��������CaCO3��SiO2���Ȳ�����ˮҲ������ϡ���ᣩ������ϡ�������Ŀ��ָ���������ⶨ��������ֻ����CaSO4��SiO2����˵�������е�̼����Ѿ���ȫ��ϡ���ᷴӦ�������˶�����̼���壻(4)��ͼ��֪��Fe��Fe2(SO4)3��Ӧ����FeSO4����Ӧ����Fe��Fe2(SO4)3����������FeSO4���ʷ�Ӧ�Ļ�ѧ����ʽΪ��Fe+Fe2(SO4)3�T3FeSO4��(5)�����������ܽ��������ͼ1���Կ����������������ܽ�����¶ȵ����߶������ñ�ˮϴ�ӵ�Ŀ����һ����ȥ������渽�ŵ�����ˮ���ʣ�������ˮ���¶ȵͣ����������ڵ����µ��ܽ��С���ɽ���ϴ�ӹ������̷����ܽ����ɵ���ʧ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ļ�ѧʽΪH2C2O4���ס�����ͬѧ�Բ������ȷֽ����ļ�������̽����
(1)��������裺��һ�֣�����ֽ������CO2��H2���ڶ��֣�����ֽ������CO2��CO��H2O�������֣�����ֽ������CO2��H2O��
(2)ʵ��װ�õ����(ͼ������̨��ȥ)��ͬѧ�������ͼ1��ʾ��װ�á���ͬѧ�������ͼ2��ʾ��װ�á�
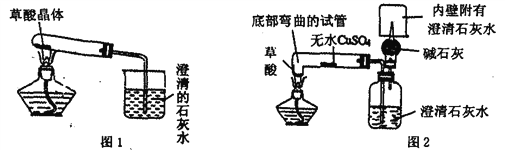
(3)ʵ�飺��ͬѧ��ͼ1װ��ʵ�飬�۲쵽����ʯ��ˮ����ǡ���ͬѧ��ͼ2װ��ʵ�飬�۲쵽��ˮ����ͭ�ɰ�ɫ�����ɫ�������ʯ��ˮ����ǣ������ɵ�����ͨ����ʯ�Һ��ڼ��촦��ȼ����ȼ�գ��ڻ����Ϸ���һ���ڱڸ��г���ʯ��ˮ���ձ��������ʯ��ˮ����ǡ�
(4)���ۣ���___�ֲ�������ȷ�ģ���д���������ȷֽ�Ļ�ѧ��Ӧ����ʽ__��
(5)��˼�����ۣ�
��ͬѧ��Ϊ��ͬѧ��Ƶ�ʵ��װ����ȱ�ݡ������Թܿ�������б�����Ҳ��ᾧ���۵�ϵͣ����ȵ�182��㿪ʼ�ۻ������ʵ���г���������ڵIJ����������ܶ�Ӱ�����ʵ�顣��ͬѧ��Ϊ��ͬѧ������ǿ�ѧ�����ġ�����̸̸ͼ2װ������ͼ1װ��֮����
��һ�㣺__________���ڶ��㣺_______________��
�����㣺_______________��
��ͬѧ��Ƶ�ͼ2װ��Ҳ��֤����������H2��֤��������______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п������п�Ĺ�������10.4g������89.8g��ϡ�����г�ֽ����ǡ����ȫ��Ӧ���õ�100g��Һ�����йط�Ӧ�Ļ�ѧ����ʽΪ��Zn + H2SO4 = ZnSO4 + H2���� ��
��1�����������غ㶨�ɣ����ɵ���������Ϊ_________g��
��2����Ӧ��������п�������Ƕ���? _________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C�������ʣ���֪A��һ���Ȼ��B��һ���ᣬC��һ�ּͼ�ױ�ʾA��B��C�������ʵ���Һ�������ʱ��ʵ��������ش�
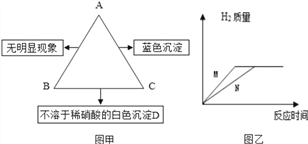
(1)D�Ļ�ѧʽΪ______________��
(2)A��C��Ӧ�Ļ�ѧ����ʽΪ____________��
(3)��һ������þ��п���ֽ���ͬʱ����A��Һ�г�ַ�Ӧ�����ˡ���ҺΪ��ɫ������Һ��һ�����е�������Ϊ_______(д���ӷ���)��
(4)��M��N�ֱ�Ϊ����п�е�һ�֣��ֱ��������������������������B��Һ��Ӧ�����������������뷴Ӧʱ��Ĺ�ϵ��ͼ����ʾ����Ӧ������ֻ��һ�ֽ�����ʣ�࣬��ʣ�����Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Ǽס��ҡ����������ʵ��ܽ�����ߣ�����˵������ȷ����
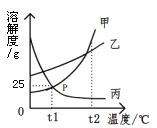
A. P���ʾ�ס����������ʵı�����Һ�������
B. t1��ʱ�������ʵı�����Һ��������t2��ʱ���DZ�����Һ
C. t1��ʱ�������ʵı�����Һ�����ʺ��ܼ���������Ϊ1��4
D. ���������ʵ���Һ��t2�潵��t1�棬��������������С��һ���DZ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ���ܺ������ᡢ���ᡢ�����ơ��Ȼ�ͭ�е�һ�ֻ��֣�Ϊ��̽������ɣ���һ�������ĸ���Һ����μ�������������Һ�����ɳ�������������������������Һ������֮��Ĺ�ϵ��ͼ��ʾ���������˵����ȷ���ǣ�����
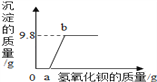
A. ��������������Һ����������������������ѧ��Ӧ
B. ��Ӧ�������ɵij���һ����������ͭ�����������ᱵ
C. ����Һһ���������ᡢ�Ȼ�ͭ�����ܺ���������
D. ����b��ʱ����������������Һ�����ʵ�������17.1g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I��A��B�������ʵ��ܽ��������ͼ����ʾ��
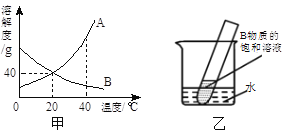
(1)20��ʱ��A���ʵ��ܽ��Ϊ____g��
(2) 40��ʱ����40 g A���ʷ���100 gˮ�У�������Һ��________(ѡ����������������������)��Һ��
(3) 20��ʱ��A���ʱ�����Һ�����ʵ���������Ϊ_________��
(4)����ͼ��ʾ��20��ʱ����ʢ��B���ʱ�����Һ��С�Թܷ���ʢˮ���ձ��У���ˮ�м���ij�����ʺ��Թ����о�����������������ʿ�����____________��
II����ͼ������Ԫ�ص�ԭ�ӽṹʾ��ͼ�����У������������ơ��ݴ˻ش�
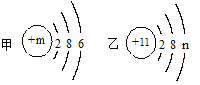
(1)m��_________����������ԭ���У�______ԭ���ڻ�ѧ��Ӧ�����õ����ӣ��γ����ӣ������ӷ�����_________��
(2)��������Ԫ���γɻ�����Ļ�ѧʽΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����ѧϰ��ѧ��һ����Ҫ;�������ͼ�ش��������⡣
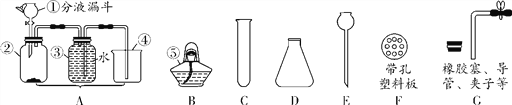
(1)ͼ�������ܵ����ƣ�________��
(2)ʵ������ȡ������ijͬѧ�����ͼA�����װ�á���������������ʢ�ŵ�����Ӧ��________��
(3)ʵ������ȡ������̼����B��G��ѡ����������װ����װ����Ҫ������ʱ���Ʒ�Ӧ�ķ�����ֹͣ������Ϊ��Ҫ��������________(����ĸ)��
(4)ʵ���Ҽ��������̼�Ļ�ѧ��Ӧ����ʽΪ__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ�ش����⡣
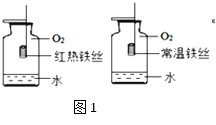

(1)��ͼ1���۲쵽��������_____________________����Ӧ�Ļ�ѧ����ʽ��___________��ƿ��������ˮ��Ŀ����_______________��ͨ��ʵ���֪����ȼ��ȼ�յ�������____________��
(2)��ͼ2����֤CO2��NaOH��Ca(OH)2���ܷ�����Ӧ���ֱ���ס�������ƿ��ע���������������������Һ���۲�ʵ������
I�����з�Ӧ�Ļ�ѧ����ʽ��___________��˵��CO2����Ca(OH)2��Ӧ��ʵ��������__________��
II������ʵ�������У�һ����˵����CO2��NaOH�����˻�ѧ��Ӧ������_____(�����)��
a��U���к�īˮ����Ҹ� b��U���к�īˮ����ҵ� c��U���к�īˮҺ��û�з����ı�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com