
【题目】某班同学在学习了铁的冶炼后,欲探究炼铁高炉气体中有害气体的成分。于是他们分成甲乙两个小组,收集炼铁高炉不同时间段的气体进行探究。回答下列问题。
已知:高炉气体中一定含有二氧化碳、氮气、极少量的氧气、稀有气体等,还可能含有一氧化碳、二氧化硫等有害气体。
[提出问题]高炉气体中的有害成分是什么?
[作出猜想]猜想一:只有CO; 猜想二:只有 SO2; 猜想三:CO 和SO2都有。
甲实验小组
[查阅资料]SO2与CO2具有许多相似的化学性质:
①都能与水反应。![]() (亚硫酸);
(亚硫酸);
②SO2也能使澄清石灰水变浑浊,生成亚硫酸钙(CaSO3)白色沉淀;
③都能与氢氧化钠溶液反应,分别生成可溶性的碳酸钠、亚硫酸钠(Na2SO3)和水。
不同之处:二氧化硫能使红色品红溶液褪色,可被酸性高锰酸钾溶液吸收。
[实验探究]甲组同学设计组装如下装置进行实验。
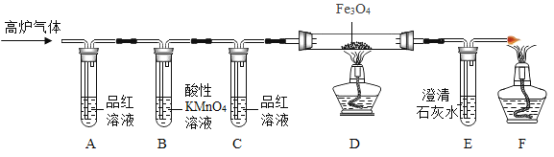
(1)A中品红溶液的作用是检验二氧化硫,B中酸性高锰酸钾溶液的作用是_____,C中品红溶液的作用是_____。
(2)观察现象发现:A中品红溶液褪色,C中品红溶液不褪色,E中澄清石灰水变浑浊。
得出结论:高炉气体中含有SO2和CO。
反思评价:部分同学认为上述结论不够准确,理由是_____。
[实验改进]同学们经过讨论后,在原有基础上改进了实验装置,如下图所示。
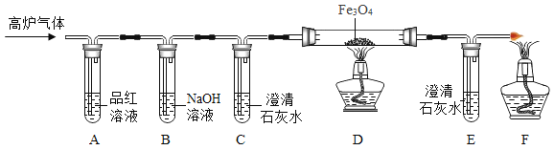
(3)用氢氧化钠溶液代替酸性高锰酸钾溶液的优点是_____,写出二氧化硫与氢氧化钠溶液反应的化学方程式_____。
乙实验小组
[查阅资料]一氧化碳能与红色氯化钯(PdCl2)溶液反应,生成黑色的金属钯(Pd)沉淀、盐酸和二氧化碳。
[实验探究]乙组同学设计如下实验装置并进行实验。
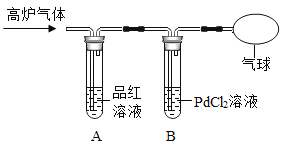
(4)B中反应的化学方程式为_____,结合已有知识和该反应可以判断:金属钯的活动性比铁_____,(填“强”或“弱”)。
[实验结论]炼铁厂排放的高炉气体中含有CO和SO2,直接排放会造成大气污染,需净化达标后才能排放。
[延伸拓展]二氧化硫排放到空气中会导致酸雨。二氧化硫与水反应生成亚硫酸,亚硫酸会被氧气进一步氧化生成硫酸。
为了研究酸雨的危害,同学们设计了如下实验探究:
②将硫燃烧的产物溶于水后,通入氧气,用所得溶液模拟硫酸型酸雨。
②模拟实验如下:
实验序号 | 所加物质 | 实验现象 |
1 | 树叶、果皮 | 树叶、果皮被腐蚀 |
2 | 细铁丝、镁条 | 产生气泡 |
3 | 石灰石、大理石碎片 | 产生气泡 |
实验结论:酸雨具有较强的危害性。
反思评价:
(5)实验室制取二氧化碳时,不能使用大理石与稀硫酸反应,但硫酸型酸雨却能腐蚀大理石雕像,其原因是_____。
(6)同学们经过讨论认为,酸雨还会加剧“温室效应”。这种说法的依据是_____。
【答案】吸收(除去)气体中的二氧化硫 检验二氧化硫是否除尽 原有气体中的二氧化碳会对CO的检验产生干扰(或)原来气体中的CO2也会使E中的澄清石灰水变浑浊 氢氧化钠溶液可以同时除去(吸收)CO2和SO2(或:可以排除原来的二氧化碳会对CO检验产生的干扰) ![]()
![]() 弱 雨水会将生成的硫酸钙冲刷掉,使得硫酸能与大理石继续反应 酸雨能与自然界中存在的碳酸盐(如碳酸钙)反应生成二氧化碳
弱 雨水会将生成的硫酸钙冲刷掉,使得硫酸能与大理石继续反应 酸雨能与自然界中存在的碳酸盐(如碳酸钙)反应生成二氧化碳
【解析】
(1)根据“二氧化硫能使红色品红溶液褪色,可被酸性高锰酸钾溶液吸收”可知,A中品红溶液的作用是检验二氧化硫,B中酸性高锰酸钾溶液的作用是吸收(除去)气体中的二氧化硫,C中品红溶液的作用是检验二氧化硫是否除尽;
(2)乙同学发现C中品红溶液没有褪色,E中澄清石灰水变浑浊,得出高炉气体中含有CO,丙同学认为乙同学的结论不正确,理由是原有气体中的二氧化碳会对CO的检验产生干扰(或)原来气体中的CO2也会使E中的澄清石灰水变浑浊;
(3)用氢氧化钠溶液代替酸性高锰酸钾溶液的优点是氢氧化钠溶液可以同时除去(吸收)CO2和SO2(或:可以排除原来的二氧化碳会对CO检验产生的干扰);SO2与NaOH溶液反应生成亚硫酸纳和水,反应的化学方程式为:![]() ;
;
(4)根据“一氧化碳能与红色氯化钯(PdCl2)溶液反应,生成黑色的金属钯(Pd)沉淀、盐酸和二氧化碳”可知,B中反应的化学方程式为![]() ;常温下CO能将Pd还原出来,高温条件下,CO能将铁还原出来,可以判断:金属钯的活动性比铁弱;
;常温下CO能将Pd还原出来,高温条件下,CO能将铁还原出来,可以判断:金属钯的活动性比铁弱;
(5)实验室制取二氧化碳时,不能使用大理石与稀硫酸反应,但硫酸型酸雨却能腐蚀大理石雕像,其原因是雨水会将生成的硫酸钙冲刷掉,使得硫酸能与大理石继续反应;
(6)同学们经过讨论认为,酸雨还会加剧“温室效应”。这种说法的依据是酸雨能与自然界中存在的碳酸盐(如碳酸钙)反应生成二氧化碳。


 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:初中化学 来源: 题型:
【题目】用如图装置进行实验。升温至70°C的过程中,仅①燃烧;继续升温至280°C的过程中, 仅③燃烧。下列分析不正确的是
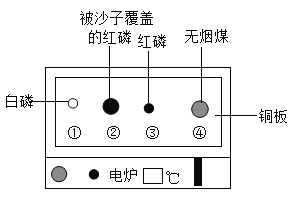
A.①③燃烧,说明白磷和红磷是可燃物
B.④未燃烧,说明无烟煤不是可燃物
C.对比①③,可说明红磷的着火点比白磷的高
D.对比②③,可验证燃烧需可燃物与氧气按触
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究金属活动性顺序,学习小组设计并进行实验I和Ⅱ,实验结束,将两实验的废液全部倒入一洁净烧杯中,实验过程及现象如下图所示:
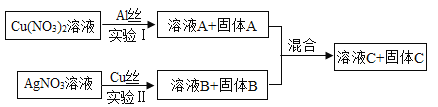
(1)实验I中反应的化学方程式为__________:
(2)实验Ⅱ中的实验现象为_________;
(3)若溶液C为蓝色,则溶液C中一定含有的溶质为__________;若溶液C为无色,则固体A的成分为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)食醋中的主要成分是醋酸(CH3COOH)、水和氯化钠。
①其中醋酸中碳元素与氧元素的质量比为________,
②1个醋酸分子中含有氢原子的个数为______,
③氯化钠是由阴离子和阳离子结合成的,其中阴离子符号为___。
(2)根据如图的原子结构示意图判断,该元素的原子的核电荷数为_____,在化学反应中这种原子容易得___个电子,形成氯离子。
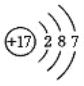
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学让世界变得更加美好。请用化学用语回答下列问题:
(1)人体中含量最多的金属元素是_____;
(2)保持氨气化学性质的最小粒子是_____;
(3)补铁剂乳酸亚铁中含有的阳离子是_____;
(4)家用天然气完全燃烧的化学方程式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室一些常见的仪器和装置,请回答有关问题。
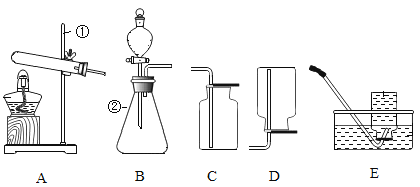
(1)仪器①的名称是_____________。
(2)实验室加热高锰酸钾制取氧气的化学方程式为_____________,选择的发生装置是_____(填字母),收集装置是____________。
(3)氨气是一种无色、有强烈刺激性气味的气体,密度比空气小,极易溶于水,实验室常用加热氯化铵(NH4C1)和熟石灰(Ca(OH)2)固体混合物的方法制取氨气,反应生成氯化钙、氨气和水,则制取氨气的装置组合是___________,NH4C1中氮元素的化合价是__________,该反应的化学方程式为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】山西的酒文化驰名中外。陈年老酒,醇香四溢。从微观角度解释这一现象:_____。我国的茶文化博大精深,绿茶中的单宁酸(化学式为C76H52O46)具有抑制血压上升、清热解毒等功效,单宁酸的相对分子质量是_____,其中质量分数最大的元素是_____(填元素符号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石为原料生产二水化钙(CaCl2·2H2O)的流程如下。原料石灰石中含有杂质主要是MgCO3、MgSO4和Al2O3。
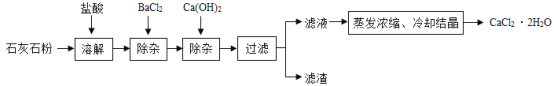
(1)石灰石粉溶解时,Al2O3发生反应的化学方程式为______________。
(2)加入BaCl2除去的杂质离子是__________;加入Ca(OH)2除去的杂质离子是________。
(3)检验“滤液”酸碱性,如果显碱性,还需加入适量的___________________(填化学式)提高产品纯度。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】探究醋蛋液
食用醋蛋液可以补充人体所需营养,做法(如下图):

将洗净的鸡蛋放入盛有7°白醋的玻璃杯中,放置3天左右,用筷子将蛋清与蛋黄打散即可。
(查阅资料)
食醋的主要成分为醋酸(CH3COOH),醋酸在水中能解离出H+和CH3COO-。
(提出问题)I.产生的气体是什么?
小英按照制作说明进行操作,把鸡蛋放入白醋中,观察到蛋壳逐渐溶解,表面有大量气泡产生,她对产生的气体进行了如下猜想:
(猜想与假设)
猜想1:二氧化碳 猜想2:氢气猜想 3:甲烷
(1)小英运用的观察方法是___________(填“直接”或“间接”)观察,小英在观察的基础上作出以上猜想的理论依据是____________。
(2)假设是利用已有的知识和经验进行加工处理形成的一种能被检验的假设性结论,其表述方式为:如果……,那么……针对以上任一种猜想做出你的假设:___________。
(获得结论)实验证明,产生的气体为二氧化碳。写出二氧化碳与澄清石灰水反应的化学方程式:_____________。
(反思与交流)
(3)将鸡蛋放入白醋中,蛋壳中的碳酸钙和醋酸作用生成可溶性的醋酸钙,可以补充人体所需钙元素。
II.醋蛋液中是否含有醋酸?
(实验探究)小英同学通过测定醋蛋液的酸碱度来确定其中是否含有醋酸,请将下表填写完整。
实验操作 | 实验现象及结论 |
________。 | 现象:_________。 结论:醋蛋液中含有醋酸。 |
(反思与交流)
(4)制得的醋蛋液中如果有过量的醋酸会为伤、腐蚀食道黏膜及损伤脾胃,食用时可加一定量的水进行稀释,加水稀释过程中醋蛋液的pH____________(填“增大”,“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com